Большинство прокариот способны синтезировать все аминокислоты, входящие в состав клеточных белков. В качестве исходных углеродных скелетов для биосинтеза аминокислот служит небольшое число промежуточных соединений различных метаболических путей (табл. 10). Введение в молекулу некоторых из них (щавелевоуксусной, -кетоглутаровой, пировиноградной кислот) аминного азота приводит к образованию аспарагиновой, глутаминовой кислот и аланина. Однако в большинстве случаев исходные соединения должны подвергнуться значительным перестройкам, чтобы сформировать углеродный остов молекулы будущей аминокислоты.
Таблица 10. Некоторые особенности биосинтеза аминокислот
| Предшественник | Метаболический путь, приводящий к образованию предшественника | Аминокислоты с общими биосинтетическими путями |
| Щавелевоуксусная кислота | цикл трикарбоновых кислот реакции карбоксилирования | аспарагиновая кислота аспарагин лизин метионин треонин изолейцин |
| -Кетоглутаровая кислота | цикл трикарбоновых кислот | глутаминовая кислота глутамин аргинин пролин |
| 3-фосфоглицериновая кислота | гликолиз цикл Кальвина | серин глицин цистеин |
| Пировиноградная кислота | гликолиз путь Энтнера-Дудорова | аланин валин лейцин |
| Фосфоенолпировиноградная кислота + Эритрозо-4-фосфат | гликолиз окислительный пентозофосфатный путь | триптофан тирозин фенилаланин |
| 5-Фосфорибозил-1-пирофосфат + АТФ | окислительный пентозофосфатный путь | гистидин |
Особенностью биосинтеза аминокислот является использование общих биосинтетических путей. Так, 19 из 20 аминокислот, входящих в состав белков, можно по способу их происхождения разделить на 5 групп. Только одна аминокислота (гистидин) образуется по отдельному биосинтетическому пути. Азот вводится в молекулу аминокислоты посредством реакций аминирования, амидирования и переаминирования. Реакции аминирования приводят к образованию из пировиноградной кислоты аланина, а из -кетоглутаровой — глутаминовой кислоты, например:
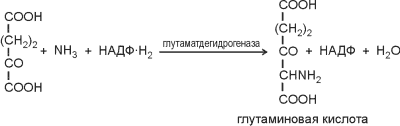 |
Две реакции амидирования ведут к образованию глутамина и аспарагина из глутаминовой и аспарагиновой кислот в реакциях следующего типа:
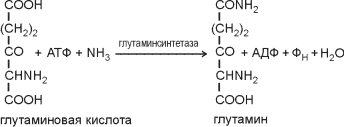 |
где Фн — неорганический фосфат. Глутаминовая кислота и глутамин прямо или косвенно служат донорами амино- и амидогрупп при синтезе практически всех аминокислот и других азотсодержащих органических соединений. Аспарагин используется только для синтеза белковых молекул. Во все остальные аминокислоты азот вводится посредством реакций переаминирования, катализируемых соответствующими аминотрансферазами, при этом во всех реакциях одним из участников является глутаминовая кислота:
глутаминовая кислота + щавелевоуксусная кислота аспарагиновая кислота + -кетоглутаровая кислота.
Еще одним путем включения азота аммиака в состав органических соединений является реакция, приводящая к образованию карбамоилфосфата:
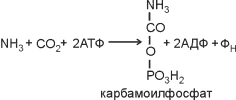 |
Дальнейшее использование азота карбамоилфосфата происходит по двум путям: для синтеза пиримидинов и аргинина.
 2015-06-16
2015-06-16 1728
1728
