ДОПОЛНИТЕЛЬНАЯ ЛИТЕРАТУРА
ОСНОВНАЯ ЛИТЕРАТУРА
1. Пасынков В.В., Сорокин В.С. Материалы электронной техники. - М.: Высш.шк., 1986. - 367 с.
2. Богородицкий Н.П., Пасынков В.В., Тареев Б.Н. Электротехнические материалы. - Л.: Энергоатомиздат, 1985. - 304 с.
3. Материалы микроэлектронной техники./ Андреев В.М., Бронгулеева А.Н., Дацко С.Н., Яманова Л.В. – М.:Радио и связь, 1989. – 352 с.
4. Штофа Ян Электротехнические материалы в вопросах и ответах. -М. Энергоатомиздат, 1984. – 200 с.
5. Справочник по электротехническим материалам. В 3 –х томах.
Т.1/ Под ред. Ю.Б.Корицкого и др.-М.:Энергоатомиздат,1986. – 368 с.
Т.2/ Под ред. Ю.Б.Корицкого и др.-М.:Энергоатомиздат,1987. – 464 с.
Т.3/ Под ред. Ю.Б.Корицкого и др.-Л.:Энергоатомиздат,1988. – 728 с.
Чрезвычайно широкое распространение трансаминаз в животных тканях, у микроорганизмов и растений, их высокая резистентность к физическим, химическим и биологическим воздействиям, абсолютная стереохимическая специфичность по отношению к L-аминокислотам, а также высокая каталитическаяактивность в процессах трансаминирования послужили предметом детального исследования роли этихферментов в обмене аминокислот. Ранее было указано, что при физиологических значениях рН средыактивность оксидазы L-аминокислот резко снижена. Учитывая это обстоятельство, а также высокую скорость протекания реакции трансами-нирования, А.Е. Браунштейн выдвинул гипотезу о возможности существования в животных тканях непрямого пути дезаминирования аминокислот через реакции трансаминирования, названного им трансдезаминированием. Основой для выдвижения этой гипотезы послужили также данные Г. Эйлера о том, что в животных тканях из всех природных аминокислот с высокой скоростью дезаминируется только L-глутаминовая кислота в реакции, катализируемой высокоактивной и специфической глутамат-дегидрогеназой.
Согласно гипотезе, получившей экспериментальное подтверждение, все или почти все природныеаминокислоты (исключение составляет метионин) сначала реагируют с α-кетоглутаровой кислотой в реакциитрансами-нирования с образованием глутаминовой кислоты и соответствующей кетокислоты. Образовавшаяся глутаминовая кислота затем подвергается непосредственному окислительномудезаминированию под действием глу-таматдегидрогеназы. Схематически механизм трансдезаминирования можно представить в следующем виде:
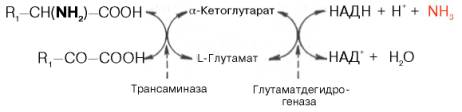
Суммарная реакция при этом следующая:
R,—CH(NH2)—COOH + НАД++H20-> R,— CO —СООН + НАДН2 + NH3.
Поскольку обе реакции (трансаминирование и дезаминирование глу-таминовой кислоты) являются обратимыми, создаются условия для синтеза по существу любой аминокислоты, если в организме имеются соответствующие α-кетокислоты. Известно, что организм животных и человека не наделен способностью синтеза углеродных скелетов (α-кетокислот), так называемых незаменимых аминокислот; этой способностью обладают только растения и многие микроорганизмы.
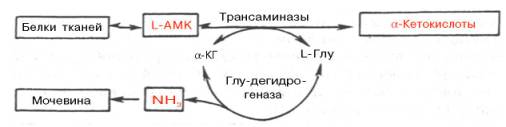
Рис. 12.4. Центральная роль трансаминаз L-аминокислот и глутаматдегидрогеназы в биосинтезе и распадеаминокислот в тканях животных. АМК - аминокислоты; α-КГ - α-кетоглутарат.
Механизм, при помощи которого в живых организмах осуществляется синтез природных аминокислот из α-кетокислот и аммиака, был назван А.Е. Браунштейном трансреаминированием. Сущность его сводится квосстановительному аминированию α-кетоглутаровой кислоты с образованием глутаминовой кислоты(реакцию катализирует НАДФ-зависимая глута-матдегидрогеназа, работающая в режиме синтеза) и к последующему трансаминированию глутамата с любой α-кетокислотой. В результате образуется L-аминокислота, соответствующая исходной кетокислоте, и вновь освобождается α-кетоглутаровая кислота, которая может акцептировать новую молекулу аммиака. Роль реакций трансаминирования как вдезаминировании, так и в биосинтезе аминокислот может быть представлена в виде схемы:
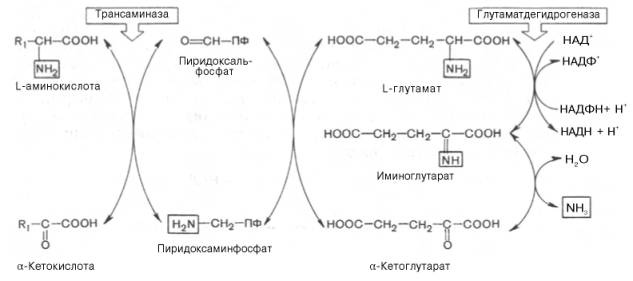
Таким образом, трансаминазы катализируют опосредованное через глутаматдегидрогеназу дезаминированиеприродных аминокислот (черные стрелки) и биосинтез аминокислот (красные стрелки). В более упрощенной форме роль этих ключевых ферментов азотистого обмена представлена на рис. 12.4.
Получены доказательства существования в организме теплокровных животных еще одного механизма непрямого (опосредованного) дезами-нирования L-аминокислот, при котором Глу, Асп и АМФ выполняют роль системы переноса NН2-группы; гидролитическое дезаминирование АМФ приводит к образованию инозинмонофосфата (ИМФ) и аммиака:
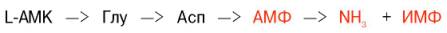
Возможно, что в аналогичной системе в качестве промежуточного переносчика NH2-группы вместо АМФучаствует НАД.
Клиническое значение определения активности трансаминаз. Широкое распространение и высокаяактивность трансаминаз в органах и тканях человека, а также сравнительно низкие величины активности этихферментов в крови послужили основанием для определения уровня ряда трансаминаз в сыворотке кровичеловека при органических и функциональных поражениях разных органов. Для клинических целей наибольшее значение имеют две трансаминазы – аспартат-аминотрансфераза (AcAT) и аланин-аминотрансфераза (АлАТ), катализирующие соответственно следующие обратимые реакции:
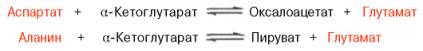
В сыворотке крови здоровых людей активность этих трансаминаз в тысячи раз ниже, чем в паренхиматозных органах. Поэтому органические поражения при острых и хронических заболеваниях, сопровождающиеся деструкцией клеток, приводят к выходу трансаминаз из очага поражения в кровь. Так, уже через 3–5 ч после развития инфаркта миокарда уровень АсАТ в сыворотке крови резко повышается (в 20–30 раз). Максимумактивности обеих трансаминаз крови приходится на конец первых суток, а уже через 2–3 дня при благоприятном исходе болезни уровень сывороточных трансаминаз возвращается к норме. Напротив, при затяжном процессе или наступлении повторного инфаркта миокарда наблюдается новый пик повышенияактивности этих ферментов в крови. Этим объясняется тот факт, что в клинике трансаминазный тестиспользуется не только для постановки диагноза, но и для прогноза и проверки эффективности лечения. При поражениях клеток печени, например при гепатитах, также наблюдается гипертрансаминаземия (за счет преимущественного повышения уровня АлАТ), но она имеет более умеренный и затяжной характер, а повышение активности трансаминазы в сыворотке крови происходит медленно. При различного рода коронарной недостаточности (стенокардия, пороки сердца и др., кроме инфаркта миокарда) гипертрансаминаземия или не наблюдается, или незначительна. Определение активности трансаминаз всыворотке крови при заболеваниях сердца следует отнести к дифференциально-диагностическим лабораторным тестам. Повышение уровня трансаминаз в сыворотке крови отмечено, кроме того, при некоторых заболеваниях мышц, в частности при обширных травмах, гангрене конечностей и прогрессивной мышечной дистрофии.
Превращения α-кетокислот. Образовавшиеся в процессе дезаминиро-вания и трансдезаминирования α-кетокислоты подвергаются в тканях животных различным превращениям и могут вновь трансаминироваться с образованием соответствующей аминокислоты. Это так называемый синтетический путь превращения. Опыты с перфузией растворов α-кето-кислот и аммиака через изолированную печень показали, что в оттекающей из печени жидкости действительно имеются соответствующие исходным кетокислотам L-аминокислоты. Открыты, кроме того, гликогенные, кето-генные и окислительные пути, ведущие к образованию соответственно глюкозы, жирных кислот, кетоновых тел и компонентов цикла трикарбо-новых кислот (ЦТК). Эти процессы можно представить в виде общей сводной схемы:
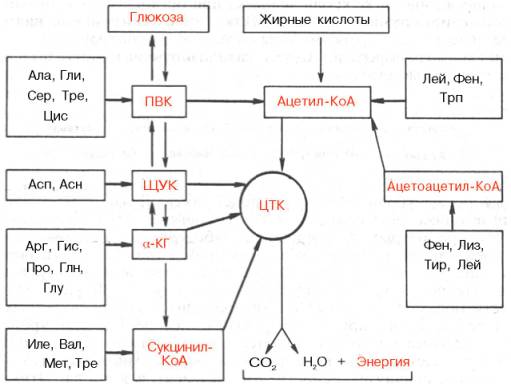
Углеродные скелеты аминокислот могут включаться в ЦТК через ацетил-КоА, пируват, оксалоацетат, α-кетоглутарат и сукцинил-КоА. Пять аминокислот (Фен, Лиз, Лей, Трп, Тир) считаются «кетогенными», поскольку они являются предшественниками кетоновых тел, в частности ацетоуксусной кислоты, в то время как большинство других аминокислот, обозначаемых как «гликогенные», служат в организме источникомуглеводов, в частности глюкозы. Подобный синтез углеводов de novo усиливается при некоторых патологических состояниях, например при сахарном диабете, а также при гиперфункции коркового веществанадпочечников и введении глюкокортикоидов (см. главу 8). Разделение аминокислот на «кетогенные» и «гликогенные» носит, однако, условный характер, поскольку отдельные участки углеродных атомов Лиз, Трп,Фен и Тир могут включаться и в молекулы предшественников глюкозы, например Фен и Тир – в фумарат. Истинно «кетогенной» аминокислотой является только лейцин.
роцесс отщепления карбоксильной группы аминокислот в виде СО2 получил название декарбоксилирования. Несмотря на ограниченный круг аминокислот и их производных, подвергающихся декарбоксилиро-ванию в животных тканях, образующиеся продукты реакции – биогенные амины – оказывают сильное фармакологическое действие на множество физиологических функций человека и животных. В животных тканяхустановлено декарбоксилирование следующих аминокислот и их производных: тирозина, триптофана, 5-окситриптофана, валина, серина, гистидина, глу-таминовой и γ-оксиглутаминовой кислот, 3,4-диоксифенилаланина, цис-теина, аргинина, орнитина, S-аденозилметионина и α-аминомалоновой кислоты. Помимо этого, у микроорганизмов и растений открыто де-карбоксилирование ряда других аминокислот.
В живых организмах открыты 4 типа декарбоксилирования аминокислот:
1. α-Декарбоксилирование, характерное для тканей животных, при котором от аминокислот отщепляетсякарбоксильная группа, стоящая по соседству с α-углеродным атомом. Продуктами реакции являются СО2 и биогенные амины:
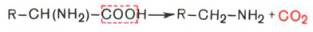
2. ω-Декарбоксилирование, свойственное микроорганизмам. Например, из аспарагиновой кислоты этим путем образуется α-аланин:

3. Декарбоксилирование, связанное с реакцией трансаминирования:
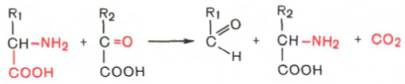
В этой реакции образуются альдегид и новая аминокислота, соответствующая исходной кетокислоте.
4. Декарбоксилирование, связанное с реакцией конденсации двух молекул:
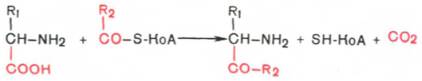
Эта реакция в тканях животных осуществляется при синтезе δ-амино-левулиновой кислоты из глицина и сукцинил-КоА (см. главу 13) и при синтезе сфинголипидов, а также у растений при синтезе биотина.
Реакции декарбоксилирования в отличие от других процессов промежуточного обмена аминокислот являются необратимыми. Они катализируются специфическими ферментами – декарбоксилазами аминокислот, отличающимися от декарбоксилаз α-кетокислот (см. главу 10) как белковым компонентом, так и природойкофермента. Декарбоксилазы аминокислот состоят из белковой части, обеспечивающей специфичностьдействия, и простетической группы, представленной пиридоксальфосфатом (ПФ), как и у трансаминаз.
Таким образом, в двух совершенно различных процессах обмена аминокислот участвует один и тот жекофермент. Исключение составляют две декарбоксилазы: гистидиндекарбоксилаза Micrococcus и Lactobacilus и аденозилметионин-декарбоксилаза Е. coli, содержащие вместо ПФ остаток пировиноградной кислоты.
Механизм реакции декарбоксилирования аминокислот в соответствии с общей теорией пиридоксалевогокатализа (см. рис. 12.3) сводится к образованию ПФ-субстратного комплекса, представленного, как и вреакциях трансаминирования, шиффовым основанием ПФ и аминокислоты:
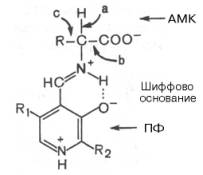
Образование подобного комплекса в сочетании с некоторым оттягиванием электронов белковой частьюмолекулы фермента сопровождается лабилизацией одной из трех связей при α-углеродном атоме, благодаря чему аминокислота способна вступать в реакции трансаминирования (а), декарбоксилирования (b) и альдольного расщепления (с).
Далее представлены отдельные примеры декарбоксилирования аминокислот, в частности тех, продуктыреакции которых оказывают сильное фармакологическое действие. Одним из хорошо изученных ферментовявляется декарбоксилаза ароматических аминокислот. Она не обладает строгой субстратнойспецифичностью и катализирует декарбок-силирование L-изомеров триптофана, 5-окситриптофана и 3,4-диоксифе-нилаланина (ДОФА); продуктами реакций, помимо СО2, являются соответственно триптамин,серотонин и диоксифенилэтиламин (дофамин).
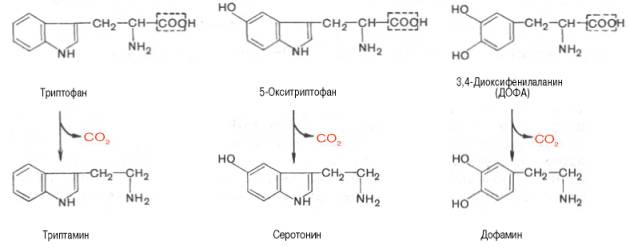
Декарбоксилаза ароматических аминокислот получена в чистом виде (мол. масса 112000), кофермент – ПФ. В больших количествах она содержится в надпочечниках и ЦНС, играет важную роль в регуляции содержания биогенных аминов. Образующийся из 5-окситриптофана серо-тонин оказался высокоактивным биогеннымамином сосудосуживающего действия. Серотонин регулирует артериальное давление, температуру тела,дыхание, почечную фильтрацию и является медиатором нервных процессов в ЦНС. Некоторые авторы считают серотонин причастным к развитию аллергии, демпинг-синдрома, токсикоза беременных, карциноидного синдрома и геморрагических диатезов.
Продукт декарбоксилазной реакции дофамин является предшественником катехоламинов (норадреналина иадреналина). Источником ДОФА в организме является тирозин, который под действием специфической гидроксилазы превращается в 3,4-диоксифенилаланин (см. главу 8). Тиро-зин-3-монооксигеназа открыта в надпочечниках, ткани мозга и периферической нервной системы. Простетической группой тирозин-моноокси-геназы, как и дофамин-монооксигеназы (последняя катализирует превращение дофамина в норадреналин) является тетрагидробиоптерин, имеющий следующее строение:
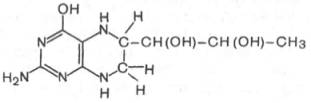
Физиологическая роль тирозин-3-монооксигеназы чрезвычайно велика, поскольку катализируемая этимферментом реакция определяет скорость биосинтеза катехоламинов, регулирующих деятельность сердечно-сосудистой системы. В медицинской практике широко используются ингибиторы декарбоксилазы ароматических аминокислот, в частности α-метилдофа (альдомет), вызывающий снижение артериальногодавления.
В животных тканях с высокой скоростью протекает декарбоксилиро-вание гистидина под действием специфической декарбоксилазы.
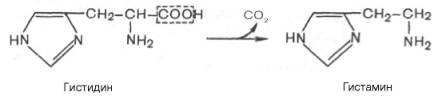
Гистамин оказывает широкий спектр биологического действия. По механизму действия на кровеносные сосудыон резко отличается от других биогенных аминов, так как обладает сосудорасширяющим свойством. Большое количество гистамина образуется в области воспаления, что имеет определенный биологический смысл. Вызывая расширение сосудов в очаге воспаления, гистамин тем самым ускоряет приток лейкоцитов, способствуя активации защитных сил организма. Кроме того, гистамин участвует в секреции соляной кислотыв желудке, что широко используется в клинике при изучении секреторной деятельности желудка (гистаминовая проба). Он имеет прямое отношение к явлениям сенсибилизации и десенсибилизации. При повышенной чувствительности к гистамину в клинике используют антигистаминные препараты (санорин,димедрол и др.), оказывающие влияние на рецепторы сосудов. Гистамину приписывают также рольмедиатора боли. Болевой синдром – сложный процесс, детали которого пока не выяснены, но участие в немгистамина не подлежит сомнению.
В клинической практике широко используется, кроме того, продукт α-декарбоксилирования глутаминовой кислоты – γ-аминомасляная кислота (ГАМК). Фермент, катализирующий эту реакцию (глутаматдекарбокси-лаза), является высокоспецифичным.

Интерес к ГАМК объясняется ее тормозящим действием на деятельность ЦНС. Больше всего ГАМК и глутаматдекарбоксилазы обнаружено в сером веществе коры большого мозга, в то время как белое веществомозга и периферическая нервная система их почти не содержат. Введение ГАМК в организм вызывает разлитой тормозной процесс в коре (центральное торможение) и у животных приводит к утрате условных рефлексов. ГАМК используется в клинике как лекарственное средство при некоторых заболеваниях ЦНС, связанных с резким возбуждением коры большого мозга. Так, при эпилепсии хороший эффект (резкое сокращение частоты эпилептических припадков) дает введение глутаминовой кислоты. Как оказалось, лечебный эффект обусловлен не самой глутаминовой кислотой, а продуктом ее декарбоксилирования – ГАМК.
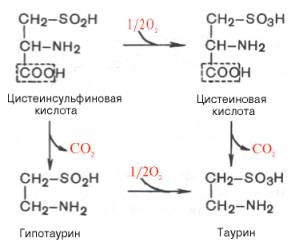
В животных тканях с высокой скоростью декарбоксилируются также два производных цистеина – цистеиновая и цистеинсульфиновая кислоты. В процессе этих специфических ферментативных реакций образуется таурин, который используется в организме для синтеза парных желчных кислот (см. главу 11).
Следует указать еще на два недавно открытых в тканях животных фермента, катализирующихдекарбоксилирование орнитина и S-аденозил-метионина: орнитиндекарбоксилазу и аденозилметиониндекарбоксилазу.
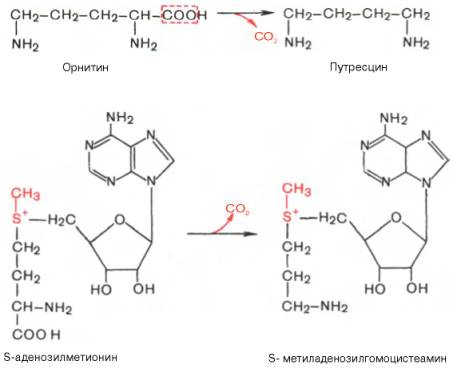
Значение этих реакций для тканей животных огромно, поскольку продукты реакций используются для синтезаполиаминов – спермидина и спермина.
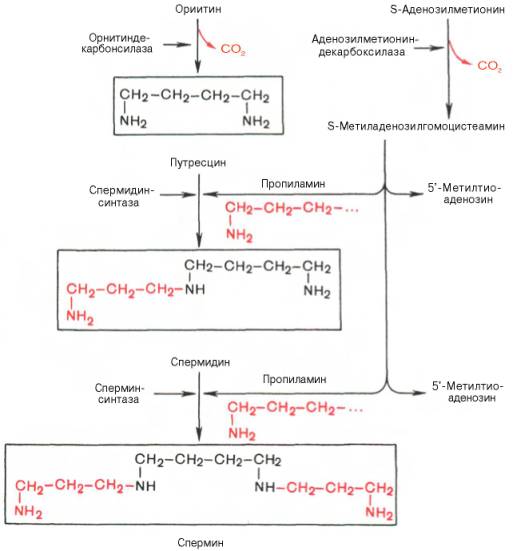
Полиамины, к которым относят также диамин путресцин, играют важную роль в процессах клеточного роста и дифференцировки, в регуляции синтеза ДНК, РНК и белка, стимулируя транскрипцию и трансляцию (см. далее), хотя конкретный механизм участия их в указанных процессах не всегда ясен.
Таким образом, биогенные амины являются сильными фармакологически активными веществами, оказывающими разностороннее влияние на физиологические функции организма. Некоторые биогенныеамины нашли широкое применение в качестве лекарственных препаратов.
Распад биогенных аминов. Накопление биогенных аминов может отрицательно сказываться на физиологическом статусе и вызывать ряд существенных нарушений функций в организме. Однако органы иткани, как и целостный организм, располагают специальными механизмами обезвреживания биогенныхаминов, которые в общем виде сводятся к окислительному дезаминированию этих аминов с образованием соответствующих альдегидов и освобождением аммиака:
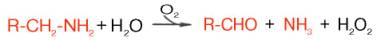
Ферменты, катализирующие эти реакции, получили название моноамин-и диаминоксидаз. Более подробно изучен механизм окислительного дез-аминирования моноаминов. Этот ферментативный процесс является необратимым и протекает в две стадии:
R-CH2-NH2+ Е-ФАД + H20-> R-CHO + NH3+ Е-ФАДН2 (1)
Е-ФАДН2 +02-> Е-ФАД + Н202 (2)
Первая (1), анаэробная, стадия характеризуется образованием альдегида, аммиака и восстановленногофермента. Последний в аэробной фазе окисляется молекулярным кислородом. Образовавшаяся перекись водорода далее распадается на воду и кислород. Моноаминоксидаза (МАО), ФАД-содержащий фермент, преимущественно локализуется в митохондриях, играет исключительно важную роль в организме, регулируя скорость биосинтеза и распада биогенных аминов. Некоторые ингибиторы моно-аминоксидазы (ипраниазид,гармин, паргилин) используются при лечении гипертонической болезни, депрессивных состояний, шизофрении и др.
 2014-02-09
2014-02-09 5558
5558