| Дисперсная фаза | Дисперсионная среда | Название системы | Примеры |
| Газ | Газ | (Дисперсная система не образуется.) | – |
| Жидкость | Пена | Пена газированной воды, пузырьки газа в жидкости, мыльная пена | |
| Твердое тело | Твердая пена | Пенопласт, микропористая резина, пемза, хлеб, сыр | |
| Жидкость | Газ | Аэрозоль | Туман, облака, струя из аэрозольного баллона |
| Жидкость | Эмульсия | Молоко, сливочное масло, майонез, крем, мазь | |
| Твердое тело | Твердая эмульсия | Жемчуг, опал | |
| Твердое тело | Газ | Аэрозоль, порошок | Пыль, дым, мука, цемент |
| Жидкость | Суспензия, золь (коллоидный раствор) | Глина, паста, ил, жидкие смазочные масла с добавкой графита или MoS | |
| Твердое тело | Твердый золь | Сплавы, цветные стекла, минералы |
Большая поверхность раздела фаз вызывает сильное взаимодействие частиц дисперсной фазы с дисперсионной средой, которое приводит к тому, что частицы дисперсной фазы окружаются молекулами и ионами дисперсионной среды (растворителя) или же приобретают довольно значительный электрический заряд.
Любые два вещества на поверхности соприкосновения обязательно взаимодействуют. Это могут быть химическая реакция, взаимодействие, обусловленное проникновением одного вещества в другое и останавливающееся при достижении некоторого равновесного состояния, образование оболочки одного вещества вокруг частицы другого и многое другое. Дисперсная фаза и дисперсионная среда также взаимодействуют, но степень взаимодействия может быть различной.
По силе взаимодействия дисперсной фазы с дисперсионной средой коллоидные системы разделяют на лиофильные (от греч. 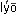 – растворяю,
– растворяю,  – люблю) и лиофобные (от греч.
– люблю) и лиофобные (от греч. 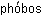 – страх). Эти названия указывают на то, что в лиофильных коллоидных системах взаимодействие частиц с веществом дисперсионной среды сильнее, чем в лиофобных.
– страх). Эти названия указывают на то, что в лиофильных коллоидных системах взаимодействие частиц с веществом дисперсионной среды сильнее, чем в лиофобных.
Лиофильные дисперсные системы характеризуются сильным притяжением молекул дисперсионной среды к частицам дисперсной фазы. Вокруг частиц самопроизвольно образуются плотные и сравнительно устойчивые сольватные оболочки. При взаимодействии с молекулами воды говорят о гидрофильности дисперсной фазы и образовании гидратных оболочек. Если частицы распределены в маслоподобных органических веществах и окружены такими оболочками, говорят об олеофильности частиц. Лиофильные вещества (тела) растворяются в данной жидкости, набухают в ней или хорошо смачиваются.
В лиофильных коллоидах поверхность частиц сильно сольватирована и поверхностная энергия (поверхностное натяжение) на границе раздела фаз мала. Лиофильные коллоиды образуются в результате самопроизвольного диспергирования крупных частиц твердого вещества или капель жидкости на мельчайшие коллоидные частицы (или мицеллы). Лиофильные коллоиды термодинамически устойчивы и поэтому почти не разрушаются при постоянстве условий их образования.
Лиофильные системы самопроизвольно образуются в жидкостях без участия электролитов или поверхностно-активных веществ. Так, гидрофильные системы образуют желатин и крахмал, которые сначала набухают в воде и затем переходят в раствор (студень, кисель, крахмальный клей); альбумины, в том числе яичный белок, также растворяются в воде; натуральный каучук легко растворяется в бензине (резиновый клей). К лиофильным коллоидным системам относятся растворы обычного мыла в воде.
Важнейшая характеристика дисперсных систем – знак и величина заряда частиц. У частиц лиофильных коллоидов заряд или очень мал, или вообще отсутствует. Заряд на частице лиофильного коллоида изменяется очень легко при прибавлении небольших количеств электролитов. Изменение концентрации ионов водорода в растворе (рН) приводит к перезарядке частиц коллоидного раствора. В электрическом поле лиофильные коллоиды или не перемещаются, или перемещаются в любом направлении.
Слабое взаимодействие молекул дисперсионной среды с частицами дисперсной фазы приводит к образованию лиофобных систем. Если дисперсионной средой является вода, говорят о гидрофобности системы, если органические маслоподобные вещества – об ее олеофобности. Частицы лиофобных веществ (тела) не растворяются, плохо смачиваются и не набухают в веществе дисперсионной среды. Лиофобные системы с концентрацией дисперсной фазы выше 1% получить не удается, а лиофильные коллоидные системы могут быть очень концентрированными.
О лиофильности или лиофобности системы можно судить по количеству теплоты, выделяющейся при растворении, набухании и смачивании. У лиофильных систем теплота взаимодействия намного больше, чем у лиофобных.
На гладкой поверхности лиофильного вещества капля жидкости растекается, образуя тонкий слой (пленку), а на лиофобной поверхности капля не растекается, образуя линзу или сплющенный шар. Количественной мерой лиофобности может служить величина угла между поверхностями капли и смачиваемого тела (краевой угол, или угол смачивания).
Лиофобные коллоидные системы по вязкости близки к дисперсионной среде, лиофильные системы имеют более высокую вязкость.
Лиофильные коллоидные растворы рассеивают свет слабее лиофобных.
Типичные лиофобные вещества – оксиды или сульфиды элементов металлического характера.
Принципиальное различие лиофобных и лиофильных коллоидных систем состоит в их термодинамических свойствах. Лиофобные системы – гетерогенные, и в этом отношении их нельзя относить к истинным растворам. Лиофильные системы – однофазные, гомогенные, обладающие многими свойствами истинных растворов. Вследствие высокой поверхностной энергии лиофобные системы термодинамически и кинетически неустойчивы. Лиофильные системы термодинамически устойчивы.
При распаде лиофобных коллоидов происходит укрупнение коллоидных частиц, которое сопровождается уменьшением энергии системы. Способность противостоять укрупнению частиц (агрегативная устойчивость) у лиофобной системы имеет временный характер и часто обусловлена наличием веществ (стабилизаторов), адсорбирующихся на поверхности частиц и препятствующих их слипанию (или слиянию).
 2015-06-05
2015-06-05 2816
2816
