Притяжение между частицами обусловлено силами Ван-дер-Ваальса. Энергия притяжения между молекулами в зависимости от расстояния между ними включает три составляющие: ориентационное (диполь-дипольное притяжение), индукционное (взаимодействие диполя с неполярной молекулой) и дисперсионное взаимодействие двух неполярных молекул.
Ориентационное и индукционное взаимодействия являются короткодействующими и составляют 5–50 % от общей энергии молекулярного притяжения.
Дисперсионные силы возникают из-за того, что даже нейтральные атомы представляют собой системы колеблющихся зарядов вследствие наличия положительного ядра и отрицательно заряженных электронов. Это приводит к тому, что в неполярных атомах и молекулах возникают мгновенные диполи, которые индуцируют возникновение диполей в соседних молекулах. Результатом взаимодействия наведенных диполей между собой является притяжение молекул.
Из сил Ван-дер-Ваальса наиболее универсальными являются дисперсионные взаимодействия. Это связано с тем, что дисперсионное взаимодействие является: всеобщим (действует всегда, составляет примерно 50 % в случае полярных молекул и 100 % в случае неполярных), аддитивным и слабоэкранируемым (взаимодействие двух молекул друг с другом не зависит от присутствия других молекул). Поэтому взаимодействие двух частиц дисперсной фазы, представляющих собой конгломерат множества молекул или атомов, находящихся на расстоянии h практически целиком определяется дисперсионными силами.
В этом случае энергия дисперсионного взаимодействия (притяжения) изменяется с расстоянием по уравнению:
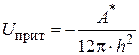 , (5.21)
, (5.21)
где А* – постоянная Ван-дер-Ваальсовых сил притяжения (постоянная Гамакера), учитывающая природу взаимодействующих частиц и диэлектрическую проницаемость среды.
Постоянная Гамакера определяется числом молекул в единице объема взаимодействующих фаз, поляризуемостью молекул и их энергией ионизации, вычисляется из квантово-статистических расчетов и выражается в единицах энергии и имеет значение порядка 10–19 Дж.
Отрицательный знак в уравнении свидетельствует о стремлении частиц к сближению под действием сил межмолекулярного притяжения. Принято считать, что силы притяжения отрицательны.
Из уравнения видно, что энергия притяжения частиц обратно пропорциональна квадрату расстояния между ними. Это указывает на то, что энергия притяжения между коллоидными частицами значительно медленнее уменьшается с расстоянием, чем энергия притяжения между атомами или молекулами, которая обратно пропорциональна расстоянию в шестой степени. Таким образом, коллоидные частицы взаимодействуют на более дальних расстояниях, чем молекулы (атомы).
Общая энергия взаимодействия между двумя частицами U (h) получается сложением энергий электростатического отталкивания и энергии притяжения:
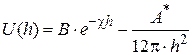 . (5.22)
. (5.22)
 2015-06-05
2015-06-05 2338
2338
