Диффузия – самопроизвольное выравнивание концентраций под влиянием теплового движения, приводящая к выравниванию химических потенциалов во всем объеме системы.
Процесс диффузии всегда необратим. Диффузия выражается в переносе вещества из мест в большей концентрацией к месту с меньшей концентрацией и идет до полного их выравнивания и заканчивается равномерным распределением молекул или частиц по всему объему системы.
Движущей силой диффузии является градиент концентраций, т.е. изменение концентрации на единицу расстояния. Скорость диффузии тем больше, чем меньше размеры диффундирующих частиц.
Рассмотрим количественные закономерности диффузии. Количественно диффузия характеризуется потоком JD, равным массе вещества, проходящей за единицу времени через условную единичную поверхность, расположенную перпендикулярно направлению потока.
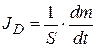 . (8.3)
. (8.3)
Первый закон Фика (1855): диффузионный поток прямо пропорционален градиенту концентрации вещества:
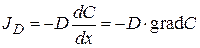 , (8.4)
, (8.4)
где 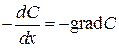 – градиент концентраций, знак минус выражает уменьшение концентрации с расстоянием х; D – коэффициент диффузии – удельная скорость диффузии, характеризующая способность вещества к диффузии (скорость диффузии при равными единице времени диффузии, площади поперечного сечения и градиенте концентрации).
– градиент концентраций, знак минус выражает уменьшение концентрации с расстоянием х; D – коэффициент диффузии – удельная скорость диффузии, характеризующая способность вещества к диффузии (скорость диффузии при равными единице времени диффузии, площади поперечного сечения и градиенте концентрации).
Изучение диффузии сводится к определению коэффициента диффузии, который зависит от концентрации дисперсной фазы.
Эйнштейн показал, что коэффициент диффузии зависит от свойств дисперсионной среды и размеров диффундирующих частиц:
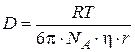 , (8.5)
, (8.5)
где η– вязкость дисперсионной среды; r – радиус коагулирующих частиц; 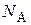 – число Авогадро.
– число Авогадро.
Из уравнения Эйнштейна следует, что чем больше радиус частицы дисперсной фазы, тем меньше скорость диффузии. Диффузия в дисперсных системах всегда значительно меньше, чем в истинных растворах (для коллоидных частиц с D = 5·10–9 cм2/с время прохождения 1 см составит около трех лет, тогда как для молекул – несколько часов).
Следовательно, для коллоидных систем характерна весьма медленная скорость диффузии, но все же измеримая, позволяющая определить размеры диффундирующих частиц по уравнению:
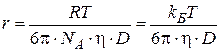 . (8.6)
. (8.6)
Пример 8.1. Коэффициент диффузии арабинозы в воде при 291 К составляет 5,4·10–5 м2/сутки. Вязкость воды 1,06·10–3 Н·с/м2. Вычислите радиус молекулы (в м) и молярную массу органического вещества. Плотность арабинозы 1,618·103 кг/м3. Полученное значение молярной массы сравните с теоретическим значением (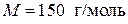 ).
).
Решение:
1. Выразим коэффициент диффузии в м2/с:
1 сутки = 24 ч = 86400 с
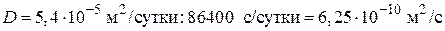 .
.
2. Вычислим радиус молекулы арабинозы:
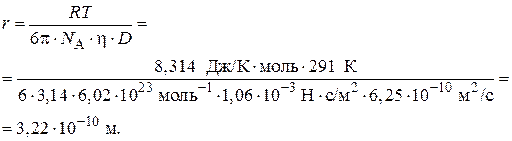
3. Рассчитаем молярную массу арабинозы:
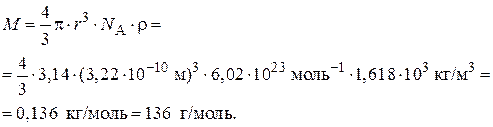
Вычисленное значение молярной массы арабинозы близко к теоретическому значению.
 2015-06-05
2015-06-05 4656
4656
