Массообменные процессы – это процессы, заключающиеся в переходе вещества из одной фазы в другую. К ним относятся:
- абсорбция;
- адсорбция;
- перегонка и ректификация;
- сушка;
- экстракция;
- кристаллизация;
- растворение.
Массопередача – процесс переноса вещества из одной фазы в другую в направлении достижения равновесия.
Основу массопередачи составляют некоторые законы.
Закон Генри определяетзависимость между растворимостью газа и его парциальным давлением
РH2S= K*СH2S(р)
где СH2S(р) – концентрация растворенного газа в растворе, мол.доли;
К – константа Генри, ат, МПа, кгс/см2. (по справочнику) [Плановский, Рамм, Коган. Процессы и аппараты химической технологии, М. Химия, 1968].
Таблица - Константы Генри
| газ | Коэффициент Генри, атм | ||||||
| 0оС | 10оС | 20оС | 30оС | 40оС | 50оС | 60оС | |
| NH3 | 0.274 | 0,485 | 0,823 | 1,36 | 2,15 | 3,36 | 5,06 |
| SO2 | 1,48 | 2,24 | 3,67 | 5,72 | 8,03 | 11,2 | 16,3 |
| CO2 | |||||||
| O2 | |||||||
| H2S |
Зная парциальное давление компонента в газовой смеси РH2S, можно рассчитать равновесное содержание поглощенного газа в газовой смеси
СH2S(г) = 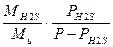
Р – давление газа.
Равновесие – это термодинамическое состояние системы, при котором скорости прямого и обратного процессов равны.
Закон Рауля-Дальтона. Позволяет произвести расчет равновесной концентрации растворенного газа в газовой смеси.
СH2S(г) = 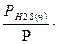 СH2S(р)
СH2S(р)
где РH2S(ч) – давление паров чистого компонента
Р – общее давление газа
СH2S(р) – содержание компонента в растворе, доли
Статика массообменных процессов.
Статика определяет равновесие и материальный баланс массообменных процессов. Статика абсорбции – равновесие между фазами определяется правилом фаз Гиббса (число степеней свободы, т.е. параметров, процесса равно числу компонентов минус число фах плюс 2):
С= К – Ф + 2
где К – количество компонентов;
Ф – количество фаз.
Для абсорбции: число фаз – 2 (газ-жидкость), число компонентов – извлекаемый компонент в газе, очищенный газ, жидкий поглотитель (трехкомпонентная система) – 3.
Тогда С= 3-2+2=3. Таким образом для абсорбции это значит, что можно изменять 3 параметра (Р, Т, состав одной из фаз), не нарушая при этом равновесия в системе.
Уравнение равновесия y = k*x
Материальный баланс массообменных процессов G*y1 + L*x2 =G*y2 + L*x2 или
G*(y1 – y2) = L*(x1- x2)
 2015-06-05
2015-06-05 825
825








