1. а) Алюминиевый электрод погружен в 5∙10-4М раствор сульфата алюминия. Вычислить значение потенциала алюминиевого электрода.

РЕШЕНИЕ: Электродный потенциал алюминия рассчитываем по уравнению Нернста: 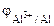 = = 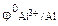 + + 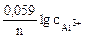 |
По таблице 11.1 определяем стандартный электродный потенциал алюминия
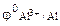 = -1,67В.
= -1,67В.
Записываем уравнение электродного процесса, протекающего на поверхности алюминиевого электрода в растворе соли:
Al - 3ē = Al3+
n – число электронов, участвующих в электродном процессе.
Для данной реакции n равно заряду иона алюминия Al3+(n=3).
Рассчитываем концентрацию ионов алюминия в растворе Al2(SO4)3:
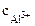 =
= 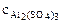 ∙α∙
∙α∙ 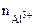
Разбавленный раствор Al2(SO4)3 – сильный электролит.
Следовательно, α = 1. По уравнению диссоциации Al2(SO4)3:
Al2(SO4)3 = 2Al3+ + 3SO 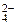
число ионов Al3+, образующихся при диссоциации одной молекулы Al2(SO4)3 равно 2.
Следовательно, 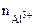 =2
=2
Тогда 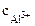 = 5∙10-4∙1∙2 =
= 5∙10-4∙1∙2 = 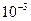 моль/л.
моль/л.
Рассчитываем электродный потенциал алюминиевого электрода:
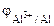 = -1,67 +
= -1,67 + 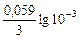 = -1,73В.
= -1,73В.
Ответ: 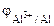 = -1,73В.
= -1,73В.
 2015-06-05
2015-06-05 5616
5616
