I. При стерилизации дан. в-ва произошло помутнение → при изготовлении не б. добавлено или было недостаточное кол-во стабилизатора (выпадает основание → р-р мутнеет)
Р-р новокаина 0,25% - 3мл
0,5% - 4мл
1% - 9мл
2% - 12мл 0,1н HCl на 1л р-ра. Исп-ся для разведения пенициллина.
Р-р новокаина 2% - 4мл
5% - 6мл
10% - 8мл 0,1н HCl на 1л р-ра + Na тиосульфат 0,2г
Р-р новокаина 5% и 10% б/стабилизаторов и б/стерилизации. Используют для спинно-мозговой анестезии.
II. Новокаин (Novocainum) – β-диэтиламиноэтилового эфира ПАБК – местноанестез. ср-во, примен-ся при инфильтрационной, проводниковой анестезии, потенцирование д-я при общей анестезии, купирование болей. Выпуск в амп, фл. 0,25%, 0,5%, 1%, 2%, 5%и 10%р-ры, суппозитории по 1г.
Описание - бесцветные крист или бел. крист порошок б/зап, горького вкуса, на языке вызывает чувство онемения. Оч.л.р. в воде, л.р. в спирте, м.р. в хлф, пр.н.р. в эфире.
Подлинность:
1)Реакции на первичную ароматическую аминогруппу
-Образование азокрасителя. Получение диазосоединения сочетают с фенолами (β-нафтолом, фенолом, резорцином) в щел. ср. или ароматич. аминами в кисл. среде. При этом образуются азокрасители.
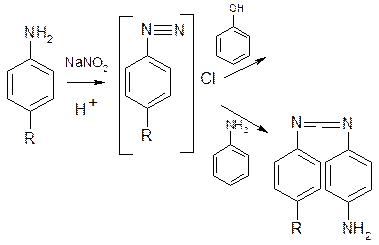
- Реакция образования основания Шифа:
а) с п -диметиламина бензоальдегидом в кислой среде + бензол + спирт → желтое окрашивание:
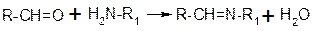
* б) Лигниновая проба - на лигнинсодержащий материал (бумагу, древесину) наносят разв. HCl и в-во с первичной аром. аминогр., появляется желто-оранж. пятно.
Растворы новокаина для инъекций 0,25%, 0,5%, 1%, 2% стабилизируются раствором кислоты хлористоводородной 0,1 М до рН 3,8-4,5 и хранятся 30 дней в защищенном от света месте.
Растворы новокаина для инъекций 2%, 5%, 10% стабилизируются 0,1 М раствором соляной кислоты (4, 6, 8 мл соответственно) и Na2S2O3 0,5 г на 1 л раствора. Хранятся 90 дней в защищенном от света месте.
Стабилизатор для раствора новокаина – раствор НСl 0,1 М готовится из 4,4 мл 8,3% HCl и воды для инъекций до 100,0 мл.
Реак. окисления: в качестве окислителей применяются растворы KМnO4, хлорамина, H2O2.
*б) Новокаин + KMnO4 + H2SO4 р.→ обесцвечивание;
в) Новокаин + H2O2 + H2SO4 к. → сиреневое окрашивание;
- Реакция галоидирования: в частности бромирование, основана на электрофильном замещении атомов водорода бензольного кольца в о - и п -положениях на галоген. Образуется амфорные осадки белого или желтоватого цвета, определяют их температуру плавления.
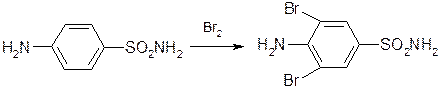
2) Реакции на сложноэфирную группу
- Гидроксамовая реакция:
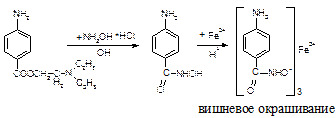
3)Реакции на третичный атом азота:
- С общеалкалоидными осадительными реактивами: атом N имеет неподеленную электронную пару и придает соединениям свойства оснований. И поэтому эти соединения могут образовывать в солянокислой среде труднорастворимые в воде соединения с общеалкалоидными реактивами (к-та пикриовая, к-та фосфорно-вольфрамовая)
Новокаин + NaOH→ при нагревании →аммиак по посинению красной лакмусовой бум.
*4) Реакции на НСl
R · HCl + NaOH → R (азотистое основание)↓ + NaCl + H2O
Новокаин при добавлении раствора NaOH образует бесцветный маслянистый осадок основания. Эта реакция может служить частной реакцией на новокаин.
2) R . НСl + AgNO3 → AgСl ↓ + НNO3 + R
5) Поглощает свет в УФ обл спектра
Новокаин проверяют на - кислотность (м/кр) - м. б. роз. окр.;
- орг. примеси (д.б. бесцветным после доб. H2SO4 к.).
1) Нитритометрия: Титрование проводят в присутствии KBr (катализатора) при пониженной температуре и медленном прибавлении титранта. Индикация конечной точки титрования проводится несколькими способами:
- * с помощью внутренних индикаторов (тропеолин 00 + м/с)
- с использованием внешних индикаторов (йодкрахмальная бумага)
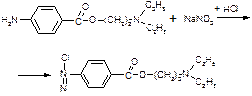 Э = М.м. инд - тропеолин 00 + м/с
Э = М.м. инд - тропеолин 00 + м/с
2) Броматометрия, йодометрия, йодхлорметрия (ароматическая первичная аминогруппа). Методы основаны на способности препаратов галоидироваться в о-положении бензольного кольца.
Прямое титрование: KВrO3 + 5KBr + 6HCl → 3Br2 + 6KCl + 3H2O

3)аргентометрия - м/д Фаянса, инд - дифенилкарбазид, титруют до фиолетов окрашивания Э=2М/1М•2=М.м
Хранение по сп Б, в ХУТ из темного стекла, предохраняя от действия света. При неправильном хранении происходит постепенный г-з препарата.
III. Проблемы чистоты и апирогенности. Стабилизация инъек. р-ров: физ., хим., м/биол.
По способу стабилизации хим.:
- Соли образуемые сил. основаниями и слаб. к-тами (кофеина-бензоат натрия стабилизируется 0,1н р-ром NaOH – 4 мл на 1 л р-ра; р-р к-ты никотиновой 1% - 7г NaHCO3 на 1л р-ра) прибавлением щелочи подавляется реакция г-за, к кот. склонны эти соли в вод. р-рах.
- Соли образ-ные солями сил. к-т и слаб. осн., в вод. р-рах дают слабокислую реак., кот. обусловлена г-зом солей алкол. (атропина сульфат, дикаин стаб-ся 0,1 HCl – 10 мл на 1 л р-ра).
- Р-ры требующие комплексной защиты. Р-р глюкозы добавлением NaCl + HCl. Необходимо соблюдать рН среды – глюк. при рН 1,0-3,0
- Р-ры в-в требующих комбин. защиту (р-р сульфацил-натрий 30% д/ин + 1н. р-рNaOH до рН 7,5-8,5 и Na метабисульфит 3г на 1л, текучий пар в теч 30 мин; р-р к-ты аскорбиновой 5% д/ин + NaHCO3 до рН 6,0-7,0 и антиоксид Na сульфит б/в (0,2%) или Na метабисульфит (1%), текучий пар в теч 15мин при 100ºС)
Физ. стабильность: раздельное ампулирование в-ва и р-ля, подбор ампул из хим стойкого материала, замена стекла на полимер.
Требования, к инъек. р-рам - стерильность, апирогенность и отсут-е мех. включений.
Получение р-ров проводят в помещениях второго кл. чистоты с соблюдением всех правил асептики при периодическом вкл бактерицидных ламп. Р-рение осущ-ся в герметически закрываемых реакторах с паровой рубашкой и мешалкой. Сх. технологии: р-рение, изотонирование, стабилизация, введение консервантов, стандартизация, фильтрование.
Стерилизация: Термические - паровой и воздушный; Хим. - газовый и различными р-рами; Фильтрованием; Радиационный.
Паровой - насыщенным вод. паром при 120oС. Время стерилизации - от физ-хим. св-в препарата, объема р-ра (вод. р-ры). До 100 мл – 8 мин, От 100 до 500 мл - 12 мин = 120oС, От 500 до 1000 – 15 мин.. Воздушный – сух. горячим воздухом при 180o или 200oС. Реком-ся д/стерилизации порошков (NаСl, ZnО, тальк, бел. глина). До 25 мл – 180С – 30 мин; от 25 до 100 мл – 180С – 40 мин; от 100 до 200 мин – 180С – 60 мин; Р-ры - нельзя. Газовый - окисью этилена или смесью ОБ (окись этилена + бромистый метил 1:2,5). Эти вещества являются токсичными. После стерилизации необходимо провентилировать помещение. Применяется д/термолабильных в-в в сластиковой упаковке. Фильтрованием - с помощью мембранных и глубинных фильтров для термолабильных веществ.
Мед. стекло – твердый р-р, получ в рез-те охлаждения расплавленной смеси силикатов, оксидов металлов и солей. Наиб терм и хим уст-ть им кварцевое стекло, в него вх. натрия и калия оксиды.
Требования: прозрачность – д/визуального и оптического контроля, бесцветность, легкоплавкость, термическая уст-ть, хим-я уст-ть, мех-я проч-ть в сочетании с необходимой хрупкостью.
IV. Марена красильная – Rubia tinctorum (Rubiaceae) – Сырьем является корни и корневища, котор сод антраценпроизводные (в основном руберитриновую к-ту, производное ализарина) пиктиновые в/ва и орг к-ты. Чаи исп как спазмолитические и мочегонные ср-ва, способствуют разрыхлению мочевых камней, используются при мочекаменной и почечнокаменной болезнях.
В виде гликозида антрагликозиды.

Кристаллическое вещества желтого, оранжевого или красного цвета. Агликоны хорошо растворимы в эфире, хлороформе, бензоле, нерастворимы в воде. Гликозиды хорошо растворимы в воде, водно-спиртовых растворах, нерастворимы в органических растворителях. И агликоны и гликозиды хорошо растворимы в водных растворах щелочей, за счет образования фенолятов.
Качественный анализ - реакция со щелочью. Ее можно проводить или непосредственно на сырье или с водным извлечением. появляется красное окрашивание. Затем раствор подкисляют соляной кислотой и извлекают агликоны этиловым эфиром. При встряхивании эфирного раствора с аммиаком антраценпроизводные вновь переходят в водноаммиачный слой окрашивая его в красный цвет.
Способность антраценпроизводных к флуоресценции в УФ свете использована для качественного обнаружения их в сырье методом люминесцентной микроскопии (оранжево-красное свечение).
Количественное определение. В настоящее время количественное содержание антраценпроизводных в ЛРС определяют ФЭК или СФ методами.:
- Определение суммы производных антрацена. Сущность метода:
1. Гидролиз антраценпроизводных при нагревании навески сырья с кислотой.
2. Экстрагирование агликонов органическим растворителем при нагревании.
3. Экстрагирование антраценпроизводных из органического растворителя щелочно-аммиачным раствором (в виде фенолятов).
4. Окисление восстановленных форм (нагревание щелочного-аммиачного извлечения или добавление окислителей, например перикиси водорода)
5. Измерение оптической плотности окрашенного раствора фенолятов антраценпроизводных.
6. Расчет содержания суммы антраценпроизводных в ЛРС.
По калибровочному графику находят содержание производных антрацена в граммах в 1 мл колориметрируемого раствора.
Содержание суммы производных антрацена в пересчете на абсолютно сухое сырье в процентах (X) вычисляют по формуле:
С х 500 х 100 х 100
Х = ---------------------,
m(100 - W)
где С - содержание свободных производных антрацена в 1 мл колориметрируемого раствора, найденное по калибровочному графику, в граммах; m - масса сырья в граммах; W - потеря в массе при высушивании сырья в процентах.
2. Определение свободных производных антрацена. Около 0,1 г (точная навеска) измельченного сырья помещают в колбу вместимостью 300 мл, прибавляют 50 мл эфира и нагревают на водяной бане с обратным холодильником в течение 10 мин с момента закипания эфира. Экстракцию повторяют трижды, затем колбу охлаждают и эфирные извлечения фильтруют через вату в делительную воронку вместимостью 20 мл. Воронку с эфирным извлечением охлаждают и производные антрацена извлекают 4 раза по 20 мл щелочно - аммиачным раствором, каждый раз встряхивая в течение 5 мин. Щелочной раствор количественно переносят в мерную колбу вместимостью 100 мл, прибавляют 1 каплю пергидроля, объем раствора доводят щелочно - аммиачным раствором до метки и перемешивают. Полученный раствор колориметрируют, как указано в п. "1".
Содержание свободных производных антрацена в пересчете на абсолютно сухое сырье в процентах (Х1) вычисляют по формуле:
С х 100 х 100 х 100
X1 = ---------------------,
m(100 - W)
где С - содержание свободных производных антрацена в 1 мл колориметрируемого раствора, найденное по калибровочному графику, в граммах; m - масса сырья в граммах; W - потеря в массе при высушивании сырья в процентах.
Содержание связанных производных антрацена в пересчете на абсолютно сухое сырье (в процентах Х2) вычисляют по формуле:
Х2 = Х - Х1.
ФЭК метод является фармакопейным и включен с небольшими вариациями в большинство ФС на ЛРС, содержащее антраценпроизводные.
IV. Ген «house keeping» (ген «домашнего хозяйства») – набор основных структурных генов, обеспечивающих жизнедеятельность клеток
Ген «ivi» - экспрессия. Происходит всегда мишени, инактивация продуктов экспрессии которых приводит к прекращению размножению и гибель патогенна.
Метод IVET основан на захвате проматора и использовании целостного живого организма или культуры животных клеток как селективной среды, выявляющий экспрессию «ivi» генов.
Определите понятие существенности гена при поиске новых лекарственных средств.
 2015-06-28
2015-06-28 3853
3853
