Какие химические связи имеются в ионах [NH4]+, [BF4]-?
Решение.
Напишем валентные электроны взаимодействующих атомов:
N 2s2 2p3,
B 2s2 2p1,
F 2s2 2p5,
H 1s1.
При образовании молекулы аммиака (см. пример 3.1) атом азота не исчерпал все валентные возможности, так как у него осталась свободной ещё одна пара электронов. При взаимодействии с ионом водорода H+, имеющего незанятую 1s-орбиталь, образуется ещё одна ковалентная связь:
NH3 + H+ 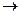 [NH4]+.
[NH4]+.
Такая ковалентная связь, когда атом-комплексообразователь (азот) предоставляет для образования связи пару электронов, а атом-лиганд - (водород) свободную орбиталь, называется дативной.
Для образования молекулы BF3 атом бора переходит в возбужденное состояние с тремя неспаренными электронами:
B 2s2 2p1 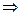 B* 2s1 2p2.
B* 2s1 2p2.
Три образующихся гибридных облака (sp2-гибридизация) перекрываются с тремя p-облаками трех атомов фтора и получается молекула BF3. Но у атома бора остается свободная орбиталь, а у иона фтора имеются свободные электронные пары (F0 + 1 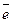 = F-) Поэтому в ионе [BF4]- четвертая ковалентная связь образуется по донорно-акцепторному механизму:
= F-) Поэтому в ионе [BF4]- четвертая ковалентная связь образуется по донорно-акцепторному механизму:
BF3 + F- 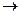 [BF4]-.
[BF4]-.
Атом бора - комплексообразователь дает для связи пустую орбиталь (акцептор), а ион фтора - лиганд, дает пару электронов (донор).
Итак, в ионах [NH4]+ и [BF4]- четыре ковалентные связи образованы разными способами:
а) одноэлектронный 1:1,
б) дативный 2:0,
в) донорно-акцепторный 0:2.
Первая цифра указывает число электронов комплексообразователя, вторая - лиганда.
Все четыре связи одинаковы по энергии, длине и другим параметрам, т. е. это не новый тип связи, а разные механизмы образования одной ковалентной связи.
Задания
61. Какую химическую связь называют ковалентной? Чем можно объяснить направленность ковалентной связи? Как метод валентных связей (ВС) объясняет строение молекулы воды?
62. Какая ковалентная связь называется s-связью и какая полярной? Что служит количественной мерой полярности ковалентной связи? Составьте электронные схемы строения молекул N2, H2O, HJ. Какие из них являются диполями?
63. Какой способ образования ковалентной связи называется донорно-акцепторным? Какие химические связи имеются в ионах [Cu(NH3)4]2+ и SbF4–? Укажите донор и акцептор.
64. Как метод валентных связей (ВС) объясняет линейное строение молекулы BeCl2 и тетраэдрическое – СН4?
65. Какая ковалентная связь называется s-связью и какая p-связью? Разберите на примере строения молекулы азота.
66. Сколько неспаренных электронов имеет атом хлора в нормальном и возбужденном состояниях? Распределите эти электроны по квантовым ячейкам. Чему равна валентность хлора, обусловленная неспаренными электронами?
67. Распределите электроны атома серы по квантовым ячейкам. Сколько неспаренных электронов имеют ее атомы в нормальном и возбужденном состояниях? Чему равна валентность серы, обусловленная неспаренными электронами?
68. Что называется электрическим моментом диполя? Какая из молекул HCl, HBr, HJ имеет наибольший момент диполя? Почему?
69. Какие кристаллические структуры называются ионными, атомными, молекулярными и металлическими? Кристаллы каких веществ: алмаз, хлорид натрия, диоксид, углерода, цинк – имеют указанные структуры?
70. Составьте электронные схемы строения молекул Сl2, H2S, ССl4. В каких молекулах ковалентная связь является полярной? Как метод валентных связей (ВС) объясняет угловое строение молекулы H2S?
71. Чем отличается структура кристаллов NаСl от структуры кристаллов натрия? Какой вид связи осуществляется в этих кристаллах? Какие кристаллические решетки имеют натрий и NaCl? Чему равно координационное число натрия в этих решетках?
72. Какая химическая связь называется водородной? Между молекулами каких веществ она образуется? Почему Н2O и НF, имея меньшую молекулярную массу, плавятся и кипят при более высоких температурах, чем их аналоги?
73. Какая химическая связь называется ионной? Каков механизм ее образования? Какие свойства ионной связи отличают её от ковалентной? Приведите два примера типичных ионных соединений. Напишите уравнения превращения соответствующих ионов в нейтральные атомы.
74. Что следует понимать под степенью окисления атома? Определите степень окисления атома углерода и его валентность, обусловленную числом неспаренных электронов в соединениях СН4, СН3ОН, НСООН, СО2.
75. Какие силы молекулярного взаимодействия называются ориентационными, индукционными и дисперсионными? Когда возникают и какова природа этих сил?
76. Какая химическая связь называется координационной или донорно-акцепторной? Разберите строение комплексного иона [Zn(NH3)4]2+. Укажите донор и акцептор. Как метод валентных связей (ВС) объясняет тетраэдрическое строение этого иона?
77. Какие электроны атома бора участвуют в образовании ковалентных связей? Как метод валентных связей (ВС) объясняет симметричную треугольную форму молекулы BF3?
78. Как метод молекулярных орбиталей объясняет парамагнитные свойства молекулы кислорода? Нарисуйте энергетическую схему образования молекулы O2 по методу молекулярных орбиталей (МО).
79. Нарисуйте энергетическую схему образования молекулы F2 по методу МО. Сколько электронов находится на связывающих и разрыхляющих орбиталях?
80. Как метод молекулярных орбиталей объясняет большую энергию диссоциации молекулы азота? Нарисуйте энергетическую схему образования молекулы N2 по методу МО. Сколько электронов находится на связывающих и разрыхляющих орбиталях?
Энергетика химических процессов
(термохимические расчеты)
 2015-06-24
2015-06-24 12201
12201
