Учебное заведение: Федеральный перечень учебников по химии (2014-2018). Тип материала: Учебное пособие
Метод МО является более совершенным методом описания строения молекул. Если метод ВС позволяет судить о направленности строения молекул, определяет форму молекулы или иона, то метод МО дает более полную информацию о строении, указывает на прочность связи, возможность существования молекулы, магнитные свойства вещества.
В основе этого метода лежит представление о том, что все электроны данной молекулы или иона (как и в атоме) распределяются по соответствующим молекулярным орбиталям. По аналогии с атомными s-, p-, d-, f- орбиталями, молекулярные орбитали обозначаются греческими буквами s-, p-, d-, j-, ….
Описать молекулу по теории МО – это значит определить ее орбитали, их энергию и выяснить характер распределения электронов по орбиталям в порядке возрастания их энергии. Образование молекулярных орбиталей можно представить как результат сложения и вычитания взаимодействующих атомных орбиталей. Метод МО основан на следующих правилах:
1. При сближении атомов до расстояния химических связей, из атомных орбиталей (АО) образуются молекулярные, число полученных молекулярных орбиталей равно числу исходных атомных.
2. Перекрываются атомные орбитали, близкие по энергии. В результате перекрывания двух атомных орбиталей образуются две молекулярные. Одна из них имеет меньшую энергию по сравнению с исходными атомными и называется связывающей, а вторая молекулярная орбиталь обладает большей энергией, чем исходные атомные орбитали, и называется разрыхляющей.
3. При перекрывании атомных орбиталей возможно образование и s -связи (перекрывание по оси химической связи), и p- связи (перекрывание по обе стороны от оси химической связи).
5. На одной молекулярной орбитали (как, впрочем, и атомной) возможно нахождение не более двух электронов (принцип Паули).
6. Электроны занимают молекулярную орбиталь с наименьшей энергией (принцип наименьшей энергии).
7. Заполнение орбиталей вырожденных (с одинаковой энергией) происходит последовательно по одному электрону на каждую из них.
  |
Схема образования и форма данных молекулярных орбиталей с учётом изложенного выше представлена на рис.3.7:
В силу осевой симметрии обеих молекулярных орбиталей относительно линии, связывающей ядра атомов, это σ-орбитали. В общем случае обозначение МО, кроме типа связи (σ-, π-, δ-) содержит также указание на их характер (связывающие, разрыхляющие, несвязывающие) и вид исходных АО: например,  и
и  или σs и
или σs и 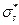 (звёздочка указывает на возбуждённое состояние).
(звёздочка указывает на возбуждённое состояние).
  |
Результаты линейной комбинации исходных АО в методе МО нагляднее демонстрировать в виде энергетической диаграммы. Для рассмотренного выше случая энергетическая диаграмма представлена на рис.3.6.
Заполнение молекулярных орбиталей электронами подчиняется тем же основным принципам, что и атомных орбиталей. В соответствии с этим энергетическая диаграмма молекулы водорода будет выглядеть так, как представлено на рис.3.7.:
 |
В нормальном состоянии молекулы водорода оба её электрона согласно принципу минимума энергии занимают наиболее низкую орбиталь  и согласно принципу Паули имеют противоположные спины. Таким образом, ёмкость МО так же, как и АО составляет два электрона. Суммарный спин при этом равен нулю, т.е. молекула должна быть диамагнитной, что и наблюдается в действительности.
и согласно принципу Паули имеют противоположные спины. Таким образом, ёмкость МО так же, как и АО составляет два электрона. Суммарный спин при этом равен нулю, т.е. молекула должна быть диамагнитной, что и наблюдается в действительности.
Изучение молекулярных спектров двуядерных молекул образованных элементами начала 2-ого периода вплоть до азота N2 дало следующий порядок следования МО:
σ1s < σ1s* < σ2s < σ2s* < πy = πz < σx < πy* = πz* < σx* (11)
 |
Другим характерным примером, который обычно используют для того, чтобы продемонстрировать дополнительные возможности метода МО, недоступные МВС, является описание строения молекулярного кислорода О2. Так, например, при совпадении данных обоих методов о двукратности связи в молекуле кислорода метод ВС не позволяет предсказывать магнитные свойства, согласно ему данная молекула диамагнитна, т.к. все электроны спарены:
В действительности молекулярный кислород парамагнитен. Метод МО позволяет объяснить это, как видно из рис. 14, наличием двух неспаренных электронов на π-разрыхляющих орбиталях (πy* и πz*).
 |
Порядок связи (кратность связи) оценивается полуразностью числа связывающих и разрыхляющих электронов:
е - (связ.) – е - (разр.)
Порядок связи = ———————;
где:
е - (связ.) - число связывающих электронов;
е - (разр.) – число разрыхляющих электронов.
Характер распределения электронов по молекулярным орбиталям позволяет объяснить магнитные свойства молекул. По магнитным свойствам различают парамагнитные (обладают собственным магнитным полем) и диамагнитные вещества (не обладают собственным магнитным полем). Парамагнитными считаются те молекулы или ионы, у которых имеются непарные электроны на молекулярных орбиталях (МО), у диамагнитных – все электроны парные.
Как определить, связи какого типа образуют атомы элементов в определенном веществе? Рассмотрим примеры.
1. Хлорид цезия CsCl. Атом цезия (IА группа) большой, с низким значением электроотрицательности, легко отдает электрон, а атом хлора (VIIА группа) небольшой с большим значением ЭО легко его принимает, следовательно, связь в хлориде цезия ионная (типичный металл с типичным неметаллом).
2. Гидрид азота (аммиак) NH3 Атомы азота (VА группа) и водорода (IА группа) отличаются по размерам – оба небольшие по размеру (неметаллы). По склонности принимать электроны они отличаются, связь в молекуле NH3 ковалентная полярная.
3. Азот N2. Простое вещество. Связываемые атомы одинаковые и при этом небольшие, следовательно, связь в молекуле азота ковалентная неполярная.
4. Кальций Са. Простое вещество. Связываемые атомы одинаковые и довольно большие, следовательно связь в кристалле кальция металлическая.
61. Исходя из теории ковалентной связи, изобразите в виде валентных схем строение молекул: HCl, H2O, NH3.
62. Почему энергия двойной связи С = С (613,2 кДж) не равна удвоенному значению энергии одинарной связи С - С (348,6 кДж)?
63. Как изменяется полярность связи и прочность молекул в ряду HF, HCl, HBr, HI?
64. Какие химические связи имеются в ионах [NH4]+, [BF4]-?
65. Какую валентность, обусловленную не спаренными электронами (спин-валентность), может проявлять фосфор в нормальном и возбужденном состояниях?
66. Что такое гибридизация валентных орбиталей? Какое строение имеют молекулы типа АВn если связь в них образуется за счет sp-, sp 2 -, sp 3 – гибридизации орбиталей атома А?
67. Как метод молекулярных орбиталей (МО) описывает строение двухатомных гомоядерных молекул элементов, второго периода?
68. Пользуясь таблицей относительных электроотрицательностей, вычислить их разность для связей Н–О и О–Rb в гидроксиде RbОН и определить: а) какая из связей в молекуле характеризуется большей степенью ионности; б) каков характер диссоциации этих молекул в водном растворе.
69. Как изменяется прочность связи в ряду СO2–SiO2–GeO2–SnO2? Указать причины этих изменений.
70. Дипольный момент молекулы HCN равен 0,97×10-29 Кл×м. Определите длину диполя молекулы HCN. 
71. Какой вид гибридизации электронных облаков имеет место в атоме кремния при образовании молекулы SiF4? Какова пространственная структура этой молекулы?
72. Опишите с помощью метода молекулярных орбиталей молекулу Н20.
73. Определите тип гибридизации орбиталей центрального атома в частице Н3О+.Назовите и изобразите геометрическую форму этой частицы.
74. Определите тип гибридизации орбиталей центрального атома в частице NO2.Назовите и изобразите геометрическую форму этой частицы.
75. Укажите тип гибридизации орбиталей бора в молекуле BBr3.
76. Какие виды химической связи имеются в молекуле NH4I?
77. Сера образует химические связи с калием, водородом, бромом и углеродом. Какие из связей наиболее и наименее полярны? Укажите, в сторону какого атома происходит смещение электронного облака связи.
78. Описать с позиции метода МО молекулу ВеН2: определить кратность связи и магнитные свойства молекулы.
79. Описать с позиции метода МО молекулу СН4: определить кратность связи и магнитные свойства молекулы.
80. Определите тип гибридизации и геометрическую форму комплексного иона [MoCl4]2-
81. Определите тип гибридизации и геометрическую форму комплексного иона [ZnCl4]2-
82. С помощью метода валентных связей (ВС) опишите пространственное строение молекулы CO2.
83. Определите тип гибридизации и геометрическую форму комплексного иона [Cd(H2O)4]2+
84. С помощью метода валентных связей (ВС) опишите пространственное строение молекулы (NН4)+.
85. Определите тип гибридизации и геометрическую форму комплексного иона [Ni(OH)4]2-
86. С помощью метода валентных связей (ВС) опишите пространственное строение молекулы PF3.
87. Определите тип гибридизации и геометрическую форму комплексного иона [Co(NH3)4]3+.
88. С помощью метода валентных связей (ВС) опишите пространственное строение молекулы SiF4.
89. Определите тип гибридизации и геометрическую форму комплексного иона [Cr(H2O)4]3+
90. Определите тип гибридизации и геометрическую форму комплексного иона [CuCl4]2-
 2015-10-22
2015-10-22 36944
36944
