При донорно-акцепторном механизме образования ковалентной связи связь также образуется с помощью электронных пар. Однако в этом случае однин атом (донор) предоставляет свою электронную пару, а другой атом (акцептор) участвует в образовании связи своей свободной орбиталью. Примером реализации донорно-акцепторной связи является образование иона аммония NH4+ при взаимодействии аммиака NH3 с катионом водорода H+. В молекуле NH3 три электронные пары образуют три связи N – H, четвертая, принадлежащая атому азота электронная пара является неподеленной. Эта электронная пара может дать связь с ионом водорода, который имеет свободную орбиталь. В результате получается ион аммония NH4+, рис. 5.2.
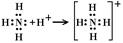
Рис. 5.2. Возникновение донорно-акцепторной связи при образовании иона аммония
Необходимо отметить, что существующие в ионе NH4+ четыре ковалентных связи N – H равноценны. В ионе аммония невозможно выделить связь, образованную по донорно-акцепторному механизму.
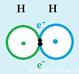
Полярная и неполярная ковалентная связь
Если ковалентная связь образуется одинаковыми атомами, то электронная пара располагается на одинаковом расстоянии между ядрами этих атомов. Такая ковалентная связь называется неполярной. Примером молекул с неполярной ковалентной связью являются Н2, Cl2, О2, N2 и др.
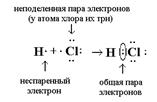
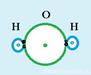
В случае полярной ковалентной связи общая электронная пара смещена к атому с большей электроотрицательностью. Этот тип связи реализуется в молекулах, образованных различными атомами. Ковалентная полярная связь имеет место в молекулах HCl, HBr, CO, NO и др. Например, образование полярной ковалентной связи в молекуле HCl можно представить схемой, рис. 5.3:
Рис. 5.3. Образование ковалентной полярной связи в молекуле НС1
В рассматриваемой молекуле электронная пара смещена к атому хлора, поскольку его электроотрицательность (2,83) больше, чем электроотрицательность атома водорода (2,1).
1. Ковалентную неполярную связь образуют одинаковые атомы неметаллов и атомы водорода;
2. Ковалентную полярную химическую связь образуют разные атомы неметаллов и неметаллы с водородом;
Ковалентная связь – возникает между атомами в результате образования общих электронных пар.
Основные положения метода валентных связей:
1) В образовании химической связи участвуют только неспаренные электроны внешней электронной оболочки.
В20 сигма σ, пи π и дельта связи
Сигма-, пи- и дельта-связь. Сигма-связь (s-связь): перекрывание валентных орбиталей происходит вдоль линии связи, т.е. линии, соединяющей ядра взаимодействующих атомов. Пи-связь (p-связь): перекрывание орбиталей происходит в направлении, перпендикулярном линии связи (боковое перекрывание). Дельта-связь (d-связь): перекрывающиеся орбитали расположены в двух параллельных плоскостях, перпендикулярных линии связи.
Химическая связь, для которой линия, соединяющая атомные ядра, является осью симметрии связывающего электронного облака, называется сигма (σ)-связью. Она возникает при «лобовом» перекрывании атомных орбиталей. Связи при перекрывании s-s-орбиталей в молекуле Н2; р-р-орбиталей в молекуле Cl2 и s-p-орбиталей в молекуле НСl являются сигма связями. Возможно «боковое» перекрывание атомных орбиталей. При перекрывании р-электронных облаков, ориентированных перпендикулярно оси связи, т.е. по оси у- и z-осям, образуются две области перекрывания, расположенные по обе стороны от этой оси. Такая ковалентная связь называется пи (p)-связью.
Перекрывание электронных облаков при образовании π-связи меньше. Кроме того, области перекрывания лежат дальше от ядер, чем при образовании σ-связи. Вследствие этих причин π-связь обладает меньшей прочностью по сравнению с σ-связью. Поэтому энергия двойной связи меньше удвоенной энергии одинарной связи, которая всегда является σ-связью. Кроме того, σ-связь имеет осевую, цилиндрическую симметрию и представляет собой тело вращения вокруг линии, соединяющей атомные ядра. π-Связь, наоборот, не обладает цилиндрической симметрией.
Одинарная связь всегда является чистой или гибридной σ-связью. Двойная же связь состоит из одной σ- и одной π-связей, расположенных перпендикулярно друг относительно друга. σ-Связь прочнее π-связи. В соединениях с кратными связями обязательно присутствует одна σ-связь и одна или две π-связи.
 2015-07-21
2015-07-21 23916
23916
