Напишите реакции получения нитрида и гидроксида бария и разложения их водой. К окислительно-восстановительным реакциям составьте электронные уравнения.
Решение.
Уже при комнатной температуре щелочноземельные металлы медленно взаимодействуют с азотом, образуя нитриды. Для получения нитридов металлы нагревают до 900 °С в атмосфере азота. Процесс протекает по уравнению
3Ba0 + N 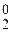 = Ba
= Ba 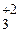 N
N 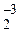 .
.
3 | Ba0 – 2 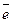 = Ba+2,
= Ba+2,
1 | N 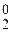 + 6
+ 6 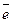 = 2N–3.
= 2N–3.
Разложение нитрида бария водой протекает по реакции
Ba3N2 + 6H2O = 3Ba(OH)2 + 2NH3.
Щелочноземельные металлы соединяются с водородом, образуя гидриды, аналогичные гидридам щелочных металлов:
Ba0 + H20 = Ba+2H2-1.
H20 + 2 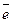 = 2H–1,
= 2H–1,
Ba0 – 2 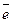 = Ba+2.
= Ba+2.
Гидрид бария бурно реагирует с водой, выделяя водород:
BaH2–1 + 2H2O = Ba(OH)2 + 2H 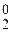 .
.
2H–1 – 2 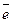 = H
= H 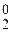 ,
,
2H+1 + 2 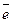 = H
= H 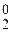 .
.
 2015-06-24
2015-06-24 974
974








