| Степень диссоциации, α | • отношение числа молекул растворенного вещества (N), продиссоциировавших на ионы, к общему числу молекул (N0) этого вещества: N α = —— N0 |
| Константа диссоциации, K | • константа равновесия процесса диссоциации;
для процесса диссоциации:
AmBn↔mAn+ + nBm−,
[An+]m ∙ [Bm-]n
 K =
[AmBn] K =
[AmBn]
|
| Закон разбавления Оствальда (связь степени и константы диссоциации) | • Cм α 2
K = ———,
1 – α
или учитывая, что для слабых электролитов α<<1, получаем выражения более простого вида: K≈ Cм α 2
и 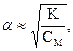 где α – степень диссоциации,
K – константа диссоциации
Cм – молярная концентрация раствора
где α – степень диссоциации,
K – константа диссоциации
Cм – молярная концентрация раствора
|
| Диссоциация многоосновных кислот | • в наибольшей степени протекает по первой ступени, при переходе к каждой последующей ступени степень диссоциации и константа диссоциации сильно уменьшаются: H3PO4 ó H+ + H2PO4‾ K1 = 7,5∙10-3 H3PO4 ó H+ + HPO42‾ K2 =6,3∙10-8 H3PO4 ó H+ + PO43‾ K3 =1,3∙10-12 |
| Изотони-ческий коэффициент, i | • показывает, во сколько раз наблюдаемые на опыте осмотическое давление (P'осм.), повышение температуры кипения (Δt'кип.), понижение температуры кристаллизации (Δt'кр) данного электролита больше значений тех же величин, вычисленных без учета диссоциации: P'осм. Δt'кип. Δt'кр i = —— = —— = —— Pосм. Δtкип. Δtкр. |
| Связь α и i | • i -1 α = ——, n-1 где n – число ионов, на которые распадается одна молекула электролита. Например, для KCl n=2, а для CuCl2 и K2S n=3 |
Свойства растворов слабых электролитов
|
|

Сейчас читают про:
 2015-06-26
2015-06-26 683
683







