Ц е л ь р а б о т ы - определить содержание сырого протеина в мышечной ткани.
Метод Конвея позволяет отрывать от 1 до 10 мкмоль азота в пробе. Первым этапом является сжигание биологического материала с образованием соли аммония. В условиях изотермической перегонки аммиак, вытесненный из растворов солей аммония сильными щелочами, поглощается кислотой. Остаток кислоты титруют щелочью или (NH4)2SO4, подвергают нсолеризации. Рассчитывают содержание азота в пробе. Изотермическую перегонку (разложение солей аммония щелочью и поглощение аммиака кислотой) осуществляют в специальных чашках Конвея.
Чашки Конвея - кристаллизаторы с низкими стенками, в центральную часть которых впаян внутренний цилиндр. Чешка плотно закрывается стеклянной крышкой, пришлифованной к внешнему цилиндру.
Оборудование, реактивы:
Чашки Конвея; H2SO4 (0,01н раствор); NaOH (0,01н раствор); K2CO3 (насыщ.);индикатор Ташира; реактив Несслера (раствор комплексной соли K2 [HgJ4] в KOH).
Приготовление и н д и к а т о р а Т а ш и р а:
Индикатор Ташира - смесь метилового красного и метиленовой сини. Окраска метилового красного на фоне метиленовой сини в кислом растворе будет фиолетово-красной, в щелочном - зеленой.
Основной раствор: смешивают 40 мл 0,1%-го спиртового раствора метилового красного и 10 мл 0,1%-го спиртового раствора метиленовой сини. Для приготовления рабочего раствора смешивают один объем основного раствора, один объем спирта и два объема воды.
Приготовление р е а к т и в а Н е с с л е р а: в 15 мл воды растворяют 10 г KJ, добавляют 15 г HgJ2, тщательно перемешивают и добавляют 80 мл 50%-го раствора NaOH (не содержащего Na2CO3). Перемешивают и доводят общий объем водой, не содержащей CO2, до 500 мл. Оставляют на сутки, после чего фильтруют через стеклянную вату. Раствор должен быть прозрачным.
1. Минерализация биологического материала.
Пробу, содержащую 10-20 мг белка (0,1 г мышечной ткани или 2 мл 1%-го раствора белка), помещают в колбу Къельдаля, добавляют 0,5 мл концентрированной серной кислоты и проводят минерализацию. Параллельно проводят контрольную пробу с дистиллированной водой (2 мл). Для проведения минерализации пробу нагревают до тех пор, пока полностью выпарится вода и и раствор в колбе приобретет бурую окраску. После этого колбу охлаждают, добавляют 2-3 капли пергидроля и раствор снова нагревают в течение 5-10 мин. Если раствор при этом побуреет, добавляют новую порцию пергидроля. По окончании минерализации содержимое колбы Къльдаля количественно переносят в мерную колбу на 25-50 мл, добавляя небольшими порциями воду и тщательно ополаскивая колбу Къельдаля. Осторожно нейтрализуют до слабокислой реакции на метиловый красный (индикатор добавляют в пробу, следя за тем, чтобы реакция не стала щелочной) доводят водой до метки. Из раствора берут пробу для определения аммиака.
2. Изотермическая перегонка аммиака.
Перед заполнением чашки на ее шлиф наносят вакуумную смазку или смесь из воска и вазелина. Во внутренний цилиндр наливают 1 мл 0,005-0,01 н раствора
H2SO4, чашку слегка наклоняют и во внешний цилиндр помещают 1 мл исследуемого раствора (необходимо следить за тем, чтобы раствор не растекался по всей поверхности чашки). Возвращают чашку в горизонтальное положение и, придерживая левой рукой крышку, в противоположный конец внешней части чашки наливают 1 мл насыщенного раствора карбоната калия. Чашку быстро закрывают и вращательными движениями перемешивают содержимое внешнего цилиндра. Ставят на 2 часа в термостат при 370С или оставляют на 24 часа при комнатной температуре. После этого определяют количество аммиака во внутреннем цилиндре методом титрования или несолеризации (взаимодействие с реактивом Несслера).
3. Определение аммиака методом титрования.
Во внутренний цилиндр чашки добавляют 1-2 капли индикатора Ташира и титруют 0,005-0,01 н раствором NaOH до появления зеленого окрашивания. При правильном приготовлении индикатора переход окраски от фиолетовой к зеленой происходит от одной капли щелочи. Параллельно проводят контрольный опыт. По разности в количестве щелочи, пошедшей на титрование контрольной и опытной проб, рассчитывают содержание общего азота, учитывая, что 1 мл 0,01 н раствора H2O4 связывает 0,14 мг азота.
Расчетные формулы: m(N) = 0,14 (n2 - n1)P,
где m(N) – масса азота, мг; 0,14 – масса азота, соответствующая 1 мл 0,01 н раствора H2SO4; n2 – объем NaOH, пошедший на титрование контрольной пробы, мл; n1 - объем NaOH, пошедший на титрование опытной пробы, мл;
Р = 25 - разведение.
w (белка) = m (белка)
m (пробы) * 100%,
где m (белка) = 6,25 * m(N), мг; m (белка) - масса сырого протеина.
4. Фотоколориметрический метод определения аммиака с реактивом Несслера.
Реактив Несслера с аммиаком образует красно-коричневый осадок. При малых количествах NH3 осадок не образуется, раствор приобретает желто-оранжевую окраску, интенсивность которой зависит от количества NH3.
Схема реакции Несслера:
Hg
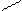
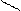
 NH4+ + 2[HgJ4]2- + 4OH- O NH4 J¯ + 7J- + 3H2O
NH4+ + 2[HgJ4]2- + 4OH- O NH4 J¯ + 7J- + 3H2O
Hg
Иодид меркуроаммония
Из внутреннего цилиндра чашки Конвея отбирают в пробирку 0,2 мл раствора, приливают 9,5 мл 0,002 н раствора H2SO4, 0,3 мл реактива Несслера. Содержимое пробирки тщательно перемешивают, оставляют на 5 мин при комнатной температуре - раствор приобретает желто-коричневую окраску.
Фотоколориметрирование проводят при длине волны 540 нм. По калибровочной кривой определяют содержание азота, пересчитывают на белок.
Построение калибровочного графика:
 Для построения калибровочного графика используют исходный 0,01 н раствор сернокислого аммония (NH4)2SO4. Методом разведения готовят 8 рабочих растворов (NH4)2SO4. Из каждого раствора отбирают по 0,2 мл пробы, добавляют по 9,5 мл 0,002 н раствора H2SO4 и по 0,3 мл реактива Несслера. Содержимое пробирок тщательно перемешивают, растворы приобретают желто-коричневую окраску. Фотоколориметрирование проводят при длине волны 540 нм. Строят зависимость D m(N).
Для построения калибровочного графика используют исходный 0,01 н раствор сернокислого аммония (NH4)2SO4. Методом разведения готовят 8 рабочих растворов (NH4)2SO4. Из каждого раствора отбирают по 0,2 мл пробы, добавляют по 9,5 мл 0,002 н раствора H2SO4 и по 0,3 мл реактива Несслера. Содержимое пробирок тщательно перемешивают, растворы приобретают желто-коричневую окраску. Фотоколориметрирование проводят при длине волны 540 нм. Строят зависимость D m(N).
 2015-06-26
2015-06-26 1216
1216








