В этом вопросе можно выделить несколько различных подходов к расчёту 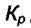 для любой температуры Т. Сам вид уравнения
для любой температуры Т. Сам вид уравнения
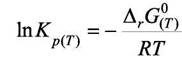
|
(7.13)
указывает на первую возможность такого расчёта. Так как
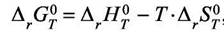
|
то надо знать 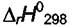 ,
, 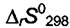 и
и 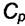 , каждого участника реакции и можно
, каждого участника реакции и можно
вычислить 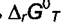 , а затем по формуле (7.13) вычислить и
, а затем по формуле (7.13) вычислить и 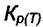
Второй подход состоит в использовании уравнения Гиббса -Гельмгольца, записанного для реакции
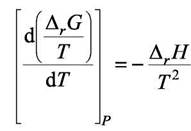
|
Продифференцируем (7.13) по температуре при постоянном р
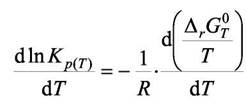
|
и используя уравнение Гиббса изобары Вант Гоффа:
- Гельмгольца, получим уравнение
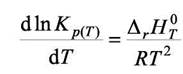
|
(7.14)
Если принять 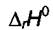 не зависящей от температуры (небольшой диапазон температур или
не зависящей от температуры (небольшой диапазон температур или 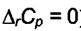 ΔrСр=0), то (7.14) можно записать в интегральной форме
ΔrСр=0), то (7.14) можно записать в интегральной форме
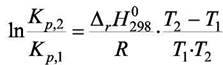
|
(7.15)
Уравнение (7.15) можно использовать и в случае грубых оценок Кр для любых температур, учитывая, что при больших абсолютных значениях
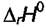 слабо меняется с температурой. В таких расчётах надо знать
слабо меняется с температурой. В таких расчётах надо знать 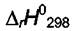 и значение
и значение 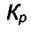 при одной температуре.
при одной температуре.
Формула (7.14) даёт возможность и точного расчёта 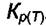 . Надо помнить, что
. Надо помнить, что 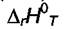 включает в себя и члены с энтальпиями
включает в себя и члены с энтальпиями
конденсированных фаз, несмотря на то, что в 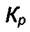 входят только газовые компоненты. Получим эту формулу. Используем закон Кирхгофа в виде
входят только газовые компоненты. Получим эту формулу. Используем закон Кирхгофа в виде
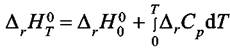
где 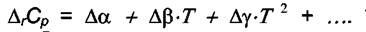 Тогда
Тогда 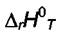 запишется
запишется
 2015-07-04
2015-07-04 471
471








