ЗАНЯТТЯ 4 (2години)
Тема: Регуляція ферментативних процесів. Інгібітори та активатори ферментів. Медична ензимологія. Кількісне визначення активності α-амілази та лактатдегідрогенази у сироватці крові.
Актуальність. Досягнення ензимології (науки про ферменти) широко впроваджуються в медицину. Розвиток медичної ензимології відбувається у трьох головних напрямках (ензимопатологія, ензимодіагностика та ензимотерапія), що дозволяє вирішувати проблеми патогенезу ензимопатій, застосовувати ферментні тести для діагностики органічних і функціональних розладів органів та тканин, а також використовувати ферменти і модулятори їхньої дії як лікарські засоби. Так, підвищення активності лужної фосфатази у сироватці крові спостерігається при рахиті, пухлинах кісткової тканини, гіперпаратиреозі, механічній жовтяниці, вірусному гепатиті, а зниження – при гіпотиреозі, гіповітамінозі С та ін. Активність лактатдегідрогенази збільшується у хворих із пошкодженням міокарда, скелетних м’язів, нирок, а також при анеміях, пухлинах, гострому гепатиті. Ферменти – пепсин, трипсин, гіалуронідаза та інші – використовуються як лікувальні препарати, а також у клініко-біохімічних лабораторіях як аналітичні реактиви (глюкозооксидаза, уреаза та ін.).
Мета. Вивчити та вміти аналізувати механізми регуляції ферментативних процесів як основи обміну речовин в організмі в нормі та при патологіях; зміни перебігу ферментативних процесів та накопичення проміжних продуктів метаболізму при вроджених (спадкових) та набутих вадах метаболізму – ензимопатіях; зміни активності індикаторних ферментів плазми крові при патологіях певних органів та тканин; застосування ферментів та їх модуляторів як фармакологічних препаратів при певних патологічних станах. Ознайомитися з методами кількісного визначення активностей α-амілази і лактатдегідрогенази у сироватці крові та їх клініко-діагностичним значенням.
ЗАВДАННЯ ДЛЯ САМОСТІЙНОЇ РОБОТИ
ПІД ЧАС ПІДГОТОВКИ ДО ЗАНЯТТЯ
ТЕОРЕТИЧНІ ПИТАННЯ
1. Регуляція ферментативних процесів, її шляхи та механізми: алостеричні взаємодії у ферментах, ковалентна модифікація ферментів, дія регуляторних білків-ефекторів (кальмодуліну, протеїназ, протеїназних інгібіторів). Циклічні нуклеотиди як регулятори ферментативних реакцій та біологічних функцій клітини.
2. Інгібітори та активатори ферментів. Типи інгібування ферментів: оборотне (конкурентне, неконкурентне, безконкурентне) і необоротне. Приклади.
3. Основні аспекти сучасної ензимодіагностики. Індикаторні, секреторні та екскреторні ферменти. Ізоферменти в ензимодіагностиці, тканинна специфічність розподілу ізоферментів. Зміни активності ферментів плазми та сироватки крові як діагностичні показники розвитку патологічних процесів в органах і тканинах.
4. Порушення перебігу ферментативних процесів: природжені (спадкові) та набуті ензимопатії, природжені вади метаболізму, їх клініко-лабораторна діагностика.
5. Ензимотерапія – використання ферментів як лікарських засобів. Фармакологічне застосування ферментів шлунково-кишкового тракту, згортальної та фібринолітичної систем крові, калікреїн-кінінової та ренін-ангіотензинової систем. Інгібітори ферментів як лікарські засоби.
ТЕСТОВІ ЗАВДАННЯ ДЛЯ САМОКОНТРОЛЮ
1. Назвіть активатор амілази слини.
| А. Хлорід натрію. | С. Сульфат міді. | Е. Глюконат кальцію. |
| В. Сульфат амонію. | D. Хлорид магнію. |
2. Укажіть тип інгібування, при якому інгібітором ферменту є продукт реакції.
| А. Конкурентне. | С. Безконкурентне. | Е. Ретроінгібування. |
| В. Неконкурентне. | D. Стереохімічне. |
3. Позначте фермент, активність якого слід визначати в сечі пацієнта при гострому панкреатиті.
| А. Амілаза. | D. Лейцинамінопептидаза. |
| В. Протеїнкіназа. | Е. Лужна фосфатаза. |
| С. Холінестераза. |
4. Укажіть патологію, при якій значення активності амілази крові зростає в 10 і більше разів.
| А. Вірусний гепатит. | D. Інфаркт міокарда. |
| В. Гострий панкреатит. | Е. Цукровий діабет. |
| С. Хронічний холецистит. |
5. Назвіть фермент, активність якого визначають у плазмі крові пацієнтів із патологією кісткової тканини.
| А. Пепсин. | С. Амілаза. | Е. Лужна фосфатаза. |
| В. Трипсин. | D. Кисла фосфатаза. |
6. Для оцінки ступеню поразки паренхіми печінки у пацієнтів визначають:
А. Концентрацію ізоформ ЛДГ1 і ЛДГ2 плазми крові.
В. Концентрацію ізоформ ЛДГ4 і ЛДГ5 плазми крові.
С. Активність амілази сечі.
D. Активність кислої фосфатази.
Е. Концентрацію ізоформи ЛДГ3 плазми крові.
7. Укажіть ізоформи ЛДГ, концентрація яких збільшується у плазмі крові пацієнтів з інфарктом міокарда.
| А. ЛДГ1 і ЛДГ2. | С. Тільки ЛДГ3. | Е. Тільки ЛДГ5. |
| В. ЛДГ3 і ЛДГ4. | D. ЛДГ4 і ЛДГ5. |
8. Назвіть фермент плазми крові, який використовують у терапевтичній практиці для зниження кров’яного тиску.
| А. Ізоформа ЛДГ1. | С. Хімотрипсин. | Е. Калікреїн. |
| В. Трипсин. | D. Холінестераза. |
9. Який механізм інгібування синтезу фолієвої кислоти сульфаніламідними препаратами?
| А. Конкурентний. | D. Неконкурентний. |
| В. Необоротний. | Е. Зв’язування з алостеричними центрами ферментів. |
| С. Денатурація ферменту. |
ПРАКТИЧНА РОБОТА
Кількісне визначення активності α-амілази у сироватці крові
за методом Каравея
Завдання. Визначити активність α-амілази у сироватці крові за методом Каравея.
Принцип методу. α-Амілаза (α-1,4-глюкан-4-глюканогідролаза; КФ 3.2.1.1) каталізує гідролітичне розщеплення крохмалю з утворенням кінцевих продуктів, які не дають забарвлення з йодом. Про активність ферменту судять за надлишком крохмалю, який визначають спектрофотометричним методом за зміною забарвлення йодо-крохмального розчину.
Хід роботи. Визначення активності α-амілази у сироватці крові провести за наступною схемою.
| Хімічний посуд | Об’єм піпетки, мл | Реактиви | Проба, мл | Контроль, мл | Етапи |
| Хімічні пробірки | субстратно-буферний розчин | перед-інкубація | |||
| Інкубувати 5 хв при температурі 37 °С | |||||
| 0,1 | сироватка крові | 0,02 | - | ||
| змішати, інкубувати протягом 7,5 хв при температурі 37 °С (ферментативна реакція) | |||||
| робочий розчин йоду | кольорова реакція | ||||
| 0,1 | сироватка крові | - | 0,02 | ||
| дистильована вода | до 10 | до 10 | |||
| змішати, виміряти Епр і Ек при довжині хвилі 630–690 нм у кюветі (10 мм) проти дистильованої води протягом 5 хв (фотометрія) |
Активність α-амілази у сироватці крові розрахувати за наступною формулою:
активність α-амілази г/л∙год = 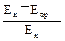 × 160×К,
× 160×К,
де Ек – екстинкція контролю, Епр – екстинкція проби, 160 – коефіцієнт розрахунку, який враховує кількість крохмалю, введеного в пробу і контроль, на 1 л біологічної рідини за 1 год інкубації при температурі 37 °С; К – коефіцієнт розбавлення досліджуваної сироватки крові.
Клініко-діагностичне значення. У нормі активність α-амілази в сироватці крові становить 12–32 г/(год×л). При захворюваннях підшлункової залози спостерігають її підвищення у крові та сечі. При гострому панкреатиті активність α-амілази підвищується в 10–30 разів, стає максимальною на першу добу хвороби, а на другу-шосту - швидко нормалізується. Гіперамілаземія також трапляється при гострому апендициті, перфоративній виразці шлунка та дванадцятипалої кишки, холециститі, розриві жовчного міхура, опіках, травматичному шоку, пневмонії, простатиті, уремії. Підвищенню активності α-амілази сприяють лікарські препарати (кортикостероїди, катехоламіни, фуросемід, антикоагулянти), наркотики, алкоголь. Зниження її активності спостерігають при гепатиті, цирозі, злоякісних утвореннях печінки, цукровому діабеті, гіпотиреозі, кахексії.
Кількісне визначення активності лактатдегідрогенази (КФ 1.1.1.27)
у сироватці крові за Севелом і Товареком
Завдання. Визначити активність лактатдегідрогенази (ЛДГ) у сироватці крові за Савелом і Товареком.
Принцип методу. Під впливом ЛДГ L-лактат за наявності нікотинамідаденіндинуклеотиду (НАД) окислюється до пірувату. Кількість утвореного пірувату визначають фотометрично за кольоровою реакцією з 2,4-динітрофенілгідразином, в якій утворюється 2,4-динітрофенілгідразон, що має червоно-буре забарвлення в лужному середовищі, його інтенсивність прямо пропорційна вмісту кетокислоти.
ЛДГ
СН3-СН(ОН)-СООН + НАД+ → СН3-СО-СООН + НАДН(Н+)
лактат піруват
Хід роботи. В одну пробірку вносять 0,1 мл розведеної у 3 рази сироватки крові, 0,3 мл свіжовиготовленого розчину 0,02 моль/л НАД+ і ставлять на 5 хв на водяну баню при 37 °С для нагрівання суміші. У другу пробірку вносять 0,8 мл розчину 0,03 моль/л натрію пірофосфату, 0,2 мл розчину 0,45 моль/л натрію лактату і нагрівають на водяній бані при 37 °С. Виливають вміст другої пробірки в першу, швидко перемішують скляною паличкою, не виймаючи пробірки з бані, й відзначають час початку інкубації. Через 25 хв реакцію припиняють додаванням 0,5 мл 0,2% розчину 2,4-динітрофенілгідразину в розчині 1 моль/л хлоридної кислоти і залишають пробірку на 20 хв при кімнатній температурі для утворення гідразону. До суміші додають 5 мл розчину 0,4 моль/л натрію гідроксиду, перемішують скляною паличкою і через 10 хв вимірюють екстинкцію дослідної проби проти контрольної на ФЕК при довжині хвилі 520-560 нм у 10 мм кюветах. Контрольну пробу готують так само як і дослідну, але розведену сироватку додають після інкубації. Активність ферменту розраховують за калібрувальним графіком, умови побудови якого наведені в таблиці.
| № пробірки | Робочий стандартний розчин натрію пірувату, мл | Розчин 0,03 моль/л натрію пірофос-фату, мл | Дист. вода, мл | Вміст пірувату в пробі, мкмоль | Одиниці активності ЛДГ ммоль/л×год | Екс-тинкція |
| 0,1 | 0,8 | 0,5 | 0,01 | 1,2 | ||
| 0,2 | 0,8 | 0,4 | 0,02 | 2,4 | ||
| 0,4 | 0,8 | 0,2 | 0,04 | 4,8 | ||
| 0,6 | 0,8 | - | 0,06 | 7,2 | ||
| 0,8 | 0,8 | - | 0,08 | 9,6 |
На осі ординат відкладають значення екстинкції, а на осі абсцис – відповідні їм одиниці активності ЛДГ, виражені в ммоль/л∙год.
Клініко-діагностичне значення. Визначення активності ЛДГ використовують у клініко-біохімічних лабораторіях для діагностики захворювань, а також як тест на одужання. У нормі активність ферменту в сироватці крові становить 0,8–4,0 ммоль/л×год. Вона підвищується при ушкодженні міокарда, лейкозі, хворобі нирок, гемолітичній та серпоподібноклітинній анемії, тромбоцитопенії, інфекційному мононуклеозі, а також прогресуючій м’язовій дистрофії. При хворобах, які супроводжуються некрозом тканин (інфаркт міокарда, некротичні ураження нирок, гепатит, панкреатит, пухлини) спостерігають різке підвищення активності ЛДГ у сироватці крові. При гострому гепатиті вона підвищується в перший тиждень жовтяничного періоду, при легких та середньої важкості формах хвороби швидко нормалізується. У хворих із гострим інфарктом міокарда спостерігається підвищення загальної ЛДГ та ЛДГ1 у сироватці крові через 8–18 год після початку нападу, яке досягає максимуму через 24–72 год. Активність ферментів залишається високою протягом першого тижня і нормалізується на 6–10-й день. Також має значення визначення співвідношення ЛДГ1/ЛДГ2, яке у нормі складає 0,4–0,74, а при гострому інфаркті міокарда зростає у 5–10 разів. При стенокардії активність ЛДГ у сироватці крові не підвищується.
 2015-07-03
2015-07-03 1213
1213








