Смачивание есть взаимодействие жидкости с твердым телом в присутствии газа или другой жидкости, которая не смешивается с первой. На границе раздела фаз молекулы, расположенные на соприкасающихся поверхностях, притягиваются за счет сил Ван-дер-Ваальса (ориентационное, индукционное и дисперсионное взаимодействие) или посредством водородных связей.
Мерой смачивания является угол смачивания или краевой угол. Краевой угол q определяется наклоном поверхности капли жидкости к смоченной ею поверхности твердого тела в точке соприкосновения фаз со стороны жидкости (рис. 5).
Изменение краевого угла в пределах 0 < q < 1800, охватывает все случаи смачивания. Значение q = 00 соответствует полному смачиванию. Например, капля воды на обезжиренной стеклянной поверхности растекается и покроет поверхность стекла тонкой пленкой (q = 0). Растекание жидкости происходит потому, что молекулы воды (диполи) притягиваются поверхностью, молекулярная структура которой обеспечивает ориентационное, индукционное или дисперсионное взаимодействие с аморфной поверхностью стекла. Изменение угла q в пределах 00 < q < 900 указывает на ограниченное смачивание. Несмачиванию соответствует угол 900 < q < 1800. Различное смачивание водой поверхности стекла,графита и парафина представлено на рис. 5.
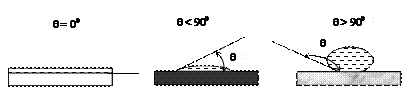
Рис. 5. Положение капли воды на твердых поверхностях при различных условиях смачивания: а) гидрофильное обезжиренное стекло; б)графит; в) парафин, проявляет гидрофобные свойства
Поверхность проявляет гидрофильные (др.-греч. ugroV влажный; jilew люблю) свойства, если она хорошо смачивается водой (обезжиренное стекло). Гидрофобные (др.-греч. ugroV влажный; joboV страх, ужас) свойства, т.е. плохое смачивание водой, наблюдается у парафина. Когда речь идет о жидкостях, отличающихся от воды, то поверхности по условиям смачивания подразделяются соответственно на лиофильные и лиофобные.
Уменьшение функции Гиббса (приходящееся на единицу поверхности) 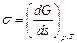 < 0 соответствует протеканию самопроизвольного процесса, сопровождающегося уменьшением поверхностного натяжения. В самопроизвольном процессе капля жидкости будет растекаться и покрывать поверхность твердого тела с уменьшением краевого угла q до минимального значения. Это соответствует уменьшению поверхностного натяжения (sт-ж ) на границе твердое тело – жидкость по сравнению с поверхностным натяжением (sт-г ) твердое тело – газ:
< 0 соответствует протеканию самопроизвольного процесса, сопровождающегося уменьшением поверхностного натяжения. В самопроизвольном процессе капля жидкости будет растекаться и покрывать поверхность твердого тела с уменьшением краевого угла q до минимального значения. Это соответствует уменьшению поверхностного натяжения (sт-ж ) на границе твердое тело – жидкость по сравнению с поверхностным натяжением (sт-г ) твердое тело – газ:
sт-г - sт-ж> 0.
Равновесное (устойчивое) состояние (рис. 6) будет достигнуто, когда равнодействующая поверхностного натяжения трех фаз равна нулю (уравнение Юнга):
sт-г - sт-ж - sж-г cos q = 0 или
cos q = (sт-г - sт-ж)/sж-г.
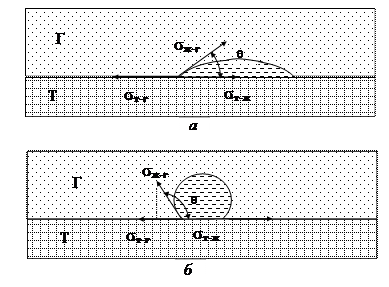
Рис. 6. Распределение энергии поверхностного натяжения: а) на гидрофильной поверхности (q < 900); б) на гидрофобной поверхности (q > 900)
Из уравнения Юнга следует, что при sт-г - sт-ж> 0 значение cos q > 0, и тогда q изменяется в пределах от 00 до 900. Величина краевого угла свидетельствует об эффективности смачивания, эффективности контактного взаимодействия жидкости с поверхностью твердого тела.
Если sт-г - sт-ж < 0, то значение cos q < 0, и q изменяется в пределах от 900 до 1800, что означает плохое смачивание или отсутствие смачивания поверхности жидкостью. В последнем случае ярко выражено более сильное взаимодействие между молекулами внутри жидкости по сравнению с взаимодействием молекул на границе двух фаз.
Изменение степени смачивания происходит при использовании поверхностно-активных веществ (ПАВ) и означает изменение поверхностной энергии на границе раздела фаз.
 2015-07-03
2015-07-03 652
652








