Метод основан на окислении альдегидной группы сахаров (глюкозы, лактозы) йодом в щелочной среде. Массовую долю сахарозы определяют по разности между количеством взятого и неизрасходованного йода, определяемого титрованием тиосульфата натрия.
СН2ОН-(СНОН)4-СНО + I2+ 3NaOH = CH2OH-(CHOH)4-COONa +2H2O + 2NaI
I2 + 2 Na2S2O3 = NaI + Na2S4O6
Для протекания реакции необходимо чтобы йода было в 2-3 раза было больше, чем требуется для окисления глюкозы, щелочи должно быть в полтора раза больше по объему, чем раствора йода. Индикатором служит раствор крахмала. Определению предшествует холостой опыт, в котором устанавливается соотношение между раствором йода и тиосульфатом натрия.
Реактивы: гидроксид натрия, растворы 0,1 н. и 1 н; 15 %-ого раствора железистосинеродистого калия, 30 %-ого раствора сульфата цинка сульфат меди; йод, 0,5 н. раствор соляной кислоты; тиосульфат натрия, 0,1н. раствор, крахмал растворимый, 1%-ный раствор, сахароза, ч.д.а.
Материалы. оборудование: электрическая водяная баня; термометр ртутный стеклянный с пределом измерения 150 оС; мерные колбы вместимостью на 100 и 250 см3; фарфоровая ступка с пестиком; пипетка вместимостью 5,10, 50 см3, конические колбы вместимостью 100, 250 см3; мерный цилиндр вместимостью 10 см3.
Проведение анализа. Из подготовленной пробы в химический стакан вместимостью 25 -50 см взвешивают навеску массой около 5 г с точностью ±0,01 г, добавляют в него 10 см 3 воды и тщательно перемешивают стеклянной палочкой. Полученную массу количественно переносят в коническую колбу на 250 см 3, остатки смывают со стенок стакана 30-40 см дистиллированной воды. В мерную колбу добавляют 3 см 3 15 %-ого раствора железистосинеродистого калия К4 [Ре+2(СН)6] и 3 см3 30 %-ого раствора сульфата цинка. Содержимое тщательно перемешивают и через 10-15 мин доводят до метки дистиллированной водой и фильтруют содержимое колбы в сухую колбу через бумажный фильтр. В коническую колбу на 200 см3 помещают 10 см3 полученного фильтрата, приливают по 25 см3 0,1 н раствора йода и при перемешивании 35 см3 0,1 н раствора NaOH. Колбу закрывают и помещают в темное место на 20 мин. Затем в колбу приливают и 10 см3 0,5 н раствора соляной кислоты. Выделившийся йод титруют 0,1 н раствором тиосульфата натрия до появления светло-желтой окраски. Затем к раствору добавляют 1 см3 крахмала и продолжают титровать, до исчезновения синей окраски.
Параллельно проводят контрольный опыт, в котором вместо водной вытяжки берут дистиллированную воду.
Массу глюкозы (Х1) в процентах рассчитывают по формуле:
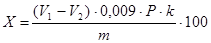 , (4.12)
, (4.12)
где V1 - объем 0,1 н раствора тиосульфата, израсходованный на титрование в контрольном опыте, мл; V2- объем 0,1 н раствора тиосульфата, израсходованный на титрование в рабочем опыте, мл; 0,009 количество глюкозы, соответствующее 1 мл 0,1 н раствора йода; Р- фактор разведения.
Расхождения между параллельными определениями не должны. превышать 0,3 %.
 2015-07-04
2015-07-04 2399
2399








