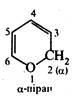
3.7.1. α-Піран і γ-піран
 а
а 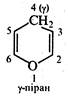 α-Піран (2Н-піран) і γ-піран (4Н-піран) являють собою шестичленні гетероциклічні сполуки, що містять як гетероатом один атом кисню.
α-Піран (2Н-піран) і γ-піран (4Н-піран) являють собою шестичленні гетероциклічні сполуки, що містять як гетероатом один атом кисню.
Ці гетероцикли є структурними ізомерами та відрізняються один від одного розміщенням метиленової групи відносно гетероатома. В молекулі α-пірану метиленова група знаходиться в α-положенні, а в γ-пірані — в γ-положенні.
В α- та γ-піранах відсутня замкнена спряжена система, через що ці речовини не мають ароматичності та характеризуються низькою стабільністю. α-Піран у вільному стані не добутий. γ-Піран виділений у вигляді індивідуальної речовини, але є дуже нестійкою сполукою, що легко розкладається на повітрі. Поряд з цим оксопохідні піранів α-пірон (2Н-пірон) і γ-пірон (4Н-пірон) являють собою досить стійкі речовини.
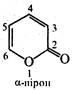
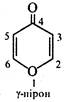 α-Пірон безбарвна рідина (т. кип. 206-209 °С) з запахом свіжого сіна, γ-пірон безбарвна кристалічна речовина (т. пл. 33 °С).
α-Пірон безбарвна рідина (т. кип. 206-209 °С) з запахом свіжого сіна, γ-пірон безбарвна кристалічна речовина (т. пл. 33 °С).
α- та у-Пірони мають у своєму складі шестичленний гетероцикл, який містить атом кисню та 5 атомів вуглецю, що перебувають у sp2 -гібридизації. Неподілена пара електронів гетероатома знаходиться у спряженні з π-електронами двох подвійних зв'язків циклу та карбонільною групою. Делокалізацію електронної густини можна подати у вигляді двох крайніх резонансних структур, одна з яких являє собою спряжений дієн, а друга — ароматичну систему, подібну піридину.
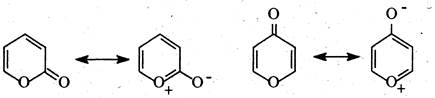
Тому α- та γ-пірони здатні вступати і в реакції, характерні спряженим дієнам, і в реакції, притаманні аренам. α-Пірон вступає переважно в реакції першого типу, тобто цей гетероцикл слід розглядати радше як ненасичений лактон.
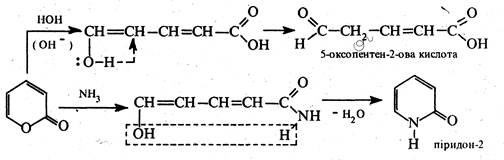
По лактонному угрупованню 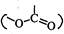 α-пірон вступає в реакції нуклеофільного приєднання, що супроводжуються розкриттям циклу. Так, у присутності лугів α-пірон легко гідролізується, під дією аміаку розкриття циклу супроводжується рециклізацієїо з утворенням піридону-2.
α-пірон вступає в реакції нуклеофільного приєднання, що супроводжуються розкриттям циклу. Так, у присутності лугів α-пірон легко гідролізується, під дією аміаку розкриття циклу супроводжується рециклізацієїо з утворенням піридону-2.
Ненасичений характер α-піронового циклу підтверджується йоги здатністю до каталітичного гідрування та до вступу в реакцію з малеїновим ангідридом за Дільсом-Альдером як 1,3-дієну.
γ-Пірон, внаслідок спряження неподіленої пари електронів гетероатома з карбонільного групою, не утворює характерних для кетонів похідних по карбонільній групі (оксимів, гідразонів, основ Шиффа) та насилу вступає в реакції приєднання за місцем розриву подвійних вуглець-вуглецевих зв'язків. При взаємодії з мінеральними кислотами (НС1, НСlО4) або алкілгалогенідами γ-пірон утворює солі пірилію:
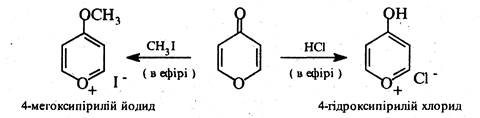
Пірилієвий катіон у солях пірилію містить замкнену π-систему з шести електронів і, таким чином, подібно бензолу або піридину має ароматичний характер.
Реакції γ-пірону з нуклеофільними реагентами, аналогічно α-пірону, як правило, супроводжуються розкриттям циклу за місцем розриву зв'язку О—С2. В присутності аміаку γ-пірон перетворюється на γ-піридон.
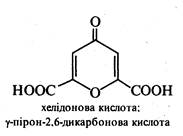
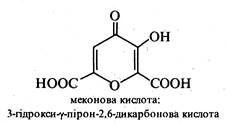
Деякі похідні γ-пірону є природними речовинами. До них відносяться хелідонова та меконова кислоти. Хелідонова кислота міститься в траві чистотілу (Chelidonium majus), меконову кислоту виділено з маку снотворного (Papaver somnifemm).
 2015-07-14
2015-07-14 1323
1323