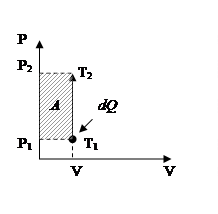
- Изохорический процесс:
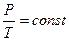 при
при 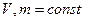
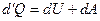 ,
, 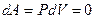 , т.к.
, т.к. 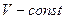
 Вся теплота идёт на приращение внутренней энергии
Вся теплота идёт на приращение внутренней энергии
Молярная теплоёмкость при постоянном объёме:
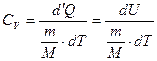
Тогда приращение внутренней энергии
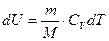 . С другой стороны:
. С другой стороны: 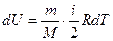 .
.
Следовательно, молярная теплоёмкость при постоянном объёме
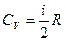
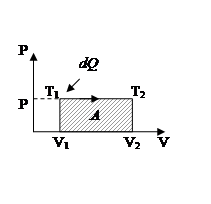
- Изобарный процесс:
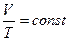 при
при 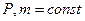
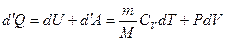
Работа при изобарном процессе: 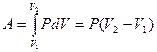
Молярная теплоёмкость при постоянном давлении
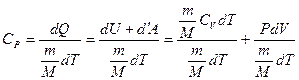
Первое слагаемое правой части даёт Сv, а второе – R – газовую постоянную. В самом деле, из уравнения 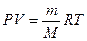 (учитывая, что P – const) следует, что
(учитывая, что P – const) следует, что 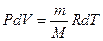 . Тогда связь между молярными и удельными теплоёмкостями (уравнения Майера) имеет вид:
. Тогда связь между молярными и удельными теплоёмкостями (уравнения Майера) имеет вид:
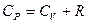 ,
, 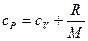
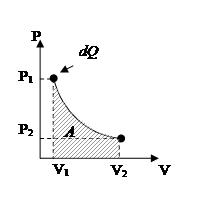
- Изотермический процесс:
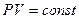 при
при 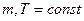
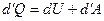
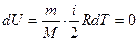 , т.к.
, т.к. 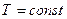
Вся теплота, сообщённая системе в ходе изотермического процесса, идёт на совершение системой работы над внешними силами.
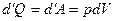 , учтем, что
, учтем, что 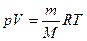 , тогда
, тогда
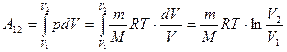
В ходе изотермического процесса внутренняя энергия системы не изменяется, 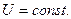
4. Адиабатический процесс – это процесс, протекающий без теплообмена с окружающей средой 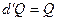 , следовательно
, следовательно 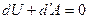
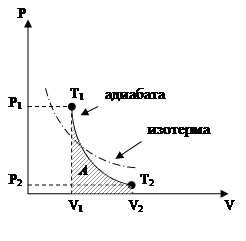
Работа в ходе адиабатического расширения осуществляется за счет убыли внутренней энергии.

Получим уравнение адиабаты. Возьмем систему (газ) в количестве 1Моль.
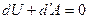 или
или 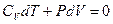 . Разделим это уравнение на уравнение Клайперона:
. Разделим это уравнение на уравнение Клайперона:
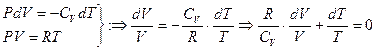 или
или 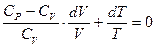
Обозначим отношение 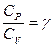 , тогда
, тогда 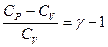
Следовательно, 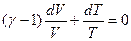 , или
, или 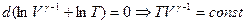
Это уравнение связывает температуру и объем газа в ходе адиабатического процесса. Из уравнения Клайперона 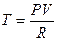 , тогда
, тогда 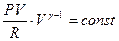 или
или 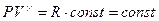
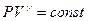 - уравнение Пуассона.
- уравнение Пуассона.
Выразим 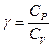 через число степеней свободы молекул газа.
через число степеней свободы молекул газа.
Молярная теплоемкость при постоянном объеме 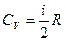 , при постоянном давлении
, при постоянном давлении 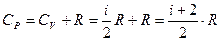
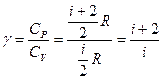
Их отношение:
 2015-07-21
2015-07-21 556
556








