Открытие двойственной природы частиц привело к пониманию о невозможности описывать поведение микрочастиц с помощью классических представлений и законов. Стало ясно, что нельзя говорить о траектории частицы, т.е. о точном ее местоположении в любой момент времени. Появилась новая наука – квантовая механика. Вместо слова траектория частицы было введено понятие о вероятности нахождения частицы в том или ином месте пространства. Для описания поведения микрочастиц Шрёдингер (1926 г) предложил дифференциальное уравнение:
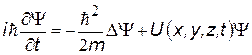 i i | нестационарное уравнение Шрёдингера; решение уравнения позволяет найти вероятность нахождения частицы в том или ином мете пространства | |
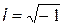 | мнимая единица | |
| m | масса рассматриваемой частицы | |
| U (x,y,z,t) | потенциальная энергия частицы, зависящая в общем случае от координат и времени | |
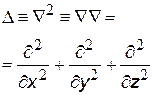 | оператор Лапласа (или лапласиан) краткое обозначение математической операции дифференцирования в частных производных; 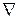 - набла (греч. слово nabla - арфа, символ по форме напоминает этот инструмент) - набла (греч. слово nabla - арфа, символ по форме напоминает этот инструмент) | |
| Y (x,y,z,t) | пси-функция или волновая функция, физического смысла не имеет, но квадрат ее модуля êYê2 – это вероятность нахождения частицы в данном месте пространства (подробнее см. дальше – стационарное уравнение Шрёдингера) | |
Математически уравнение Шрёдингера имеет бесконечное число решений, что физически неприемлемо, поэтому на пси-функцию накладываются дополнительные условия:
1).Пси-функция должна быть:
а) конечной – вероятность не может быть больше 1,
б) непрерывной – вероятность не может внезапно оборваться,
в) однозначной – не может быть две вероятности в одной точке,
2) Производные пси-функции должны быть непрерывны,
3) Пси-функция должна подчиняться условию нормировки:
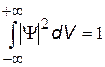 | условие нормировки; смысл его в том, что вероятность обнаружить частицу во всем мыслимом пространстве равна 1. |
В тех случаях, когда потенциальная энергия зависит только от координат и не зависит от времени, т.е U = U (x,y,z), пси-функцию можно представить как произведение двух функций: Y (x,y,z,t) = y (x,y,z)× j (t). (Y - большая буква пси,
y - малая буква пси, обе функции называются пси- или волновыми функциями.) Подставим в уравнение (i) и, разделим на (y × j).. Получим:
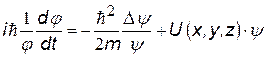 | Левая часть уравнения зависит только от t, правая – только от координат, следовательно, каждая из них должна быть равна некоторой постоянной, которую мы обозначим Е. | |||
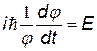 | 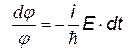 | 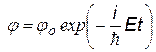 | j (t) называется временнОй частью пси-функции, со временем она затухает | |
Если приравнять константе Е правую часть уравнения, получим:
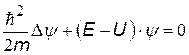 a a | стационарное уравнение Шрёдингера Е – полная энергия частицы, U – потенциальная энергия |
При решении уравнения Шредингера мы
| задаем | находим |
| U – потенциальную энергию частицы m – массу частицы | y - пси-функцию (собственные функции) Е – полную энергию частицы (собственные значения) |
Решение уравнения с учетом дополнительных условий, накладываемых на пси-функцию, приводит не к любым величинам энергии Е, а к дискретным:
Е1, Е2,…, Еn. В теории Бора электрон мог находиться тоже только в дискретных энергетических состояниях, но при этом была введена искусственно гипотеза о квантовании момента импульса электрона. Уравнение Шрёдингера приводит к квантованию энергии естественно, как математическое решение.
При решении оказывается, что данному энергетическому состоянию частицы могут соответствовать одна или несколько (к) пси-функций. Иначе говоря, при данной энергии Еn частица может вести себя по-разному. Тогда говорят, что уровень Еn к -кратно вырожден и обозначают пси-функцию как 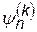 Если на систему воздействовать внешним, например магнитным полем, то вырождение снимается, уровень расщепляется на несколько уровней. Практически это обнаруживается в спектрах, вместо одной линии появляются несколько. Например, в спектре атома водорода на приборе с большим разрешением можно обнаружить, что почти все линии спектра являются дублетами.
Если на систему воздействовать внешним, например магнитным полем, то вырождение снимается, уровень расщепляется на несколько уровней. Практически это обнаруживается в спектрах, вместо одной линии появляются несколько. Например, в спектре атома водорода на приборе с большим разрешением можно обнаружить, что почти все линии спектра являются дублетами.
Рассмотрим подробнее пси-функцию.
| y - пси-функция | физического смысла не имеет | |
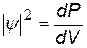 1/м3 для 3-х-мерного случая 1/м3 для 3-х-мерного случая | плотность вероятности (квадрат модуля пси-функции) – по смыслу – это вероятность того, что частица находится в единичном объеме в данном месте пространства Р – вероятность. | |
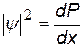 1/м для одномерного случая 1/м для одномерного случая | --²--…. вероятность того, что частица находится на единичном отрезке… | |
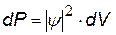 | вероятность того, что частица находится в элементарном объеме dV | |
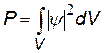 | вероятность того, что частица находится в конечном объеме V | |
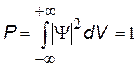 | вероятность того, что частица находится во всем пространстве | |
Уравнение Шрёдингера (a) решается точно только для упрощенных, нереальных случаев, например, электрон в одномерной потенциальной яме. Из реальных объектов уравнение можно решить точно только для атома водорода при использовании сферических координат и для иона 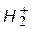 в эллиптических координатах. Во всех остальных случаях для решения применяются приближенные методы.
в эллиптических координатах. Во всех остальных случаях для решения применяются приближенные методы.
ПРИМЕНЕНИЕ УРАВНЕНИЯ ШРЁДИНГЕРА
 2015-07-14
2015-07-14 1807
1807








