ВАРИАНТ № 2
1. Определить объем SО2, (в пересчете на нормальные условия), который нужно пропустить через раствор НСlO3, чтобы восстановить 16 г этой кислоты до НСl.
2. Определить объем 0,2 М раствора К2Сr2O7, который потребуется для окисления в сернокислом растворе объемом 50 мл сернистой кислоты. 
 Плотность раствора 1,022 г/мл, массовая доля сернистой кислоты (в пересчете на SO2) 4%.
Плотность раствора 1,022 г/мл, массовая доля сернистой кислоты (в пересчете на SO2) 4%.
3. Написать формулы сульфита калия, гидросульфита калия, сульфата калия, селенита калия. Какие из этих солей подвергаются гидролизу? Написать молекулярные и ионные уравнения гидролиза. Для какой соли степень гидролиза наибольшая? Ответ обосновать.
4. Закончите уравнения химических реакций. Расставьте коэффициенты:
а) методом электронного баланса:
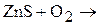
б) методом ионно-электронного баланса:
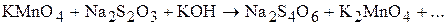
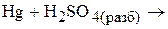
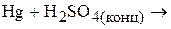
 2015-07-21
2015-07-21 546
546








