Обезуглероживание стали при нагреве происходит в результате взаимодействия печных газов с углеродом, который находится в стали или в виде твердого раствора, или в виде карбида железа Fе3С. Реакции обезуглероживания в результате взаимодействия различных газов с карбидом железа следующие:
Fе3С + Н20 = ЗFе + СО + Н2; 2Fе3С + 02 = 6Fе + 2СО; Fе3С + С02 = ЗFе + 2СО; Fе3С + 2Н2 = ЗFе + СН4.
Аналогичные реакции протекают при взаимодействии этих газов с углеродом, находящимся в твердом растворе. Установлено, что процесс обезуглероживания при взаимодействии газов с карбидом железа происходит при его предварительной диссоциации.
Скорость обезуглероживания определяется не только константами скорости записанных выше химических реакций, но также условиями процесса двусторонней диффузии.
Как константы скорости химических реакций, так и коэффициенты диффузии увеличиваются с повышением температуры. Поэтому глубина обезуглероженного слоя возрастает с увеличением температуры нагрева.
К числу газов, входящих в состав печной атмосферы и выбывающих обезуглероживание, относятся Н20, С02, 02 и Н2. Наиболее сильным обезуглероживающим воздействием на сталь обладает Н20, а наиболее слабым Н2. Обезуглероживающая способность С02 увеличивается с ростом температуры, а обезуглероживающая способность сухого Н 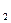 уменьшается. Водород в присутствии водяных паров оказывает очень сильное обезуглероживающее воздействие на поверхностный слой стали.
уменьшается. Водород в присутствии водяных паров оказывает очень сильное обезуглероживающее воздействие на поверхностный слой стали.
Степень обезуглероживания и глубину обезуглероженного слоя можно определить несколькими способами, из которых наиболее распространенными являются следующие: измерение твердости поверхности образца до нагрева и после него в данной атмосфере (твердость зависит от содержания углерода) и анализ микроструктуры, выявляющий картину происшедших в стали превращений. Возможно проведение химических анализов последовательно срезаемых слоев металла, а также нахождение изменения его массы.
Защита стали от окисления и обезуглероживания.
Вредное влияние окисления и обезуглероживания стали при нагреве на ее качество вызывает необходимость принимать меры, предупреждающие эти явления. Наиболее полная защита поверхности стали достигается в печах, где исключается воздействие на нее окисляющих и обезуглероживающих газов. К таким печам относятся соляные и металлические ванны, а также печи, где нагрев ведется в контролируемой атмосфере. В печах подобного типа либо от газов изолируется нагреваемый металл, обычно закрываемый специальным герметичным муфелем, либо само пламя помещается внутрь радиационных труб, тепло от которых передается нагреваемому металлу без его контакта с окисляющими и обезуглероживающими газами. Рабочее пространство таких печей заполняют специальными атмосферами, состав которых выбирают в зависимости от технологии нагрева и марки стали. Защитные атмосферы приготовляют отдельно в специальных установках.
В последнее время широкое распространение получает способ создания безокислительной атмосферы непосредственно в рабочем пространстве печей без муфелироваиия металла или пламени. Это достигается при неполном сжигании топлива (с коэффициентом расхода воздуха 0,5—0,6). В состав продуктов сгорания при этом входят Н2 и СО наряду с продуктами полного сгорания Н20 и С02. При определенном соотношении этих газов в смеси нагрев стали происходит без окисления ее поверхности.
Уменьшение окалинообразования может быть достигнуто также в результате сокращения времени нагрева металла, что осуществляют установлением наиболее рационального теплового и температурного режимов работы печей.
Основы рациональной технологии нагрева стали.
Процессы, протекающие внутри нагреваемого металла.
Важнейшими показателями процесса нагрева металла являются температура и скорость нагрева. Температурой нагрева называют конечную температуру, при которой металл выдают из печи и которая определяется целями дальнейшей обработки металла. Скорость нагрева — это изменение температуры металла во времени.
При термообработке температуру нагрева выбирают в соответствии с видом термообработки и критическими температурами, характерными для стали данной марки.
Обработка металла давлением требует такой температуры нагрева, при которой металл обладает необходимыми пластическими свойствами. Температуру нагрева металла следует выбирать с учетом того, какая минимальная температура допустима в конце обработки. На скорость нагрева накладывают ограничения те процессы, которые протекают внутри металла в процессе его нагрева. При термической обработке эти ограничения связаны со структурными изменениями металла; при нагреве перед обработкой давлением в металле возможны большая неравномерность нагрева по толщине металла и как следствие возникновение недопустимых внутренних напряжений. Чем выше скорость нагрева металла, тем больше перепад температур по толщине металла и тем значительнее возникающие при нагреве температурные напряжения.
Перепад температур связан со скоростью нагрева следующим выражением:
ΔT=Tпов-Tц=СнS2/(2а), (87)
где С 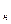 — скорость нагрева, К/с; S — толщина металла, м.
— скорость нагрева, К/с; S — толщина металла, м.
Температурные напряжения в металле опасны до возникновения в нем пластических свойств. Для стали напряжения опасны в интервале температур 273—773 К. При температуре выше 773 К напряжения исчезают в результате возникновения пластической деформации. При нагреве малоуглеродистой стали, обладающей высокой пластичностью, возникающие напряжения не опасны даже при температурах ниже 773 К. Если толщина нагреваемого материала незначительна (например, у листа), то значительный перепад температур, а следовательно, и напряжения возникнуть не могут.
Таким образом, при нагреве углеродистых и легированных сталей в интервале температур от 273 до 773 К возникающие напряжения не должны превышать максимально допустимых. Иными словами, скорость нагрева следует выбирать так, чтобы не возникали чрезмерные, недопустимые температурные напряжения, которые способны вызвать разрушение металла.
За допустимое напряжение следует принимать истинное сопротивление разрыву, на основании которого можно определить допустимую скорость нагрева.
Наибольшие по абсолютной величине напряжения сжатия, наблюдающиеся на поверхности нагреваемого металла в форме пластины, могут быть определены по формуле, Па
σ= 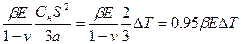 (88)
(88)
где |β — коэффициент линейного расширения, 1/К; Е — модуль упругости, Па; v — пуаоссоново отношение; для стали принято v =0,3; С 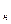 — скорость нагрева, К/с; S — толщина пластины, м; а —■ коэффициент температуропроводности, м2/ч;
— скорость нагрева, К/с; S — толщина пластины, м; а —■ коэффициент температуропроводности, м2/ч; 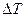 — перепад между температурой поверхности и центра в нагреваемом материале, К.
— перепад между температурой поверхности и центра в нагреваемом материале, К.
Если в формуле (88) σ принять за допускаемое напряжение σ 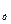 , то для определения допустимой скорости нагрева стали получаем выражение
, то для определения допустимой скорости нагрева стали получаем выражение
Cн= 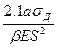 (89)
(89)
Из формулы (88) вытекает, что допустимая разность температур
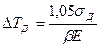 (90)
(90)
Для того чтобы уменьшить перепад температур по толщине металла и прогреть его более равномерно, осуществляют выдержку (томление), при которой температура поверхности металла не повышается, а тепло, поступающее на его поверхность, проникает внутрь и способствует повышению температуры его центра.
Основные положения рациональной технологии нагрева стали.
На практике часто пользуются значениями температуры и времени (продолжительности) нагрева, а не скорости нагрева, поскольку при помощи этих параметров удобнее наблюдать и контролировать режим нагрева металла. Выбрать (разработать) рациональную технологию нагрева стали — это значит обеспечить нагрев металла в оптимальных условиях с точки зрения интенсивности и качества нагрева.
Условия, в которых происходит нагрев металла, можно разделить на две группы:
1. Условия, определяющие внешний теплообмен, т. е. теплоотдачу от печных газов и обмуровки к поверхности металла. К ним относят: температуру печи, металла в начале и конце периода нагрева, излучательную способность печных газов и обмуровки, размеры рабочего пространства, печи.
2. Условия, определяющие внутренний (в металле) теплообмен, т. е. характеризующие передачу тепла теплопроводностью от поверхности металла внутрь него. К ним относят: теплопроводность и теплоемкость металла, его толщину и химический состав.
Количественное влияние перечисленных факторов на время нагрева рассматривается в гл. II. Здесь рассмотрим два дополнительных фактора внешнего теплообмена, заметно влияющих на нагрев металла: расположение заготовок в печи и изменение степени черноты металла в процессе его нагрева.
От расположения заготовок на поду печи в процессе их нагрева зависит, какая часть поверхности каждой заготовки способна воспринимать тепло. Возможны такие случаи, когда заготовки в той или иной мере экранируют одна другую и тем самым уменьшают общую тепловоспринимающую поверхность металла, что приводит к увеличению времени нагрева металла.
В прокатных печах с толкателями (методические печи) заготовки лежат, тесно соприкасаясь одна с другой, и могут обогреваться с одной или двух сторон, что приводит к увеличению времени нагрева.
В кузнечных печах камерного типа заготовки должны быть расположены на некотором расстоянии одна от другой, поскольку это благоприятно влияет на их нагрев.
Время нагрева заготовок при отношении их длины к толщине более трех не зависит от длины заготовок. При длине заготовки меньше трех диаметров (размеров ширины) следует учитывать нагрев с торцов заготовки. Если принять за единицу время нагрева заготовки, у которой длина равна трехкратной толщине, то при отношении длины заготовки к толщине, равном 2, коэффициент сокращения времени нагрева составит 0,8, а при отношении, равном 1, он будет равен 0,71.
Степень черноты поверхности металла в расчетах времени нагрева обычно принимают постоянной. В действительности степень черноты в процессе нагрева металла в пламенных печах претерпевает изменения, связанные с образованием окалины.
Проведенные исследования показали, что при нагреве стали в интервале температур 573—723 К происходит быстрое увеличение степени черноты на 80—90 % независимо от качества обработки поверхности перед нагревом. Это изменение степени черноты заметно влияет на время нагрева металла, вызывая ускорение нагрева образцов с черной окисленной поверхностью.
Таким образом, комбинируя условия внешнего и внутреннего теплообмена, можно разработать оптимальные условия нагрева, т. е. можно выбрать рациональную технологию нагрева металла.
В практических условиях встречается одно-, двусторонний, а иногда и многосторонний (в нагревательных колодцах) нагрев металла.
При дву- или многостороннем нагреве процесс ускоряется и его можно вести с меньшим перепадом температур по сечению металла, в результате чего обеспечивается большая равномерность нагрева.
Равномерность — весьма важный показатель нагрева металла. Равномерно нагретый металл имеет одинаковые пластические свойства и равномерно деформируется при обработке давлением.
В некоторых случаях применяют режимы нагрева в несколько ступеней.
Одноступенчатый нагрев применяют тогда, когда в печи поддерживают одинаковую температуру по всему ее объему и металл помещается сразу в среду с весьма высокой температурой. Такой метод нагрева применим для тонкого металла (листа, сутунок и т. п.), в котором не могут возникнуть значительный перепад температур и высокие температурные напряжения.
Часто такой режим применяют для нагрева металла при горячей посадке, т. е. такого металла, который при посадке в печь имеет достаточно высокую температуру.
При таком режиме нагрева в случае термической обработки металла иногда делают выдержку для полного завершения внутренних превращений в этом металле.
Двухступенчатый нагрев обычно складывается из периодов предварительного и интенсивного нагревов. Этот режим применяют для изделий из углеродистой и легированной стали значительной толщины.
Зона предварительного нагрева печи характеризуется относительно низкой температурой, что позволяет осуществлять нагрев в интервале 273—773 К с допустимой скоростью, без возникновения чрезмерных температурных напряжений.
В зоне интенсивного нагрева металл догревается до конечной температуры обязательно при достаточной равномерности нагрева (не более 200 К на 1 м толщины). Если при двухступенчатом режиме достаточная равномерность нагрева не обеспечивается, то необходимо добавить третью-ступень нагрева.
В трехступенчатый режим нагрева, кроме рассмотренных выше двух степеней, входит еще и третья ступень — период выдержки при нагреве крупных заготовок. Назначение этого периода заключается в том, чтобы, не увеличивая температуры поверхности металла, прогреть его по толщине, т. е. уменьшить температурный перепад, возникший в зоне интенсивного нагрева.
Невыполнение необходимых технологических требований нагрева может привести к неблагоприятным последствиям. Это в первую очередь относится к правильному выбору температуры нагрева. Чрезмерное повышение температуры нагрева металла ведет к излишнему росту зерна, увеличивает угар и может вызвать также перегрев или пережог металла.
Перегрев металла наступает при таком значительном укрупнении зерен, когда связь между ними ослабевает, механическая прочность металла падает и становится возможным образование в нем трещин. Перегретый металл можно исправить нормальным отжигом до температуры, несколько превышающей температуру Ас3. Пережог исправить нельзя, и такой металл отправляют в переплавку. При пережоге кислород проникает внутрь металла и как следствие этого происходит окисление и оплавление его зерен. В результате пережога настолько падает прочность металла, что он совершенно не выдерживает механической обработки. Практикой установлено, что температура нагрева при обработке давлением должна быть на 100—150 К ниже температуры, отвечающей кривой солидуса диаграммы Fе—С.
3.2 Расчет нагрева металла
Характеристика методов расчета нагрева
Теоретической базой разработки методов расчета нагрева металла являются решения основных уравнений теплопроводности при различных краевых условиях. Наиболее широкую практическую реализацию имеют краевые условия III рода. Большую роль в расчетах времени нагрева металла играет критерий Вi. Напомним, что физический смысл и роль критерия Вi становятся ясными, если его значение записать в таком виде:
Вi = 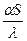 =
= 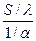 . (91)
. (91)
Числитель этого выражения S/λ представляет собой тепловое сопротивление нагреваемого тела (поскольку S— толщина тела, а λ — его теплопроводность), а знаменатель 1/α—также тепловое сопротивление, возникающее при переходе тепла от нагревающей среды к нагреваемому телу. Коэффициент теплоотдачи α, входящий в критерий Вi, характеризует интенсивность передачи тепла от печного пространства к поверхности нагреваемого металла. При нагреве по толщине металла возникает перепад температур, величина которого тем больше, чем быстрее греется металл. При одних и тех же условиях нагрева перепад температур тем больше, чем толще нагреваемая заготовка. Вместе с тем иногда и массивная заготовка (значительной толщины) может нагреваться как тонкое тело, без возникновения существенного перепада температур. Это происходит в тех случаях, когда заготовка греется медленно, т. е. к поверхности заготовки поступает такое количество тепла, которое может быть передано от поверхности заготовки внутрь ее без существенного повышения температуры поверхности.
Таким образом, разделение тел в соответствии с их поведением при нагреве следует вести не только по их геометрической толщине, но и по тепловой «массивности», которая зависит как от условий нагрева, так и от геометрических размеров. Тепловая массивность должна определяться соотношением внешнего (по отношению к поверхности металла) теплового сопротивления 1/α и внутреннего теплового сопротивления металла S/λ., которые и объединены в критерий Вi. В соответствии с этимисоображениями к тонким телам относят такие, для которых Вi<0.25. При Вi >0,5 тела ведут себя как массивные. В пределах значений Bi от 0,25 до 0,50 находится переходная область; при таких значениях целесообразнее вести расчет тела как массивного.
Нагрев тел при краевых условиях третьего рода
Тонкие тела. Обычно в печах передача тепла к поверхности нагреваемого изделия осуществляется конвекцией и излучением.
Если преобладает конвективный переход тепла и, следовательно, справедливо уравнение Ньютона
Q = α(Тп-Тм)Fτ, (92)
то время нагрева металла определяют по уравнению
τ= 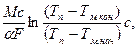 (93)
(93)
где с — теплоемкость металла, Дж/(кг-К); М — масса находящегося в печи металла, кг; F —поверхность металла, воспринимающая тепло, м2; 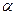 — коэффициент теплоотдачи к поверхности металла, Вт/(м2 К); Тп — температура печи, К; Tм.нач и Tм.кон — температура металла соответственно начальная и конечная, К.
— коэффициент теплоотдачи к поверхности металла, Вт/(м2 К); Тп — температура печи, К; Tм.нач и Tм.кон — температура металла соответственно начальная и конечная, К.
В тех случаях, когда преобладает передача тепла излучением и справедлив закон Стефана — Больцмана, время нагрева тонких изделий следует определять по выражению, с
τ= 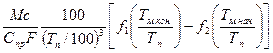 (94)
(94)
где СПР — приведенный коэффициент излучения системы печь — металл, Вт/(м2-К4).
Значение функций f1 и f2 можно выбирать из графика, приведенного на рис. 26.
Массивные тела. Как показано выше, решение дифференциального уравнения теплопроводности для этих условий обычно представляют в виде следующего критериального уравнения:
θ = f(Fо; Вi; х/s).
Решение этого уравнения для пластины (рис. 27) и цилиндра (рис. 28) было представлено Д. В. Будриным в графическом виде.
Из этих номограмм для определения времени нагрева необходимо найти критерий Fо = аτ/S2. Предварительно нужно определить температурный критерий θ и критерий Вi. При определении значения Вi, а затем и времени нагрева из критерия Fо необходимо правильно выбирать расчетную толщину нагреваемой заготовки. При двустороннем нагреве в качестве расчетной толщины надо принимать половину истинной (геометрической) толщины. При одностороннем нагреве в расчете необходимо учитывать полную толщину заготовки. Теплопроводность металла следует находить по средней его температуре за весь период нагрева. Теплоемкость металла принимают по конечной температуре нагрева металла.
Для определения значения Fо из точки на ординате (рис. 27 и 28), соответствующей найденному значению θ, проводят горизонтальную линию до пересечения с линией Вi, соответствующей найденному значению этого критерия. Из полученной таким образом точки пересечения двух линий опускают перпендикуляр и на абсциссе находят искомое значение Fо, из которого определяют время нагрева τ = Fos2/а.
Таким образом определяется время нагрева при условии, что температура в печи практически одинакова во всех точках рабочего пространства. Несколько сложнее проводится расчет времени нагрева для печей с постоянной во времени, но переменной по длине рабочего пространства температурой. К таким печам относятся методические печи.
В методической зоне этих печей температура изменяется по длине. Чтобы к расчету времени нагрева в методической зоне можно было применить описываемый метод расчета при краевых условиях III рода, всю зону необходимо разбить на некоторое число участков с усреднением температуры печи в пределах каждого из них. Усредненную температуру следует принимать постоянной в пределах каждого участка и определять соответствующее этому участку время нагрева. Очевидно, что чем больше таких участков, тем более точным (но и тем более трудоемким) будет расчет. Обычно рекомендуется разбивать методическую зону на три участка и определять время нагрева на каждом участке. Таким образом, время нагрева в методической зоне определяется как суммарное время нагрева для всех участков. Для того чтобы получить полное время нагрева металла в методической печи, надо суммировать время нагрева, полученное для методической и сварочных зон. В случае, если металл к концу зоны нагрева (сварочной зоны) прогрет по сечению недостаточно, необходимо осуществить его выдержку.
Определение выдержки металла. Выдержку (томление) металла осуществляют для выравнивания температуры по его толщине. Для этого в зоне выдержки поддерживают температуру в печи приблизительно на 50 К выше температуры поверхности металла с тем, чтобы температура поверхности заметно не повышалась, а тепловой поток, падающий на поверхность металла, проникал бы внутрь и способствовал повышению температуры центра заготовки или слитка. Выдержку можно выполнить, используя графики (рис. 29), специально построенные для определения выдержки металла, т. е. при постоянной температуре поверхности металла. Если принять, что ΔТнач --начальная разность температур поверхности и центра тела, а ΔТкон - конечная разность этих температур, то отношениеΔТкон/ ΔТкон представляет собой степень выравнивания температуры, определяющую в основном выдержку металла.
Выдержка металла может быть определена по выражению, с
τ = т 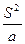 , (95)
, (95)
где S —толщина заготовки, м; а — коэффициент температуропроводности, м2/с; т — коэффициент, зависящий от степени выравнивания температур, который может быть определен по графику на рис. 40.
Во всех расчетах времени нагрева металла необходимо определять среднюю (для всего периода нагрева или для его интервала) величину коэффициента теплоотдачи излучением αизл. При краевых условиях третьего рода, т. е. при постоянстве температуры печи эта величина может быть найдена следующим образом:
αизл= 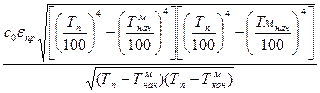 (96)
(96)
здесь Тп — температура печи, К; Тнач — температура металла в начале интервала нагрева, К; Ткон — температура металла в конце интервала нагрева, К.
Принципы скоростного нагрева
Процесс нагрева металла складывается из внешнего и внутреннего теплообмена. В зависимости от теплового сопротивления металла всегда наблюдается определенное соотношение между внешним и внутренним тепловыми потоками. Чтобы достигнуть максимально возможной скорости нагрева металла, следует как можно быстрее повысить температуру его поверхности до требуемой величины. Иначе говоря, для обеспечения скоростного нагрева надо создавать максимально возможный внешний тепловой поток. Однако это не всегда допустимо.
При нагреве тонких тел (Вi<0.25) внутренний тепловой поток практически не ограничен и процесс нагрева определяется исключительно внешним тепловым потоком. В этом случае металл воспринимает практически любое количество тепла, поданное на его поверхность.
При нагреве массивных изделий важное значение имеет процесс распространения тепла по толщине материала. Быстрый нагрев поверхности металла до заданной температуры в массивных изделиях создает значительный перепад температур по толщине.
В некоторых случаях (при нагреве мягких сталей) этот не опасный и быстрый нагрев поверхности вызывает внутренний поток большойвысокую величины, что значительно ускоряет нагрев.
Во многих случаях быстрый нагрев поверхности металла до заданной температуры во избежание недопустимых напряжений оказывается возможным только после достижения массой металла 773—823 К.
Таким образом, при нагреве тонкого и массивного металла можно применять скоростной нагрев, для чего необходимо обеспечивать большой внешний тепловой поток.
В большинстве практических случаев скорость нагрева металла зависит от внешнего теплового потока, который часто бывает сравнительно малым. В ряде случаев тонкий металл нагревается так, что внешний тепловой поток оказывается меньше возможного, т.е. на поверхность металла поступает тепла меньше, чем он может принять.
Для обеспечения скоростного нагрева в печи необходимо создавать весьма температуру, и обеспечит интенсивное движение раскалённых газов.
Для обеспечения скоростного нагрева можно использовать два метода создания значительного теплового потока на поверхность металла.
При первом методе эффект достигается за счёт увеличения до максимально возможных пределов лучистой составляющей теплообмена, для чего в печи создаётся весьма высокая температура. Печи, построенные по такому принципу, имеют ряд недостатков, главные из которых яв – ся тяжёлые температурные условия, в которых работает кладка печи.
При втором методе, получившем название ударного нагрева, большой внешний тепловой поток обеспечивается за счёт конвективной составляющей. Высокие значения αконв (350 – 400 Вт/м2 К) обеспечиваются при этом большими скоростями продуктов сгорания, которые направляются непосредственно на поверхность металла, разрушаютпограничный слой и вызывают интенсивную теплоотдачу. Такой метод требует особых, весьма сложных по конструкции горелок.
Раздел 4.Топливо и расчёты горения топлива.
4.1.Общая характеристика топлива. Понятие об условном топливе. Виды топлива.
Классификация топлива. В основном топливо классифицируют по его происхождению и агрегатному состоянию (табл. 1). В соответствии с этим топливо всех видов подразделяют на естественное и искусственное, каждое из которых в свою очередь подразделяют на твердое, жидкое, газообразное.
Химический состав топлива. Большинство видов топлива органического происхождения, поэтому основными его составляющими являются углерод и водород, которые находятся в топливе в виде различных соединений. В состав топлива обычно входят кислород, азот и сера. Все эти элементы образуют различные соединения, составляющие
Таблица 1. Общая классификация топлива
| Агрегатное состояние топлива | Вид топлива по происхождению | |
| естественному | искусственному | |
| Твердое Жидкое Газообразное | Дрова, торф, бурый уголь, каменный уголь, антрациты, горючие сланцы. Нефть. Природный газ. | Древесный уголь, кокс угольная пыль, термоан-трацит, полукокс Бензин, керосин, мазут спирт, каменноугольная смола и др. Коксовый, доменный, све тильный, генераторный, во -дяной газы |
основу топлива. Кроме того, в топливе всегда присутствуют вода и зола.
Зола — это негорючая минеральная часть твердого и жидкого топлива, состоящая из А1203, SiO2, СаО, Fе203 и др.
Содержащаяся в топливе сера может встречаться в виде органической серы (Sо), колчеданной (SК) и сульфатной (SС). Общее количество серы Sоб = Sо + Sк + Sс.
Органическая и колчеданная сера участвует в процессах горения топлива, а сульфатная сера в горении не принимает участия.
Влага, которая содержится в топливе, подразделяется на гигроскопическую (химически связанную) и внешнюю, которая механически удерживается в топливе и теряется при сушке.
Чтобы установить состав топлива, проводят технический и химический (элементарный) анализ топлива. При техническом анализе определяют влагу, летучие и золу. Химический анализ топлива можно выполнить по элементарному составу (С, Н, О, N. S) и определением содержания в топливе отдельных химических соединений (СО, С02, СН4 и др.). Первый метод анализа применяют для твердого и жидкого топлива, второй — для газообразного топлива.
Элементарный анализ проводят с целью определения содержания углерода, водорода, кислорода, азота и серы в процентах по массе. Однако подобный метод анализа не дает возможности судить о том, из каких соединений этих элементов состоит топливо, а следовательно, и о многих свойствах топлива. Элементарный анализ дает представление о топливе как о механической смеси отдельных элементов, что достаточно для проведения необходимых расчетов сжигания топлива. В соответствии с элементарным анализом в топливе различают органическую (С, Н, О, N), горючую (С, Н, О, N. S) и сухую (С, Н, О, N, А) массы и рабочее топливо (С. Н, О, N. А, W).
Органическая масса топлива дает возможность судить о его природе, а горючая масса — о топливе как о горючем.
При записи результатов анализа пользуются индексами, например: С0 обозначает содержание углерода в органической массе; Sг — содержание серы в горючей массе; Ас — содержание золы в сухой массе и Wр — содержание влаги в рабочем топливе. Естественно, что состав рабочего топлива записывают так:
СР + НР + ОР + Np +Sр + АР + WР = 100%.
Пересчет состава угля из одной массы в другую легко выполнить по следующим выражениям (%):
x0=xг 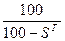 ; xг=xс
; xг=xс 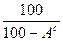 ; x0=xс
; x0=xс 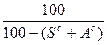 ; xс=xр
; xс=xр 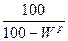 ;
;
x0=xр 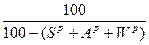 ; (97)
; (97)
где хс — содержание какого-либо элемента в сухой массе, %; хр — содержание какого-либо элемента в рабочем топливе, %; хГ — то же, в горючей массе, %; х° — то же, в органической массе, %.
Химический анализ газообразного топлива можно выполнить последовательным поглощением отдельных составляющих различными реактивами. Его результаты, выраженные в объемных процентах, показывают содержание составных частей газообразной смеси С02, СО, СН4, 02, СmНm Количество N2 определяют по разности.
Подобный анализ по химическим соединениям, составляющим топливо, позволяет судить о его свойствах. Анализ с последовательным поглощением отдельных составляющих характеризует состав сухого топлива, поскольку влага, содержащаяся в газе, в процессе анализа не учитывается. Вместе с тем в газах в большинстве случаев содержится влага, которую обычно определяют как массу воды в единице объема сухого газа W (г/м3). В связи с этим бывает необходимо пересчитывать состав сухого газа с тем, чтобы учесть влагу, т. е. определять состав влажного газа.
Теплота сгорания топлива. При сжигании топлива выделяется тепловая энергия. Количество выделившегося тепла связано с химическим составом топлива.
Количество тепла, которое выделяется при сжигании единицы топлива, называется теплотой сгорания топлива [кДж/кг; кДж/м3 или кДж/кмоль]. В технике различают высшую и низшую теплоты сгорания топлива.
Высшая теплота сгорания Q 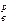 соответствует условию, что все водяные пары, образовавшиеся при горении, доводятся до жидкого состояния при 273 К. При этом возвращается следующее количество тепла:
соответствует условию, что все водяные пары, образовавшиеся при горении, доводятся до жидкого состояния при 273 К. При этом возвращается следующее количество тепла:
Скрытая теплота испарения 1 кг Н20, кДж..... 2256,8
Теплота нагрева 1 кг Н2 0 от 273 до 373 К, кДж... 418,7
Итого.................. 2675,5
Низшая теплота сгорания Q 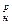 соответствует условию, что содержащийся в продуктах сгорания водяной пар охлажден с 373 до 293 К. При этом высвобождается количество тепла, равное 1,0*2,041 (373 — 293)≈ 163,3 кДж/кг,
соответствует условию, что содержащийся в продуктах сгорания водяной пар охлажден с 373 до 293 К. При этом высвобождается количество тепла, равное 1,0*2,041 (373 — 293)≈ 163,3 кДж/кг,
где 2,041 кДж/кг К) —теплоемкость паров воды.
Низшая теплота сгорания топлива больше соответствует действительности, так как практически при сжигании топлива пары воды в газообразном состоянии уносятся с продуктами сгорания.
Количественная разница между Q 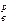 и Q
и Q 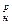 на 1 кг Н20 составляет
на 1 кг Н20 составляет
Q 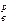 - Q
- Q 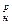 = 2675,5 — 163,30 ≈2512,2 кДж/кг. (98)
= 2675,5 — 163,30 ≈2512,2 кДж/кг. (98)
Поскольку в продуктах сгорания содержится влага топлива W1 и вода, полученная от сгорания водорода [ W2 = H2 O/Н2= (18/2)H = 9Н], разность между высшей и низшей теплотами сгорания на 1 кг топлива составляет
Q 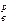 - Q
- Q 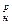 = 2516,39 (W1 + W2) = 2512,2(W1+9Н) кДж/кг (99)
= 2516,39 (W1 + W2) = 2512,2(W1+9Н) кДж/кг (99)
или если W1 и Н выражены в процентах (т.е. Wр и Нр), то
Q 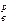 - Q
- Q 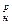 = 25,122(Wр+9Нр) кДж/кг. (100)
= 25,122(Wр+9Нр) кДж/кг. (100)
При использовании топлива для практических целей совершенно необходимо определять его теплоту сгорания. Теплоту сгорания топлива можно измерять сжиганием навески или определенного объема топлива в специальных приборах — калориметрах. В инженерной практике теплоту сгорания топлива часто определяют расчетом на основании данных элементарного анализа с использованием тепловых эффектов реакций горения отдельных составляющих топлива.
Теплоту сгорания твердого и жидкого топлива на основании элементарного анализа обычно определяют по формулам, полученным эмпирически. Для отечественных видов твердого и жидкого топлива достаточно точные результаты дает формула Д. И. Менделеева:
Q 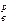 = 4, 187[81СР + 300НР — 26 (Oр — Sр)] кДж/кг. (101)
= 4, 187[81СР + 300НР — 26 (Oр — Sр)] кДж/кг. (101)
При определении низшей теплоты сгорания формула Д. И. Менделеева имеет вид
Q 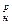 = 4,187 [81СР + 300НР — 26 (Ор — Sр) -6 (WР + 9Нр) ] кДж/кг.
= 4,187 [81СР + 300НР — 26 (Ор — Sр) -6 (WР + 9Нр) ] кДж/кг.
(102)
Теплота сгорания газообразного топлива может быть с достаточной точностью получена расчетом, поскольку могут быть известны соединения, составляющие горючую массу топлива, и теплоты сгорания этих соединений. В табл. 2 приведены тепловые эффекты реакций окисления ряда соединений, входящих в состав топлива.
Следовательно, если известен состав газообразного топлива, то не представляет труда подсчитать его теплоту сгорания.
Условное топливо. Чтобы сравнить топливо различных видов, иногда используется понятие условного топлива, характеризуемого тепло-
Таблица 2. Тепловые эффекты реакций окисления
| Тепловой эффект реакции | |||
| Реакция | |||
| к Д ж/моль | кДж/кг | кДж/м3 | |
| с+о2=со2 | +408860 | + 34070 | |
| СО+0,5О2=СО2 | +285640 | — | + 12645 |
| СО+(Н20)п=С02+Н2 | + 433590 | — | — |
| С+(Н20)п=СО+Н2 | +118897 | —9902 | — |
| Н2+0,5О2=(Н2О)ж | +286223 | + 143112 | + 12770 |
| Н2+0,5О2=(Н2О)п | +241800 | + 121025 | + 10760 |
| СН4+202=С02+(2Н20)П | +805560 | — | +35800 |
| С2Н4+302=2С02+(2Н20)П | + 1341514 | — | + 59037 |
| Н2S+1,502=(Н20)п+S02 | + 519188 | — | — |
той сгорания 29300 кДж/кг. Для перевода любого топлива в условное следует разделить его теплоту сгорания на 29310 кДж/кг, т.е. найти эквивалент данного топлива.
В настоящее время в металлургической промышленности наиболее распространенным является газообразное топливо. Достаточно часто употребляется жидкое топливо. Практически единственным видом твердого топлива, которое употребляется в металлургии, является кокс.
Газообразное топливо по сравнению с жидким и твердым имеет ряд преимуществ, главные из которых: более простое смешение горючего и воздуха, позволяющее проводить сжигание газа с меньшим избытком воздуха; легкость транспортировки; простота обслуживания печей, работающих на газе. Все это приводит к тому, что газообразное топливо становится преобладающим. Газообразное топливо бывает естественное и искусственное. Естественными видами газообразного топлива являются природный газ и попутный газ, который улавливают при добыче нефти. Искусственными видами газообразного топлива являются коксовый и доменный газы, получаемые соответственно при коксовании угля и при доменной плавке. Кроме того, к искусственным относятся генераторные газы, которые в последние годы полностью вышли из употребления на предприятиях черной металлургии.
Природный газ. Природный газ — наиболее дешевое топливо. Себестоимость его значительно ниже себестоимости угля и нефти.
Природный газ основных месторождений России (СССР) состоит главным образом из метана и содержит небольшой процент его гомологов. Содержание в нем балласта (N2 и СО2) невелико. Важно отметить, что природный газ большинства месторождений не содержит сероводорода и других сернистых соединений (табл. 3).
В связи с ростом добычи и переработки нефти соответственно возрастают ресурсы нефтепромысловых газов, добываемых попутно с нефтью. Нефтепромысловые газы отличаются от природных чисто газовых месторождений большим содержанием гомологов метана (этана, бутана и др.) и соответственно более высокой теплотой сгорания.
Таблица 3. Примерный состав сухих природных газов некоторых месторождений России
| Состав, % (объемы.) | ||||||||
| Месторождение | метан | этан | пропан | бутан | тяжелые углеводороды | CO2 | N2 | Q 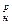 , кДж/м3 , кДж/м3 |
| Елшанское (Саратовская область) Северное поле Дашава (Западная Украина). Шебелинское.. Газлинское... | 93,2 97,7 97,8 93,5 94,6 | 0,7 0,5 4,0 2,3 | 0,6 0,2 1,0 0,5 | 0,6 0,1 0,5 0,3 | 0,5 0,05 0,5 | 0,7 0,05 0,1 0,1 | 4,4 1,6 1,3 0,4 0,2 | 36034 38354 |
Искусственное газообразное топливо. Коксовый газ, получаемый при коксовании углей, играет очень важную роль в топливном балансе металлургических заводов. В табл. 4 приведен состав коксового газа.
Колебания в содержании отдельных компонентов объясняются различием в составе коксуемых углей, температурах и режимах коксования.
Доменный (колошниковый) газ получают в больших количествах (около 3 м3 на 1 кг чугуна) в процессе доменной плавки. На металлургических заводах доменный газ играет существенную роль в тепловом балансе, на его образование расходуется свыше 40 % теплоты сгорания кокса, загруженного в доменную печь. Доменные воздухонагреватели, печи коксовых и прокатных цехов в большей или меньшей мере отапливают доменным газом в смеси с коксовым или природным газом. Средний состав доменного газа (Q 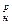 = 3500÷3800 кДж/м3): 9—.
= 3500÷3800 кДж/м3): 9—.
14% С02, 25—31 % СО, 0,3—0,5% СН4, 2—3% Н2, 57—58% N2.
Генераторные газы представляют собой продукты безостаточной газификации твердого горючего. Газификация может быть проведена при помощи кислорода, вводимого с воздухом, или водяного пара. Аппараты, в которых твердое топливо превращается в газообразное, называют газогенераторами, процесс газификации — газогенераторным.
На рис. 30 изображена схема газогенератора, который представляет собой шахту— железный кожух, изнутри футерованный огнеупорным кирпичом. Топливо загружают в газогенератор сверху через загрузочное устройство. Дутье (воздух, водяной пар) поступает снизу под колосниковую решетку). Образующиеся золу и шлак удаляют снизу. Полученный генераторный газ отводят из верхней части генератора над слоем топлива.
Воздух попадает в слой раскаленного кокса и вступает в реакцию с углеродом:
с + о2 = со2.
Двуокись углерода и образующийся в результате испарения влаги топлива пар, захватываемые газовым потоком, восстанавливаются углеродом раскаленного кокса в окись углерода и водород:
С02 + С = 2СО и Н20 + С = СО + Н2.
Высокие температуры в зоне реакций воздушного газогенератора обусловливают ряд трудностей при проведении процесса.
Понижение температуры в зоне реакций, следовательно, и понижение температурного уровня процесса во всем газогенераторе могут быть достигнуты совмещением воздушной и водяной газификации. В этом случае параллельно с экзотермическим процессом образования воздушного газа развивается эндотермический процесс газификации водяным паром. Регулирование развития того и другого процесса, достигаемое изменением соотношения воздуха и пара в смеси, поступающей в слой, позволяет непрерывно поддерживать температуру комплексного процесса на желательном уровне. Такая схема работы приводит к образованию смешанного газа. Этот вид газификации топлива наиболее распространен в промышленности, так как по схеме работы
и конструкции устройства он близок к воздушной газификации, а по качеству получаемого газа ее превосходит.
Состав смешанных генераторных газов приведен в табл. 5.
Таблица 5. Состав смешанных генераторных газов, °/о (объемн.)
| Топливо | о | (Л X | е X е и | о и | К | о" + г" | <3Р, чн' кДж/м'" | Выход сухого газа, м3/кг | |
| Коксовая мелочь.... | 5,0 | 0,3 | 0,0 | 28,5 | 13,0 | 0,7 | 52,4+0,2 | 3,2 | |
| Донецкий газовый уголь | 5,0 | 0,3 | 0,3 | 26,5 | 13,5 | 2,3 | 51,9+0,2 | 3,3 | |
| Подмосковный уголь.... | 6,5 | 1,2 | 0,4 | 25,0 | 14,0 | 2,2 | 50,5+0,2 | 1,4 |
Жидкое топливо
Естественное жидкое топливо. К естественным жидким топливам относят сырую нефть, которую как топливо используют очень ограниченно. Использование продуктов переработки нефти дает более высокий эффект, чем использование нефти в сыром виде.
Искусственное жидкое топливо. Основную массу искусственного жидкого топлива составляют продукты переработки сырой нефти.
Бензин представляет собой жидкое топливо, состоящее из наиболее легкокипящих фракций нефти (температура кипения до 473 К). Элементарный состав бензина зависит от содержания в нем различных углеводородов. Можно считать, что бензин в среднем состоит из 85 % С и 15 % Н. Низшая теплота сгорания составляет около 41900 кДж/кг. Бензин служит топливом для авиационных и автомобильных двигателей.
Несколько более высокую температуру кипения (473—493 К) имеет лигроин, используемый в качестве топлива для тракторных двигателей.
Керосин представляет собой фракцию, в основном кипящую при температуре выше 523 К. При дальнейшем повышении температуры из него отгоняется соляровый дистиллят.
В зависимости от типа нефти выход легких фракций при перегонке составляет 25—30%. Остальная часть — это более тяжелые фракции (мазут). Мазут широко применяют для отопления металлургических печей.
Мазут различного происхождения по элементарному анализу мало отличается один от другого: 86,3—87,1 % СГ, 12,3—13,1 % Нг, 0— 0,35 % Ог, 0,05 % Nг и 0—10 % Wр.
Содержание серы в мазуте, получаемом при переработке малосернистой нефти, составляет около 0,5 %: в мазуте, получаемом из высокосернистой нефти, содержание серы может быть около 4 %. Выпускают топочные мазуты марок 40, 100, 200 и МП (мазут для мартеновских печей). Для этих мазутов температура вспышки составляет 363—383 К, а температура застывания 283—298 К.
Важными показателями, характеризующими качество мазута, являются температура застывания и вязкость. Вязкость в значительной степени снижается при повышении температуры нефтепродукта. Поэтому для обеспечения возможности перекачивания и сжигания в форсунках вязкие мазуты приходится предварительно подогревать до 343—353 К.
Низшая теплота сгорания мазута в зависимости от его состава и содержания влаги колеблется в пределах 35615—39805 кДж/кг.
Большое значение жидкого топлива заставляет изыскивать пути для замены нефти другими видами горючих ископаемых, которые можно использовать для получения моторных топлив. Существует ряд методов переработки твердого топлива: гидрогенизация, синтез углеводородов и др.
В практике металлургического производства в качестве заменителя мазута в виде добавки к газообразному топливу (для увеличения излучательной способности факела) нередко применяют смолы, получаемые как продукт переработки твердых топлив.
Твердое топливо
Для естественного твердого топлива всех видов общим является не только одинаковое агрегатное состояние, но и общность условий происхождения. Твердое топливо естественного типа — растительного происхождения. Чем старше топливо, тем выше содержание углерода (табл. 6) и теплота сгорания.
Твердое топливо, кроме данных элементарного анализа, характеризуется также данными технического анализа, при котором определя-
Таблица 6. Характеристика твердого топлива основных видов
| Состав органической массы:. % | ||||
| Вид топлива | С | н | Теплота сгорания органической массы, кДж/кг | |
| Древесина.... Торф...... Бурые угли... Каменные угли.. | 55-60 67—78 80—96 | 5,5-6 2—15 | 35—39 17—28 2—15 | 18 840 20 935—23 800 27 200—30 900 31 800—36 400 |
ют: содержание влаги, выход летучих веществ и кокса, зольность, количество серы, теплоту сгорания топлива.
Влажность является весьма важной характеристикой твердого топлива и в большой мере определяет эффективность его использования. Летучие вещества выделяются из топлива при его термическом разложении без доступа воздуха. При этом происходит разложение неустойчивых молекул и выделение газообразных горючих веществ. Кроме летучих веществ, продуктом термического разложения являются также кокс — твердый остаток продуктов разложения. Летучие вещества играют весьма важную роль в процессе сгорания твердого топлива, ибо воспламеняются первыми и способствуют развитию процесса горения.
Твердое топливо содержит в составе негорючие элементы, составляющие основу золы. Чем выше количество этих негорючих элементов и выше зольность, тем ниже качество топлива.
Сера является крайне вредной примесью твердого топлива. При сжигании топлива, в состав которого входит сера, образуется оксид серы S02; он является очень сильным окислителем. При применении твердого топлива (кокса) в доменном производстве сера, содержащаяся в топливе, в значительной части переходит в чугун, понижая его качество и усложняя операции по его дальнейшему переделу в сталь. Твердое топливо в металлургических печах практически не применяют. Исключение составляет кокс, необходимый для доменного процесса. Кокс получают в специальных печах — коксовых батареях из каменных углей, обладающих необходимыми свойствами (коксующиеся угли). Исходным материалом для производства кокса в коксовых батареях служат угли, дающие спекшийся кокс.
Процесс коксования состоит в следующем. Измельченную до кусков размером меньше 3 мм и увлажненную угольную шихту загружают через загрузочные люки в камеры коксовых печей, температура в которых поддерживается в пределах 1083—1273 К. В первый момент в камерах происходит испарение влаги. Затем наступает первая стадия пирогенетических процессов (процессов разложения без доступа воздуха), которая начинается с момента нагревания угля до 473 К. На этой стадии выделяются пары первичной смолы, состоящей главным образом из углеводородов жирного ряда. Эти соединения, проходя через раскаленную твердую массу топлива, превращаются в газы и ароматические углеводороды бензольного ряда.
Летучие продукты коксования направляют на химический завод для улавливания из них ценных продуктов. Газ, выходящий из коксовой камеры печи, называется прямым, а газ, из которого на химическом заводе выделили пары смолы, сырого бензола и аммиака, — обратным.
Каменноугольную смолу подвергают разгонке. В получаемых маслах и сыром бензоле содержатся ценные вещества, служащие сырьем для химической промышленности, например бензол, толуол, фенол, ксилолы, нафталин и другие соединения, из которых вырабатывают различные химические продукты.
Количество смолы, получаемой при коксовании, зависит от выхода летучих и составляет 2—3 °/о массы угля. Остающийся после перегонки смолы пек используют при производстве брикетов, толя, пластмасс и др.
При оценке кокса как топлива для доменных печей наибольшее значение имеют данные его технического состава и результаты исследования механической прочности. На основе технического анализа определяют содержание в коксе влаги, золы, серы и летучих. Количество влаги в коксе зависит главным образом от способа тушения кокса при выдаче из печи. Нормально в коксе содержится 2—5 % влаги. Большое значение имеет зольность кокса, так как минеральная масса в коксе понижает его теплоту сгорания и вызывает повышенный расход флюсов в доменной шихте. Производительность доменных печей при работе на коксе с большим содержанием минеральной массы понижается, а расход топлива возрастает. Среднее содержание золы в донецком коксе составляет 9—10 %, в коксе из восточных углей 10— 11 %■
Содержание серы в коксе всегда отрицательно влияет на его свойства. Предотвращение перехода больших количеств серы в металл связано с необходимостью увеличения количеств шлака и его основности, что неизбежно влечет за собой увеличение расхода горючею. В процессе коксования 80—85 % серы сырого угля удерживается в коксе.
Значительной сернистостью характеризуются коксы из донецких углей (1,5—2,0%), малой — из кузнецких (0,5—0,7%)- Выход летучих из нормально выжженного кокса не превышает 1,4—1,8%. По этой величине судят о завершении процесса коксования.
По назначению кокс подразделяют на доменный (пористость 45— 55%) и литейный для вагранок (пористость не более 45%). Большое значение для доменного производства имеет механическая прочность кокса, подвергающегося в доменной печи ударам при падении и истиранию. Обладая высокой твердостью, кокс вместе с тем весьма хрупок. Вторым по количественному выходу продуктом коксования является газ, вызываемым коксовым. Средний состав обратного коксового газа следующий: 57—60 % Н2, 24—26 % СН4, 6,0—6,8 % СО, 2 2— 2,5% СмНn, 2-2,3% С02 + Н2S, 0,2-0,4% 02, 3,0-4,0% N2. В 1 м3 прямого газа, кроме перечисленных составляющих, содержится 100 — 125 г смолы, 25—40 г бензольных углеводородов, 5—15 г водорода и 5—10 г аммиака, в большей или меньшей мере улавливаемых при обработке газа на химическом заводе.
Как видно из приведенного состава, обратный газ — высокоценное горючее, его теплота сгорания составляет 16000—18000 кДж/м3. Основными его потребителями являются металлургические заводы.
Для получения кокса применяют специальные печи, одна из которых показана на рис. 31. Прямоугольные камеры для коксования длиной около 13, высотой 4,2—4,5 и шириной около 0.4 м собраны в батареи. Торцовые части камер закрываются дверями 6 и 9. Угольную шихту в камеры для коксования загружают через люки 8 в сводах. Летучие продукты, образующиеся в процессе коксования, т.е. коксовый газ и пары смолы, отводят из камер через отверстие в своде 7 в стояк и газосборник. Воздух, подаваемый для сжигания газа, используемого для отопления печей, предварительно подогревают в воздушных регенераторах 5, размещенных по камерам. Воздух поступает в низ регенераторов через подовый канал 10. Нагретый в регенераторах воздух через косые ходы 3, минуя блок 4, направляется в нижнюю часть вертикальных отапливаемых каналов 2, которые расположены между камерами коксования.
При отоплении коксовых печей доменным или генераторным газом осуществляют его подогрев в газовых регенераторах. Нагретый газ смешивается в отопительных каналах 2 с воздухом, где и сжигается, нагревая при этом боковые стенки камер коксования до температуры около 1573—1673 К. В случае применения коксового газа для отопления печей его направляют в горелки через специальные каналы.
Дымовые газы отводят через перекидные каналы 1 в верхнюю
Таблица 7. Состав и пористость доменного кокса, %
| Кокс | Влага | Летучие | Зола | Сера | Фосфор | Углерод | Пористость |
| Донецкий. Кузнецкий. | 7—14 9 | 0,6—1,2 1,2—1,7 | 9—10 ~ 10 | 0,8—2,0 -~0,5 | 0,03—0,05 0,04 | 75—93 77 | 46—55 ---- |
* Нелетучий.
часть смежных нагревательных каналов, а также через специальные косые ходы в верх регенераторов, где ими нагревается насадка регенераторов. Из нижней части регенераторов дымовые газы отводят в боров и дымовую трубу.
Воздушные регенераторы разделены на две батареи. Когда в нечетных регенераторах нагревается воздух, насадка четных регенераторов нагревается дымовыми газами. Затем в результате перекидки клапанов изменяют направление потока воздуха и дымовых газов. Воздух поступает для нагрева в четные регенераторы, а дымовые газы — в нечетные.
Процесс коксования длится около 15—16 ч. Из 1 т угля получают (в зависимости от влажности угля и выхода летучих веществ) около 720—800 кг кокса, 300 м3 коксового газа, 30—40 кг смолы, 10 кг бензола и примерно 3 кг аммиака.
Расход тепла на коксование 1 т угля составляет около 2514 МДж; при этом около 40—50 % расходуемого тепла заключается в физическом тепле кокса, т. е. в том тепле, которое было израсходовано на нагрев кокса до той температуры, при которой его выгружают из печи.
В табл. 7 приведены состав и пористость кокса отечественного производства.
4.2 Расчеты горения топлива.
При горении топлива в качестве окислителя используют кислород воздуха. В результате образуются продукты сгорания и развивается определенная температура горения. Поэтому расчеты горения топлива выполняются с целью определения:
а) количества необходимого для горения воздуха;
б) количества и состава продуктов сгорания;
в) температуры горения.
Расход воздуха
Расходы воздуха можно определять как в объемных, так и в массовых единицах.
Для уяснения методики определения расхода воздуха рассмотрим полное горение метана (СН4) по реакции СН4 + 202 = С02+2Н20.
Сначала определим расход воздуха в объемных единицах. Как следует из приведенной реакции, для сжигания 1 моля СН4 требуется 2 моля 02. Поскольку 1 кмоль любого газа занимает при нормальных условиях одинаковый объем (22,4 м3), то для сжигания 22,4 м3 СН4 потребуется 2*22,4 = 44,8 м3 02. Таким образом, для сжигания 1 м3 СН4 требуется 2 м3 02, но в сухом воздухе кислород по объему составляет 21 %, остальные 79% приходятся на долю азота. Следовательно, количество азота в воздухе в 3,762 раза больше количества кислорода. Поэтому расход воздуха на сжигание 1 м3 метана составит 2+2*3,762 = 9,524 м3.
Аналогичный расчет можно провести и в массовых единицах. Подобные расчеты чаще делают для твердого или жидкого топлива. Возьмем, например, горение углерода С+02 = С02. Из этой реакции видно, что на 1 кмоль С расходуется 1 кмоль 02, но 1 кг*моль С имеет массу, равную 12 кг, а кг-моль 02 32 кг; следовательно, для сжигания 1 кг
С потребуется 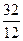 =2,67 кг кислорода. В воздухе кислород по массе составляет 23,2 %, а азот 76,8 %. Поэтому вместе с кислородом войдет азота 2,67
=2,67 кг кислорода. В воздухе кислород по массе составляет 23,2 %, а азот 76,8 %. Поэтому вместе с кислородом войдет азота 2,67 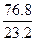 =2,67-3,31 =8,83 кг.
=2,67-3,31 =8,83 кг.
Следовательно, для сжигания 1 кг углерода потребуется воздуха 2,67+8,83=11,50 кг. Это количество можно перевести в объемное, поделив общую массу воздуха на его плотность (1,293 кг/мь), т. е. 11,50/1,293=8,89 м3.
Как при горении метана, так и при горении углерода полученные по реакциям количества кислорода и воздуха представляют собой те наименьшие количества, которые необходимы для полного окисления единицы горючего вещества. Такое наименьшее необходимое количество воздуха (кислорода) называется теоретическим количеством. На практике, однако, сжигание топлива осуществляется при расходах воздуха, несколько превышающих теоретическое количество. Величина, показывающая отношение действительного расхода воздуха (Vд) к теоретическому количеству (Vт), называется коэффициентом избытка воздуха п= Vд / Vт и играет на практике очень важную роль.
Более универсальной величиной является коэффициент расхода кислорода (п0), который показывает отношение действительного расхода кислорода (V  ) к теоретически
) к теоретически
необходимому (V 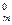 ), т.е. п0 =.V
), т.е. п0 =.V  / V
/ V 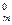
Коэффициент избытка воздуха пригоден только для полного сгорания топлива в воздухе.
При неполном же сгорании, когда подаваемое количество кислорода меньше теоретического, применим только коэффициент расхода кислорода, который становится меньше единицы. При применении обогащенного дутья, в котором количество кислорода превышает 21 %, характерным также является коэффициент расхода кислорода. В этом случае метод определения расхода дутья аналогичен выше изложенному с той лишь разницей, что изменяется соотношение между азотом и кислородом.
Всякое промышленное топливо представляет собой механическую или химическую смесь отдельных горючих элементов, поэтому общий расход воздуха (кислорода) определяется суммированием аналогичного расхода для отдельных элементов.
Состав и количество продуктов сгорания
Состав и количество продуктов сгорания определяют по методу, применяемому для определения расхода воздуха. Рассмотрим снова пример полного горения метана при коэффициенте избытка, равном единице. В результате горения образуются С02 и Н20. Кроме того, в продуктах сгорания будет присутствовать N2, внесенный с воздухом. Определим последовательно количество каждой составляющей продуктов сгорания. При сжигании 1 м3 метана образуется С02 1м3 и Н:20 2 м3. Кроме того, с воздухом вносится 2-3,762 = 7,524 м3 N2. Таким образом, полное количество продуктов сгорания составит 1 м3+2 м3+7,524 м3 = = 10,524 м3.
Состав продуктов сгорания следующий:
С02= 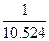 .100% =9,5%;
.100% =9,5%;
H 2 O= 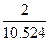 100% = 19,0%;
100% = 19,0%;
N2= 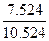 100%=71,5%-
100%=71,5%-
Если бы СН4 сжигали с коэффициентом избытка воздуха, превышающим единицу, то общее количество продуктов сгорания возр
 2015-08-21
2015-08-21 11245
11245








