Кислоты -сложные вещества, состоящие из одного или нескольких атомов водорода, способных
заместиться на атом металла, и кислотного остатка.Число атомов кислорода определяет основность кислот.
| Бескислородные
| Кислородсодержащие
|
| HCl, HBr, HI, H2S анион "-ид" HCl-хлороводородная(соляная кислота), Cl--хлорид H2S-сероводородная, S2-
| H2SO4, HNO3, H2CO3, H3PO4 и другие.
|
ПОЛУЧЕНИЕ.
| Кислородсодержащие
| 1.Кислотный оксид+вода
| SO3+H2O=H2SO4 P2O5+3H2O=2H3PO4
|
| 2.Металл+сильный окислитель
| P+5HNO3+2H2O=3H3PO4+5NO
|
| 3.Cоль+менее летучая кислота
| NaNO3+H2SO4=HNO3  +NaHSO4 +NaHSO4
|
| Бескислородные
| 1.Водород+неметалл
| H2+Cl2=2HCl
|
| 2.Cоль+менее летучая кислота
| NaCl+H2SO4=2HCl  +NaHSO4 +NaHSO4
|
КЛАССИФИКАЦИЯ И ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ
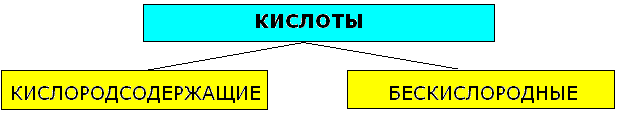
|
| 1.Изменяют окраску индикаторов
|
| лакмус-красный, метилоранж-красный (только для растворимых кислот)
|
| 2.Взаимодействие с металлами, стоящими до водорода
|
H2SO4+Ca=CaSO4+H2 
| 2HCl+Ca=CaCl2+H2 
|
| 2.Взаимодействие с основными оксидами
|
| H2SO4+CaO=CaSO4+H2O
| 2HCl+CaO=CaCl2+H2O
|
| 3.Взаимодействие с основаниями
|
| H2SO4+Ca(OH)2=CaSO4+2H2O
| 2HCl+Ca(OH)2=CaCl2+2H2O
|
| 4.Взаимодействие с амфотерными оксидами
|
| H2SO4+ZnO=ZnSO4+H2O
| 2HCl+ZnO=ZnCl2+H2O
|
| .Взаимодействие с солями, если образуется малорастворимое, летучее или малодиссоциирующее вещество
|
| H2SO4+BaCl2=BaSO4+2HCl
| 2HCl+Na2CO3=2NaCl+H2O+CO2 
|
| 6.При нагревании
|
| Слабые кислоты легко разлагаются H2SiO3=H2O+SiO2
| H2S=H2+S
|
| Физические свойства кислот
|
| Жидкости H2SO4 HClO4 и др.
| Твердые H3PO4 H2SiO3 и др.
| Газообразные HCl H2S и др.
|
 +NaHSO4
+NaHSO4
 +NaHSO4
+NaHSO4

 2015-08-21
2015-08-21 334
334







