Эти правила полезны во многих случаях. Посмотрите, например, как c их помощью легко определяется степень окисления элемента с переменной (или неизвестной) валентностью по молекулярной формуле. Допустим, имеется соединение H2SO3. Спрашивается, какова степень окисления серы? Поскольку степень окисления водорода всегда (+1), а степень окисления кислорода (–2), то нетрудно подсчитать, что положительные и отрицательные степени окисления "уравновесят" друг друга в молекуле H2SO3 тогда, когда степень окисления серы составит (+4). В этом случае алгебраическая сумма всех степеней окисления в молекуле равна нулю:
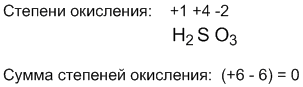
Действие этого правила можно показать и на примере реакции серы с кислородом, в которой электроны формально переходят от одного атома к другому:
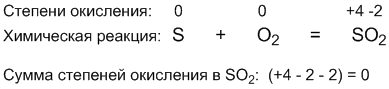
До реакции сера и кислород имели одинаковую – нулевую степень окисления. В результате реакции степень окисления серы повысилась (+4). Значит, сера окислилась.
Степень окисления кислорода понизилась (-2), то есть кислород восстановился. Алгебраическая сумма всех степеней окисления в SO2 осталась равной нулю.
Подобных реакций с изменением степеней окисления реагирующих атомов – огромное множество. Все вместе они называются окислительно-восстановительными реакциями.
В последующих главах мы рассмотрим эти реакции подробнее, а пока еще раз разберемся в новых терминах.
Просто так трудно запомнить, какой процесс – отдачи или захвата электронов – называется окислением, а какой – восстановлением. Какой атом приобретает отрицательную, а какой – положительную степень окисления.
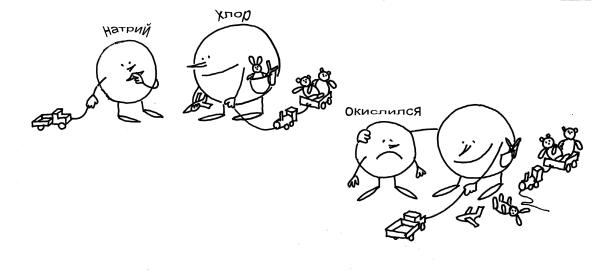
Рис. 3-11. Не совсем обычная запись уравнения химической реакции: Na + Cl = NaCl (см. текст). Хлор – "отрицательный", он отбирает чужие электроны. Натрий "окислился" – это заметно по его кислой физиономии.
Кому-то из вас поможет рис. 3-11, который рассказывает о реакции между натрием и хлором так, как будто это случилось в "химическом детском саду". В этом “детском саду” порядки такие же, как и в обычном. У Хлора целых 7 игрушек (электронов). Натрию же достался только грузовичок (1 электрон). Тут Хлор увидел у Натрия грузовичок и решил, что именно этой игрушки ему и не хватает! Хлор посильнее, поэтому грузовичок мгновенно оказался у него. А чтобы Натрий не ябедничал (у него такой окислившийся вид!), Хлор предложил поиграть вместе. Какое там! Конечно же, все 8 игрушек Хлор подтащил поближе к себе, а Натрию только и остается, что стоять рядом с “окисленным” видом.
Итак, какова мораль? Хлор, конечно, отрицательный. Он отобрал чужую игрушку-электрон. Теперь у него отрицательная степень окисления. Натрий, безусловно, окислился - вон какой у него “кислый” вид. Но и от Хлора не отходит - игрушек-то больше нет! Чем не картина образования химической связи в типичной окислительно-восстановительной реакции?
Остается только добавить, что восстанавливается в таких реакциях окислитель, а окисляется – восстановитель. В нашей истории хлор – окислитель, а натрий – восстановитель.
Точно так же реагирует с хлором-окислителем металлический калий (востановитель). У калия еще легче "отобрать" электрон, чем у натрия, поскольку его внешняя электронная оболочка находится дальше от ядра. Реакция протекает с выделением белого "дыма" - кристаллов соли KCl (посмотрите видеоопыт из "Единой коллекции цифровых образовательных ресурсов").
 2015-08-13
2015-08-13 1930
1930