Большое значение природных полимеров в качестве носите лей для иммобилизации объясняется их доступностью и наличием реакционно-способных функциональных групп (в исходном или модифицированном препарате), легко вступающих в различные химические реакции, а также высокой гидрофильностыо. К недостаткам природных носителей можно отнести неустойчивость к воздействию микроорганизмов и относительно высокую стоимость многих из них.
Полисахариды. Наиболее часто для иммобилизации используют целлюлозу, декстран, а га розу и их производные.
Целлюлоза представляет собой поли-],4-Р-£>-глюкопиранозил-£>-глкжопиранозу
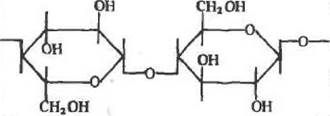
Целлюлоза отличается высокой степенью гидрофильности, а наличие большого числа гндроксильных групп дает возможность ее легко модифицировать путем введения различных заместителей. Препараты целлюлозы для придания им химической устойчивости «сшивают» эпихлоргидрнном. Для увеличения механической прочности целлюлозу гранулируют путем частичного гидролиза, в результате которого разрушаются ее аморфные участки. На их место для сохранения пористости между кристаллическими участками вводят химические сшивки. Гранулированная целлюлоза благодаря простоте получения, сравнительно низкой стоимости относится к удобным носителям для иммобилизации ферментов и аффинной хроматографии.
Гранулированную целлюлозу довольно легко превращают в
ю
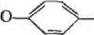
Таблица L Целлюлоза и некоторые ее производные
 Заместитель по ОН-групие
Заместитель по ОН-групие
Название препарата
Фирма

 |
| NH: |
0<CHa)aNH5
ОРОаН
ОСНаСООН O(CHa)aNH*
Целлюлоза
Аминоэтялцеллюлоза
Фосформл целлюлоза (Р-10)
Целлюлоза
Диэтиламиноэтнлцел-поза
Карбокснметнлцеллю-за
А м нноэтил цел л юл оэа
п -Амин обензон л целлюлоза
«Whatman» (Англня)
То же
«Sigma» (США)
*Bk)-Rad-Labs>
(США)
ОСОСН,Вг
O(CH2>aN(CaH5h
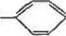
OCH^CONHNHs ОСОСНгВг
Бром аиетн л целл юлоэа
Бенэонлдиэтнламнно
этнлцеллюлозз
Г ндразидка рбокснметнл -
целлюлоза
Ьромя цетил целл юлояа
* ~ Ам ннобензилоксн метил цел л юлоэа
«Serva» (ФРГ) «Reanal» {ВНР)
То же
«Miles Labs» (Англня)
То же То же
I NHs
O(CH5)2N(C*H6)a
OCHjCOOH
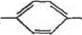 |
| NH? |
осн.
O(CHa)aSO3H O(CHahfi(CaHsb
Д Э АЭ - пел л юл оз а
КМ- целл юлоза
п-А мн н обензнл целлюлоза
С ул ьфоэтнл целл юл оза
Триэтил аммоннйэтнл-
цел.пю;киа
НПО «Биохим-реактнв»
То же
 различные ионообменные производные, В табл. I приведены основные промышленные марки целлюлозы, выпускаемые различными фирмами.
различные ионообменные производные, В табл. I приведены основные промышленные марки целлюлозы, выпускаемые различными фирмами.
Недостатком целлюлозы как носителя можно считать ее неустойчивость к воздействию сильных кислот, щелочей н окнсли-телей.
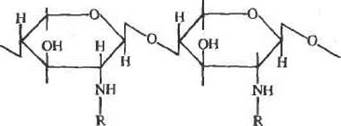
Хитин- —природный аминополнсахарид. Его можно рассматривать как целлюлозу, в которой СН^ОН-группа заменена ацет-амндным остатком:
И
 СН2ОП
СН2ОП
Сн, он
JO
(в хитине R=
в хитозане R =—Н)
Хитин — основной компонент наружного скелета ракообразных, насекомых, а также клеточных оболочек некоторых грибов. Это соединение является отходом промышленной переработки креветок и крабов, поэтому доступно в больших количествах при относительно низкой стоимости.
Хитин обладает пористой структурой, не растворяется в воде, разбавленных кислотах и щелочах, а также в органических растворителях. Для переведения в реакционноспособную форму он может быть модифицирован глутароиым альдегидом, а также солями тяжелых металлов [например, Ti(IV)].
Обработка хитина концентрированными растворами щелочей (деацилирование) приводит к образованию хитозана. Хитозан, имеющий свободные аминогруппы, может использоваться для ковалентной иммобилизации ферментов с помощью таких бифункциональных реагентов, как диа льде гиды, диизоцианаты (см, гл. ill). В отличие от хитина хитоэан растворяется в минеральных и органических кислотах, поэтому для иммобилизации он часто применяется в виде растворов (рН 3—7).
Употребление хитоэана в качестве носителя дает хорошие результаты, так как полученные препараты иммобилизованных ферментов обладают высокой каталитической активностью и устойчивостью к микробному воздействию; наблюдается также существенное повышение термостабильности белков» иммобилизованных на хитозат'.
Декстран — поли-1,6-а-/)-глюкопиранозил-0-гл1ОКопирано-за — разветвленный полисахарид из бактериальных источников, содержащий остатки глюкозы, связанные, в основном, 1,6-глюко-знднымн связями (а также, 1,2-, 1,3- и 1,4-связями):
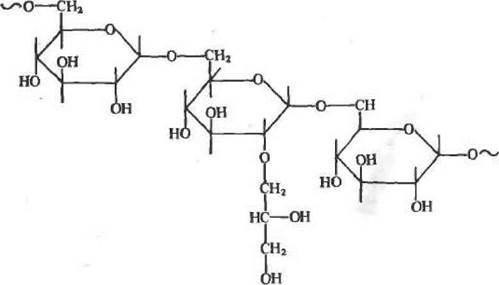
Гели на основе декстрана, сшитые эпихлоргидрнном» выпускаются фирмой «Pharmacia» (Швеция) под названием «сефа-декс» и «Reanab (ВНР) под названием кмолселект». При высушивании сефадексы легко сжимаются, а в водных растворах сильно набухают. Эти качества выражены тем сильнее, чем меньше процентное содержание сшивки. Изменением доли сшивки регулируется средний размер пор, образуемых пространственной сеткой геля.
Следует отметить, что продажные препараты сефадексов содержат небольшое количество карбоксильных групп, что придает им некоторое сродство к катионам Этот факт необходимо учитывать при иммобилизации металлозависимых ферментов.
Обращают на себя внимание такие свойства гелей на основе декстрана, как высокая химическая стойкость и гидрофиль-ность (из-за наличия большого количества гидроксильных групп), Сефадексы G-типов различаются по степени сшитости и, следовательно, по степени набухания и по пористости. Существуют разновидности модифицированных сефадексов для использования в органических растворителях (LH-20 н LH-60).
Фирмы «Pharmacia» и «Reanab выпускают также ряд производных декстрана, содержащих различные функциональные группы (табл. 2),
К группе декстранов можно отнести крахмал, являющийся смесью полисахаридов, основным компонентом которой является амилоза — поли-1,4-а-£)-глюкопиранозил-£) -глюкопираноза и амилопектин — разветвленный полисахарид, состоящий из остатков £>-глюкозы, связанной 1т4-а-глюкозидными связями, а в местах разветвлений — 1,6-оглюкозидными связями.
 Химической модификацией крахмала сшивающими агентами, такими, как формальдегид, глиоксаль, глутаровый альдегид» получен новый носитель — губчатый крахмал, обладающий повышенной устойчивостью по отношению к ферментам, гидролизую-
Химической модификацией крахмала сшивающими агентами, такими, как формальдегид, глиоксаль, глутаровый альдегид» получен новый носитель — губчатый крахмал, обладающий повышенной устойчивостью по отношению к ферментам, гидролизую-
Таблица 2. Коммерческие препараты производных декстрана
 Функциональная группа
Функциональная группа
Название и марка
Фирма



 ОСНгСООН
ОСНгСООН
OCH2CH*N (— СН(ОН)СНЭ
OCHsCOOH
Карбо кс и мети л сефа деке (СМ)
Сульфоп ропнлесфадекс <SP)
Д иэтил а м н ноэти л сефа -деке IDEAE)
Днэтщ] (2-окси пропил) амнноэтнлсефадекс (QAE)
Молселект (СМ)
Молседект (SE)
Молсе-лект (DEAE)
«Pharmacia» (Швеции)
«Reanal» (ВНР)
щим полисахариды. Введение днэтаиол- и триэтаноламиннык групп дает возможность применять губчатый крахмал для иммобилизации различных ферментов.
На основе декстранов могут быть получены водорастворимые препараты с различными функциональными группами, применяемые в медицине как носители лекарственных веществ. Выбор носителей иа основе декстрана для медицинских целей обусловлен, в частности» тем, что они легко подвергаются биодегра-дзции.
Агароза ■ — поли-{5-галактопиранозил*3,6-ангидро-а-/^галакто*-пираноза:
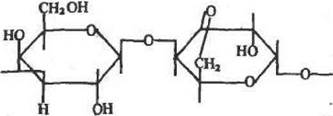
Она широко используется как носитель для иммобилизации. Однако стоимость агарозы довольна высока, поэтому разрабатываются различные методы ее модификации с целью получения легко регенерируемых форм. При охлаждении горячего 2—6%-ного водного раствора агарозы до температуры ниже 45°С образуются прочные крупнопористые гели, представляющие собой сложную смесь из заряженных и нейтральных полисахаридов. В процессе образования геля индивидуальные полисаха-ридные цепи образуют двойные спирали, которые далее агрегируют с образованием «узлов*. При температуре около Ю0°С гель агарозы плавится, поэтому в отличие от сефадексов его нельзя автоклавировать. Высушивание агарозы приводит к необратимой деструкции геля, поэтому его необходимо кранкть в виде водной суспензии.
Гели на основе агарозы производятся фирмами «Pharmacia* (Швеция) и «Bio-Rad Labs» (США) и выпускаются под названиям к «сефароза» и «биогель А» соответственно (табл. 3), а также «LKB» (Швеция) и «IBF* (Франция) — под названием «ультрогель А». При производстве сефарозы агароза подвергается специальной обработке, в частности, из нее удаляются заряженные полисахариды- Различают 3 типа сефароды и 6 типов биогеля А в зависимости от концентрации агарозы (табл. 3).
Дли придания большей химической и термической стабильности препараты сефарозы обрабатывают 2,3-дибромпропанолом в сильно щелочных условиях, В результате такой обработки получается поперечное шитый гель агарозы — сефароза CL (препарат фирмы «Pharmacia»),
Агар выделяют из клеточных мембран некоторых красных морских водорослей. Точный состав ею не известен Однако установлено, что он содержит» по крайней мере, два полисаха-
U
Таблица 3. Агароэа и некоторые ее производные
| Функциональнаягруппа | Названиеи марка | Концентра | Фнрыа | |
| (заместитель по ОН-группе) | ц»я яга розы. | |||
| _ | С-ефароэа 6Б | «Pharmacia» | ||
| (Швеции) | ||||
| — | Сефароза 4В | То же | ||
| I | Ссфароэа 2В | -*- | ||
| + | ДЭАЭ-сефароза | ■ д^ | ||
| CL-6B | ||||
| -ОСНаСООН | КМ—«ефароза CL-6B | — *— | ||
| —OCN | Бромциаисефароэа | _,____________ | ||
| 4В | ||||
| __ОС Н2—С Н—CHs-^O— | Октнлсефароэа | —1— | ||
| | | CL-4B | |||
| ОН | ||||
| —(CHsJt—СНэ | ||||
| —ОСНг—СНОН—СНа—О— | Феннл сефароза | —*— | ||
| -О | CL-4B | |||
| Биогель А-0,5 | «Bio-Rad | |||
| ■ | Labs» (США) | |||
| Биогель А-1,5 | —i— | |||
| Бногель А-5 | —3-------------------- | |||
| Бногель А-15 | —»— | |||
| Биогель А-50 | — и— | |||
| Биогель А-150 | —*— | |||
| —O(CH2)sN(C2H5)2 | ДЭАЭ-бногель А | — | — >— | |
| Активированная | <Pharmada> | |||
| (Швеция) | ||||
| —NH—(СНЙ) в—СОО— | СН—^сефйроза 4В Эпокснактнниро- | |||
| с/ —О—СН£СН—СНа— | То же | |||
| й | наиная сефарояа, 6В | |||
| — О (СНа) 4—О^СНа— | ||||
| ~wm^j FT"""~*Vj -Fli | ||||
рнда: а га розу и агаропектин, Г ел к агара образуются аналогично агарозным при охлаждении горячего водного раствора до температуры 38СС. После высушивания гель агара превращается в прозрачную пленку, что позволяет использовать для изучения иммобилизованного в геле фермента оптические методы исследования. К преимуществам агара следует отнести его низкую стоимость и нетоксичность. Отличительной особенностью этого носителя является способность формировать механически прочные гели даже при малых концентрациях в растворе.
Существенного улучшения свойств агара можно достичь сшиванием эпихлоргидрином, диэпоксидными соединениями и т. д. Сшитый агар с регулируемой проницаемостью устойчив к нагреванию даже в щелочной среде, обладает высокой механической прочностью, а наличие большого количества оксигрупп позволяет легко модифицировать носитель. Это дало основания Дж. Порату (1976) считать агар почти идеальным носителем.
Альгиновые кислоты и их соли — это полисахариды бурых морских водорослей, состоящие из связанных р-1,4-связями остатков £>-маннуроноБОЙ кислоты:
 сода
сода
сош
п
Характерным свойством этих носителей является резкая зависимость их растворимости от температуры и рН раствора. Так, альгиновые кислоты хорошо растворимы в горячей воде и плохо — в холодной. Алыинаты кальция обладают способностью образовывать гели, поэтому они используются для иммобилизации ферментов, клеток и органелл путем включения.
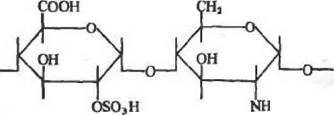
Гепарин представляет собой кислый полисахарид, содержащий чередующиеся звенья сульфатированной D-глюкуроноеой кислоты (или L-идуроновой) и сульфатиро ванного глюкоза мина (или N -ацетил -глюкоз амина):
 |
| OSOaH |
| SOjH |
Гепарин успешно применяется для получения водорастворимых препаратов иммобилизованных ферментов, используемых в медицине для введения in vivo.
Белки. Использование белков в качестве носителей для нм-
мобилизации ферментов представляет интерес как для фундаментальных биохимических исследований, так и для практических целей» в частности для медицины. Этот интерес обусловлен тем, что многие ферменты в клетке функционируют в тесном контакте с другими ее компонентами, & частности с липидами и белками. Поэтому полагают, что изучение поведения ферментов, иммобилизованных на белковых матрицах, позволит понять закономерности функционирования ферментов in vivo. С точки зрения практической значимости важными свойствами этих носителей являются высокая вместимость по отношению к ферментам и способность к биодеградации, а также возможность применения большинства из них (благодаря фибриллярной природе) в виде тонкой толщиной 80 мкм пленки (мембраны). Иммобилизацию на белковых носителях можно проводить как в отсутствие, так и в присутствии сшивающих агентов.
К недостаткам белков как носителей медицинских препаратов для использования in vivo следует отнести высокую иммуно-генность (исключение составляют коллаген и фибрин).
Наиболее часто в качестве носителей применяются структур-ные белки, такие, как кератин, фиброин, коллаген; двигательные белки, в частности миозин, а также транспортные белки» например сывороточный альбумин.
Коллаген — фибриллярный белок группы склеропротеидов, основной компонент хрящей и сухожилии, обладаем высокой прочностью на разрыв. Особенностью этого белка является его высокая гидрофильность. Так, коллаген способен сорбировать от 1 до 5 г воды на 1 г белка, оставаясь в нерастворенном виде и сохраняя волокнистую структуру.
Коллаген — самый распространенный белок высших животных. Легкость выделения коллагена из ряда биологических источников в сочетании со свойственным белкам наличием большого числа групп — участков для связывания ферментов — привлекает внимание к коллагену как к носителю для иммобилизации ферментов. Коллаген используют и в виде модифицированных производных, придавая матрице широкий набор желаемых свойств. Так, блокированием амино- или карбоксильных групп можно изменить поверхностный заряд носителя и, соответственно, гидрофильно — гидрофобный баланс; с помощью сшивающих агентов можно получить сжатую микроструктуру. Наиболее часто коллаген употребляется в азид ной форме. Для этого
карбоксильные группы коллагена®* этерифицируют с последующей обработкой гидразином и азотистой кислотой:
@—CONHNHj
Продуктом переработки коллагена является желатина. Способ ее получения весьма прост-— коллаген длительно обрабаты-
и аллее символом (и) обозначается носитапь
вается кипящей водой, в ходе чего гидролизуются некоторые ковалентные связи коллагена, В результате волокнистый, нерастворимый коллаген превращается в растворимую смесь полинеп-тидов, называемую желатиной. Ценность этого носителя, обладающего гелевой структурой, заключается в его нетоксичности, легкости биодеградации, что позволяет применять желатину в фармацевтической и пищевой промышленностих.
Другим весьма распространенным фибриллярным белком группы склеропротеидов является кератин. Из кератина почти полностью состоят шерсть, волосы, роевые покровы, шелк и т. д. Как правило, кератин получают при переработке перьев (побочный продукт.птицеперерабатывающих фабрик). Таким образом, кератин дешев и доступен в больших количествах, что немаловажно при использовании белков в качестве носителей.
Существуют две формы кератина — аир. Важной особенностью а-кератина является высокое содержанке цистеина, что представляет особый интерес для иммобилизации ферментов, содержащих свободные SH-группы. р-Кератины, в частности фиброин (белок шелка и паутины), не содержат остатков цистеина, но в них очень высокое содержание глицина н аланнна, что необходимо для образования вытянутой зигзагообразной конформа-ции полипептидной цепи. Для 0-конформации характерны межцепочечные водородные связи, в образовании которых участвуют все пептидные группы ji-кератина, что придает значительную устойчивость ^-структуре- Молекулярные отличия влияют на механические свойства. Так, нити fj-кератина обладают мягкостью, гибкостью и нерастворимостью, однако уступают по прочности а-кератину. Выбор той или иной формы кератина для иммобилизации определяется конкретной задачей, стоящей перед исследователем.
При иммобилизации ферментов на носителях белковой природы нельзя не считаться с появлением диффузионных ограничений, определяемых гелевой структурой матрицы. Интересное решение проблемы диффузионных ограничений было найдено в случае использования в качестве носителей бел ков-глобул и но в хлопчатника. Так как комплекс фермент-носитель способен находиться как в растворимой, так и в нерастворимой форме в зависимости от ионной силы раствора, то, изменяя последнюю, можно переводить комплекс в растворимую форму и облегчать, например, переработку нерастворимых в воде субстратов. Здесь укажем также, что подобным свойством обладают и некоторые синтетические полимеры, в частности полиэлектролиты и их комплексы, находящие все более широкое применение для иммобилизации (ферментов.
§ 2. Синтетические полимерные носители
Огромное разнообразие доступных синтетических полимеров обеспечило их широкое использование в качестве носителей для иммобилизации ферментов. Вводя в полимерные молекулы раз-
личные функциональные группы, можно в широких пределах варьировать физические свойства носителя и создаваемое им микроокружение для иммобилизованных молекул фермента. Синтетические полимеры применяются как для ковалентной иммобилизации ферментов, так и для сорбционной, для получения гелей, микрокапсул.
Полимеры на основе стирола. Они янлнются основой многих промышленных марок ионообменных материалов. Для сорбцион-ной иммобилизации применяются как микропористые, так и макропористые {размер пор 10—1000 нм) материалы. Сополимеры стирола в виде сферических частиц с различными сшивающими агентами можно получить гранульной полимеризацией. Наиболее часто в качестве сшивающего агента используется дивинил бензол. Структурный фрагмент с дивинил бензолом можно представить так:
| сн—сн*—сн—Ob—сн—сн,—сн~ |
 сн—сна—сн—сн,—сн—ш3~
сн—сна—сн—сн,—сн—ш3~
Геометрическая структура таких макропористых носителей (размер пор, удельная поверхность) варьируется в широких пределах при изменении количества сшивающего агента и концентрации растворителя мономеров в реакционной среде. Пористость сополимеров стирола регулируют также тем, что проводят полимеризацию в присутствии порообразователей, например добавок, разлагающихся при нагревании с выделением газообразных веществ (NH.C1),
 2015-08-13
2015-08-13 1429
1429
