Более пригодными для промышленного использования могут оказаться природные алюмосиликаты — глины, цеолиты, а также пористая керамика, в состав которой, помимо алюмосиликатов,
входят оксиды титана, циркония, или другие добавки. Поверхность таких носителей аналогично кремнеземным может быть модифицирована различными органическими веществами, например замещенными с плана ми (у-аминопропилтриэтоксисиланом).
Важной характеристикой силикатных и алюмосиликатных носителей является высокая плотность поверхностных групп, связывание белковых молекул на которых может осуществляться как за счет электростатических взаимодействий, так и водородных связей. Это имеет немаловажное значение для эффективной иммобилизации ферментов.
Следует также отметить широко распространенные носители — уголь и графитированную сажу. Уголь может быть использован в качестве носителя как для адсорбционной, так и для ковалентной иммобилизации (после предварительной активации поверхностных оксидных групп).
К достоинствам графитированной сажи можно отнести высокую однородность и электрическую проводимость ее поверхности. Последнее свойство важно при создании биоэлектрокаталитиче-ских систем на основе иммобилизованных ферментов. Серьезным недостатком этого носителя является низкая механическая прочность, что ограничивает его применение. Отложением углерода на гранулированной саже был создан новый носитель - карбо-хром, в котором высокая механическая прочность сочетается с достоинствами графитированной сажи.
Весьма перспективными представляются носители па основе металлов и их оксидов. Эти носители характеризуются высокой механической прочностью, относительной дешевизной, стабильностью, хорошими гидродинамическими свойствами. На практике чаще и ее го употребляются носители ни основе оке идя алюминия и титана. Б промышленном масштабе их получают обычно в виде макропористых порошков, однородных по форме и размеру. Применение матриц этого типа позволяет проводить иммобилизацию ферментов как ко валентным связыванием с носителем, так и адсорбцией на нем. Для ковалентной иммобилизации носитель предварительно активируют <У"амиивПР°пилтриэтоксиси-ланом.
Металлические поверхности, используемые в качестве носителей (А1, Ni, Ti), как правило, модифицируют, либо создавая оксидную пленку на поверхности матрицы, либо покрывая их слоем полимера (производные полистирола, целлюлозы и т, д.). Это позволяет значительно повысить сорбционную вместимость носителя.
Таким образом, рассмотрение основных типов носителей свидетельствует о широких возможностях» предоставляемых химией инженерной энзнмологии. Наиболее полный перечень неорганических и органических носителей для иммобилизации, вырабатываемых промышленностью многих стран мира, приведен в справочнике А. А. Лурье «Хроматографические материалы» (1978).
МЕТОДЫФИЗИЧЕСКОЙ
ИММОБИЛИЗАЦИИФЕРМЕНТОВ
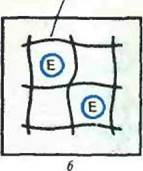
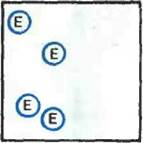
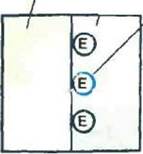
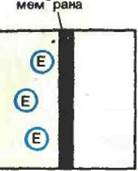
 Согласно одному из принятых определений, которое вытекает из более общего определения иммобилизации, сформулированного во Введении, под иммобилизацией фермента понимается его включение в какую-либо изолированную фазу, которая отделена от фазы свободного раствора, но способна обмениваться с находящимися в последней молекулами субстрата или эффектора. Иными словами, иммобилизация представляет собой включение фермента в такую среду, в которой для него доступной является лишь ограниченная часть общего объема. На основании этого определения все существующие методы физической иммобилизации (т. е. иммобилизации» при которой фермент не соединен с носителем ковалентными связями) можно разделить на четыре группы: I) адсорбция на нерастворимых носителях; 2) включение в поры геля; 3) пространственное отделение фермента от остального объема реакционной системы с помощью полупроницаемой перегородки (мембраны); 4) включение в двухфазную реакционную среду, где фермент растворим и может находиться только в одной из фаз.
Согласно одному из принятых определений, которое вытекает из более общего определения иммобилизации, сформулированного во Введении, под иммобилизацией фермента понимается его включение в какую-либо изолированную фазу, которая отделена от фазы свободного раствора, но способна обмениваться с находящимися в последней молекулами субстрата или эффектора. Иными словами, иммобилизация представляет собой включение фермента в такую среду, в которой для него доступной является лишь ограниченная часть общего объема. На основании этого определения все существующие методы физической иммобилизации (т. е. иммобилизации» при которой фермент не соединен с носителем ковалентными связями) можно разделить на четыре группы: I) адсорбция на нерастворимых носителях; 2) включение в поры геля; 3) пространственное отделение фермента от остального объема реакционной системы с помощью полупроницаемой перегородки (мембраны); 4) включение в двухфазную реакционную среду, где фермент растворим и может находиться только в одной из фаз.
Сущность перечисленных подходов иллюстрируется рис. 2.
Приведенная классификация условна, поскольку не всегда возможно провести четкую границу между различными способами иммобилизации. Например, при иммобилизации путем включения в гель последний можно рассматривать как полупроницаемую мембрану, отделяющую фермент от раствора субстрата. Тем не менее использование такой классификации полезно в том отношении, что она позволяет систематизировать существующие методы физической иммобилизации и помогает ориентироваться в их огромном многообразии.
В задачу настоящей главы не входит подробное описание носителей, применяющихся для иммобилизации, и рассмотрение конкретных примеров иммобилизации различных ферментов. Сведения такого рода содержатся, соответственно, в первой гла-

 |
 |
твердый
носитель раствор фермент
полупроницаемая б
полимерная сетка
ве этой книги и в работав, включенных в список рекомендуемой литературы. В последующем изложении конкретные данное привлекаются лишь в тех случаях, когда это нео& ходимо дли более ясного понимания общих принципов и закономерностей.
Ниже более подробно рассмотрены четыре подхода к физической иммобилизации ферментов, составляющие основу классификации.
ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ ПУТЕМ АДСОРБЦИИ^ НА НЕРАСТВОРИМЫХ НОСИТЕЛЯХ
| Рнс. 2. Способы физической ферментов: а —адсорбция на нерастворимых носителях; б -включение в поры геля; в — отделение фермента с помощью полупроницаемой мембраны; г — не двухфазной реакционной среды |
Адсорбционная иммобилизация является наиболее старым из всех существующих сейчас способов иммобилизации ферментов. Еще в 1916 г.
Дж. Нельсон я Э. Гриффин провели успешную иммобилизацию инвертазы путем адсорбция на активированном угле и геле гид-роксида алюминия. Этот же метод был использован для получения первого технологического иммобилизованного ферментного препарата в 1969 г., когда И. Шибата с сотрудниками осуществили гидролиз Г^-ацетил-£),/,-аминокислот под действием адсорбци-онно иммобилизованной L-аминоацилазы. В настоящее время адсорбционная иммобилизация благодаря целому ряду преимуществ является наиболее широко распространенным способом получения иммобилизованных ферментных препаратов промышленного значения.
 2015-08-13
2015-08-13 792
792








