Температура является количественной мерой «нагретости» тела. Понятие температуры занимает особое место в ряду физических величин, определяющих состояние системы. Температура не только характеризует состояние теплового равновесия данного тела. Она является также тем параметром, который принимает одинаковое значение для любых двух или большего числа тел, находящихся в тепловом равновесии друг с другом, т.е. характеризует тепловое равновесие системы тел. Это значит, что если два или несколько тел, имеющих разные температуры, привести в контакт, то в результате взаимодействия между молекулами эти тела примут одинаковое значение температуры.
Молекулярно-кинетическая теория позволяет выяснить физический смысл температуры. Сравнивая выражения (2.4) и (2.7), видим, что они совпадают, если положить
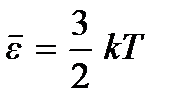 (2.8)
(2.8)
или
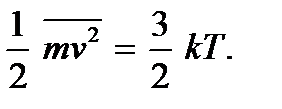 (2.9)
(2.9)
Эти соотношения называют вторыми основными уравнениями молекулярно-кинетической теории газов. Они показывают, что абсолютная температура 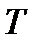 есть величина, определяющая среднюю кинетическую энергию поступательного движения молекул; она является мерой энергии поступательного движения молекул, а тем самым и интенсивности теплового движения молекул. В этом состоит молекулярно-кинетический смысл абсолютной температуры. Как видим, процесс нагревания тела непосредственно связан с увеличением средней кинетической энергии частиц тела. Из (2.9) видно, что абсолютная температура – величина положительная:
есть величина, определяющая среднюю кинетическую энергию поступательного движения молекул; она является мерой энергии поступательного движения молекул, а тем самым и интенсивности теплового движения молекул. В этом состоит молекулярно-кинетический смысл абсолютной температуры. Как видим, процесс нагревания тела непосредственно связан с увеличением средней кинетической энергии частиц тела. Из (2.9) видно, что абсолютная температура – величина положительная: 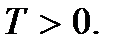 Значение
Значение 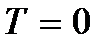 называется абсолютным нулем температуры. Согласно (2.8) при абсолютном нуле должно полностью прекращаться поступательное движение частиц (
называется абсолютным нулем температуры. Согласно (2.8) при абсолютном нуле должно полностью прекращаться поступательное движение частиц (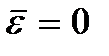 ). Следует, однако, отметить, что при низких температурах газ переходит в конденсированное состояние. Следовательно, теряют смысл и все выводы, сделанные на основе кинетической теории газов. И при абсолютном нуле температуры движение не исчезает. Движение электронов в атомах, движение свободных электронов в металлах полностью сохраняются и при температуре абсолютного нуля. Кроме того, даже при абсолютном нуле сохраняется некоторое колебательное движение атомов внутри молекул и атомов в узлах кристаллической решетки. Существование этих колебаний связано с наличием нулевой энергии у квантового гармонического осциллятора (
). Следует, однако, отметить, что при низких температурах газ переходит в конденсированное состояние. Следовательно, теряют смысл и все выводы, сделанные на основе кинетической теории газов. И при абсолютном нуле температуры движение не исчезает. Движение электронов в атомах, движение свободных электронов в металлах полностью сохраняются и при температуре абсолютного нуля. Кроме того, даже при абсолютном нуле сохраняется некоторое колебательное движение атомов внутри молекул и атомов в узлах кристаллической решетки. Существование этих колебаний связано с наличием нулевой энергии у квантового гармонического осциллятора (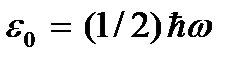 ), в качестве которого можно рассматривать указанные выше колебания атомов. Эта энергия не зависит от температуры, а значит, не обращается в нуль и при
), в качестве которого можно рассматривать указанные выше колебания атомов. Эта энергия не зависит от температуры, а значит, не обращается в нуль и при 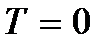 . При низких температурах классические представления о движении перестают выполняться. В этой области действуют квантовые законы, в соответствии с которыми движение частиц не прекращается, даже если понизить температуру тела до абсолютного нуля. Но скорость этого движения уже не зависит от температуры и это движение не является тепловым. Это подтверждается и принципом неопределенности. Если бы частицы тела покоились, то их положения (координаты x, y, z) и импульсы (проекции импульса px, py, pz) были бы точно определены
. При низких температурах классические представления о движении перестают выполняться. В этой области действуют квантовые законы, в соответствии с которыми движение частиц не прекращается, даже если понизить температуру тела до абсолютного нуля. Но скорость этого движения уже не зависит от температуры и это движение не является тепловым. Это подтверждается и принципом неопределенности. Если бы частицы тела покоились, то их положения (координаты x, y, z) и импульсы (проекции импульса px, py, pz) были бы точно определены 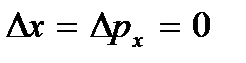 и т.д., а это противоречит соотношениям неопределенностей
и т.д., а это противоречит соотношениям неопределенностей 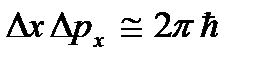 и т.д. Абсолютный нуль не достижим. Ниже будет показано, что абсолютный нуль температуры означает такое состояние системы, при котором система находится в состоянии с наименьшей энергией, и поэтому дальнейшее уменьшение интенсивности движения ее частиц за счет отдачи его энергии окружающим телам не возможно.
и т.д. Абсолютный нуль не достижим. Ниже будет показано, что абсолютный нуль температуры означает такое состояние системы, при котором система находится в состоянии с наименьшей энергией, и поэтому дальнейшее уменьшение интенсивности движения ее частиц за счет отдачи его энергии окружающим телам не возможно.
Формулу (2.7) можно записать в виде.
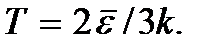
Эта формула может служить определением понятия абсолютной температуры для одноатомного газа. Температуру любой другой системы можно определить как величину, равную температуре одноатомного газа, находящегося в тепловом равновесии с этой системой. Определение температуры с помощью этой формулы верно вплоть до температур, при которых уже нельзя пренебречь вероятностью возникновения электронно-возбужденных состояний атомов газа.
Соотношение (2.8) позволяет ввести так называемую среднюю квадратичную скорость молекулы 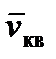 , определив ее как
, определив ее как
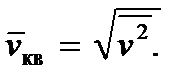
Тогда получим
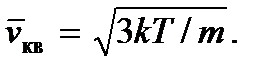
Понятие абсолютной температуры можно более строго ввести в статистической физике, где ее можно рассматривать как модуль статистического распределения частиц по энергиям. Отметим также, что поскольку температура, так же как и давление, как видно из формул (2.7) и (2.8), определяется средней кинетической энергией молекулы идеального газа, то тони представляют собой статистические величины и, следовательно, бессмысленно говорить о температуре или давлении одной или небольшого числа молекул.
 2015-09-06
2015-09-06 6294
6294
