Напомним, что числом степеней свободы материального тела называют число независимых перемещений, которое тело может совершить в пространстве. Оно равно числу независимых переменных (координат), определяющих положение тела в пространстве.
В молекулярно-кинетической теории атом считается материальной точкой (не учитывается его внутренняя структура), поэтому одноатомные молекулы газа обладают только тремя поступательными степенями свободы. В состоянии теплового равновесия вследствие хаотичности теплового движения молекул ни одна поступательная степень свободы не имеет преимущества перед другими. Умножив соотношение (2.5) на 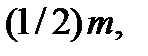 где
где 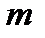 – масса молекулы, придем к соотношению
– масса молекулы, придем к соотношению
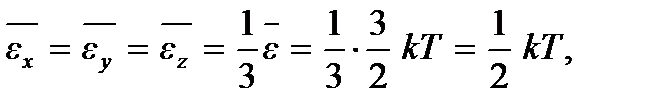
где 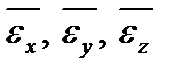 – средние кинетические энергии поступательного движения молекулы вдоль координатных осей
– средние кинетические энергии поступательного движения молекулы вдоль координатных осей 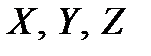 соответственно. Это равенство интерпретируют в виде утверждения о том, что в состоянии теплового равновесия на каждую поступательную степень свободы приходится одинаковая тепловая энергия, равная
соответственно. Это равенство интерпретируют в виде утверждения о том, что в состоянии теплового равновесия на каждую поступательную степень свободы приходится одинаковая тепловая энергия, равная 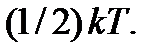
Молекулы газа, содержащие два и более атомов, помимо трех поступательных степеней свободы, связанных с поступательным движением их центра масс, обладают еще и внутренними степенями свободы – вращательными и колебательными, связанными с вращением атомов в молекуле вокруг ее центра масс и колебаниями атомов в молекуле относительно этого центра масс. Количество вращательных степеней свободы 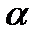 у молекулы в общем случае равно трем (вращение относительно трех координатных осей
у молекулы в общем случае равно трем (вращение относительно трех координатных осей 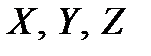 ). Если же атомы в молекуле расположены вдоль одной прямой (такую молекулу называют линейной молекулой), то эту прямую можно совместить с одной из координатных осей, и тогда число вращательных степеней у молекулы будет
). Если же атомы в молекуле расположены вдоль одной прямой (такую молекулу называют линейной молекулой), то эту прямую можно совместить с одной из координатных осей, и тогда число вращательных степеней у молекулы будет 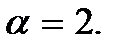 К линейным молекулам относятся и все двухатомные молекулы. Число колебательных степеней свободы
К линейным молекулам относятся и все двухатомные молекулы. Число колебательных степеней свободы 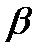 у r -атомных молекул можно определить, вычтя из общего числа
у r -атомных молекул можно определить, вычтя из общего числа 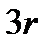 степеней свободы три поступательные степени свободы, связанные с движением их центра масс и
степеней свободы три поступательные степени свободы, связанные с движением их центра масс и 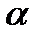 вращательных. Тогда получим
вращательных. Тогда получим 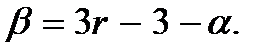
При взаимных столкновениях молекул энергия вращательного движения молекулы может увеличиться за счет энергии поступательного движения другой молекулы либо, наоборот, часть энергии ее вращательного движения может перейти в энергию поступательного движения другой молекулы. Таким путем устанавливается равенство между средними значениями энергии поступательного и вращательного движений молекул газа. Так как при хаотическом движении ни один из видов движения не имеет преимущества перед другими, то можно утверждать, что средняя энергия, приходящаяся на каждую степень свободы вращательного движения, будет также равна 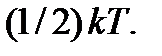
Колебательные движения всегда связаны с переходом кинетической энергии в потенциальную энергию и обратно. Поэтому при учете энергии колебаний атомов в молекуле уже невозможно отделить один вид энергии от другого. В этом случае нужно учитывать не только среднюю кинетическую энергию, приходящуюся на каждую колебательную степень свободы, но и среднюю потенциальную энергию. Если считать, что колебания атомов в молекуле являются гармоническими и учесть, что средние значения кинетической и потенциальной энергий при гармонических колебаниях одинаковы, то можно утверждать, что на колебательную степень свободы приходится в среднем тепловая энергия 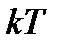 (по
(по 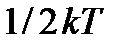 на каждый вид энергии). Иначе говоря, колебательная степень свободы обладает вдвое большей энергоемкостью по сравнению с поступательной и вращательной степенями свободы. Учитывая это для полной средней тепловой энергии многоатомной молекулы можно записать
на каждый вид энергии). Иначе говоря, колебательная степень свободы обладает вдвое большей энергоемкостью по сравнению с поступательной и вращательной степенями свободы. Учитывая это для полной средней тепловой энергии многоатомной молекулы можно записать
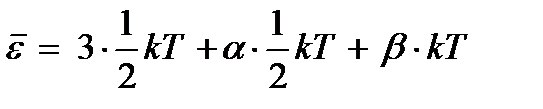
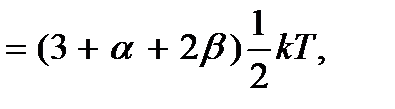
откуда
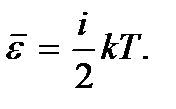 (2.10)
(2.10)
Здесь 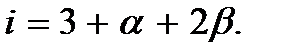 Эту величину называют числом степеней свободы молекулы. При этом считается, что каждое колебание имеет не одну, а две степени свободы. Из равенства (2.10) следует, что в состоянии теплового равновесия на каждую степень свободы молекулы приходится в среднем одинаковая тепловая энергия, равная
Эту величину называют числом степеней свободы молекулы. При этом считается, что каждое колебание имеет не одну, а две степени свободы. Из равенства (2.10) следует, что в состоянии теплового равновесия на каждую степень свободы молекулы приходится в среднем одинаковая тепловая энергия, равная 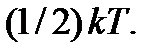 Это утверждение называют законом равнораспределения энергии по степеням свободы.
Это утверждение называют законом равнораспределения энергии по степеням свободы.
Опыт показывает, что вращательными и колебательными степенями свободы молекула обладает не при любой температуре. При низких температурах молекула может двигаться только поступательно (имеет только поступательные степени свободы), а ее вращение и колебание не происходит (вращательные и колебательные степени свободы отсутствуют или, как говорят, «заморожены»). При температурах 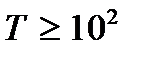 К происходит возбуждение вращательных степеней свободы, а при
К происходит возбуждение вращательных степеней свободы, а при 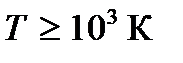 – также и колебательных. Следовательно, при комнатной температуре молекула обладает поступательными и вращательными степенями свободы. В частности, у двухатомной молекулы число степеней свободы равно пяти.
– также и колебательных. Следовательно, при комнатной температуре молекула обладает поступательными и вращательными степенями свободы. В частности, у двухатомной молекулы число степеней свободы равно пяти.
Это объясняется тем, что, согласно квантовым представлениям, энергия внутренних движений молекулы (вращательных и колебательных) может принимать не любые, а лишь отдельные дискретные значения. При описании вращения молекулы ее можно рассматривать как ротатор, а при описании колебаний – как совокупность линейных гармонических осцилляторов. Известно, что энергия ротатора квантована и ее уровни определяются выражением 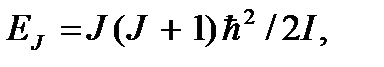 где
где 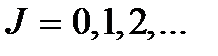 – вращательное квантовое число.
– вращательное квантовое число. 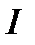 – момент инерции молекулы. Как видим, вращение возникает только при
– момент инерции молекулы. Как видим, вращение возникает только при 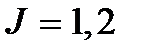 и т.д. Уровень энергии
и т.д. Уровень энергии 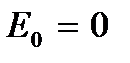 является основным, а энергии
является основным, а энергии 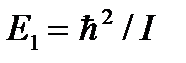 – первым возбужденным. Поэтому для возбуждения вращения требуется энергия
– первым возбужденным. Поэтому для возбуждения вращения требуется энергия 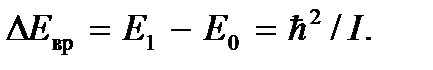 В случае молекулы водорода, например, энергия возбуждения вращательных степеней свободы
В случае молекулы водорода, например, энергия возбуждения вращательных степеней свободы 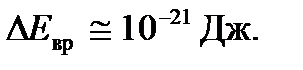 Вероятность возбуждения вращения как вероятность преодоления так называемого термодинамического барьера высотой
Вероятность возбуждения вращения как вероятность преодоления так называемого термодинамического барьера высотой 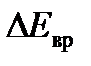 пропорциональна множителю
пропорциональна множителю 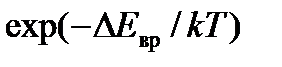 Молекула может получить эту энергию только при столкновении с другой молекулой, при котором энергия поступательного движения другой молекулы может частично или полностью израсходоваться на возбуждение вращения первой молекулы. Энергия теплового движения молекулы по порядку величины равна
Молекула может получить эту энергию только при столкновении с другой молекулой, при котором энергия поступательного движения другой молекулы может частично или полностью израсходоваться на возбуждение вращения первой молекулы. Энергия теплового движения молекулы по порядку величины равна 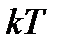 . Следовательно, вращение молекулы возникает при температуре
. Следовательно, вращение молекулы возникает при температуре 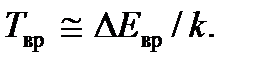 Для молекулы водорода эта температура и составляет указанные выше 102 К. Энергия колебательного движения также квантована и ее уровни определяются выражением
Для молекулы водорода эта температура и составляет указанные выше 102 К. Энергия колебательного движения также квантована и ее уровни определяются выражением 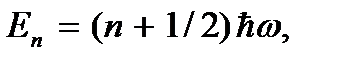 где
где 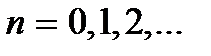 – колебательное квантовое число,
– колебательное квантовое число, 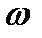 - собственная частота колебаний молекулы. Основным уровнем здесь является уровень
- собственная частота колебаний молекулы. Основным уровнем здесь является уровень 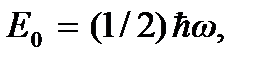 а первым возбужденным – уровень
а первым возбужденным – уровень 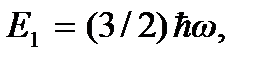 поэтому для возбуждения колебания молекулы ей следует сообщить энергию
поэтому для возбуждения колебания молекулы ей следует сообщить энергию 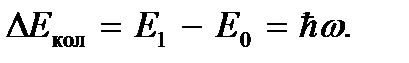 Этой энергии соответствует температура
Этой энергии соответствует температура 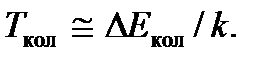 Для молекулы водорода эта температура составляет около 103 К.
Для молекулы водорода эта температура составляет около 103 К.
 2015-09-06
2015-09-06 5437
5437