Сильні електроліти внаслідок повної дисоціації не підлягають закону діючих мас. Еквівалентна електрична провідність сильних електролітів відрізняється від такої слабких електролітів не тільки значенням, але й характером залежності від концентрації. Так, якщо навести графічно залежність l від 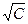 , для слабких електролітів у ділянці великих розведень одержується крива, а для сильних — пряма лінія, яка описується емпіричним рівнянням
, для слабких електролітів у ділянці великих розведень одержується крива, а для сильних — пряма лінія, яка описується емпіричним рівнянням
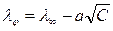 (4.11)
(4.11)
В цьому рівнянні коефіцієнт а залежить від природи розчинника і температури. В цілому другий член рівняння 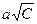 xaрактеризує зменшення електричної провідності за рахунок взаємного гальмування іонів. Для визначення l∞ проводять лінійну екстраполяцію до нульової концентрації. Відрізок, який відсікається на осі ординат, відповідає значенню l∞. Одержані значення порівняють з вирахуваними за рівнянням (4.8), яке справедливе для розведених розчинів сильних електролітів. Відношення електричної провідності за даної концентрації до електричної провідності при нескінченному розведенні для сильних електролітів називається коефіцієнтом електричної провідності
xaрактеризує зменшення електричної провідності за рахунок взаємного гальмування іонів. Для визначення l∞ проводять лінійну екстраполяцію до нульової концентрації. Відрізок, який відсікається на осі ординат, відповідає значенню l∞. Одержані значення порівняють з вирахуваними за рівнянням (4.8), яке справедливе для розведених розчинів сильних електролітів. Відношення електричної провідності за даної концентрації до електричної провідності при нескінченному розведенні для сильних електролітів називається коефіцієнтом електричної провідності
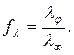 (4.12)
(4.12)
Цей коефіцієнт може приймати значення менше одиниці не в результаті неповної дисоціації, а за рахунок міжіонної взаємодії.
 2015-09-06
2015-09-06 598
598








