Т(n)= 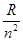 , (1.6)
, (1.6)
то будь-яку довжину хвилі, а значить і частоту, можна представити у вигляді різниці величин Т (n) при різних значеннях цілих чисел:
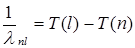 . (1.7)
. (1.7)
Якщо одне з цілих чисел зафіксовано, а інше пробігає всі цілі значення, що більші зафіксованого, отримаємо певну серію.
Величини Т(n) = 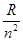 (n =1, 2, 3…) називаються спектральними термами.
(n =1, 2, 3…) називаються спектральними термами.
Таким чином, усі випромінювані частоти можуть бути представлені як комбінації спектральних термів. Це правило називається комбінаційним принципом Ритца.
Як випливає з формул (1.1-1.5), лінії в серії не знаходяться на одній відстані друг від друга.
При збільшенні n частоти спектра наближаються до граничної частоти (наприклад, для серії Бальмера) 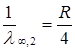 , а різниця між сусідніми частотами необмежено зменшується, тобто експериментально спостерігається згущення ліній у спектрі, що суперечить класичним уявленням про однакову відстань між лініями і про кратність самих частот.
, а різниця між сусідніми частотами необмежено зменшується, тобто експериментально спостерігається згущення ліній у спектрі, що суперечить класичним уявленням про однакову відстань між лініями і про кратність самих частот.
Постулати Бора. Для пояснення експериментальних фактів Нільс Бор у 1913 р. сформулював два постулати:
1) атоми можуть знаходитися не в усіх станах, що допускаються класичною механікою, а тільки в деяких визначених станах, що характеризуються певними, дискретними значеннями енергії Е1, Е2, Е3, …... У цих станах атоми не випромінюють енергію. Тому вони називаються стаціонарними станами. Енергії стаціонарних станів Е1, Е2, Е3 … утворюють дискретний спектр.
2) при переході атома зі стаціонарного стану з більшою енергією Еп2 у стан з меншою енергією Еп1 відбувається випромінювання кванта світла з енергією:
h 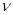 = Еп2 – Еп1 . (1.8)
= Еп2 – Еп1 . (1.8)
- де h - стала Планка, що дорівнює 6,625·10-34 Дж·с;
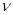 - частота випромінювання.
- частота випромінювання.
Співвідношення (1.8) називається правилом частот Бора. Таке ж співвідношення справедливе і для випадку поглинання, коли падаючий фотон переводить атом з нижчого енергетичного рівня на більш високий.
Енергія Еn електрона, що знаходиться на n-й стаціонарній орбіті, за теорією Бора, дорівнює
Еn =- 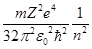 . (1.9)
. (1.9)
Ця формула описує рівні енергії стаціонарних станів електрона у водневоподібному атомі.
Зі зростанням n сусідні рівні енергії атома зближуються, і при n 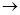 ∞ відстань між ними прагне скоротитися до нуля. Дискретність енергетичного спектра стає усе менш і менш помітною. Тому очікується, що в такому граничному випадку квантова система буде поводитися, як класична. Це положення було висунуто Бором і названо принципом відповідності.
∞ відстань між ними прагне скоротитися до нуля. Дискретність енергетичного спектра стає усе менш і менш помітною. Тому очікується, що в такому граничному випадку квантова система буде поводитися, як класична. Це положення було висунуто Бором і названо принципом відповідності.
Принцип відповідності дозволяє виразити сталу R через фундаментальні величини, що характеризують атом.
З порівняння формули (1.9) і комбінаційного принципу (1.7) одержуємо (при Z =1):
R = 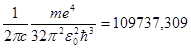 см-1~1,09∙ 107м –1 (1.10)
см-1~1,09∙ 107м –1 (1.10)
Ця величина називається сталою Рідберга для атома водню.
В даній роботі досліджується серія Бальмера, лінії якої знаходяться у видимій частині спектру. Для серії Бальмера n = 2. Для перших чотирьох ліній цієї серії m приймає значення 3, 4, 5 i 6. Ці лініїприйнято умовно позначати H a, H b, H g, H d.
 2015-09-06
2015-09-06 273
273