1. Ввімкнути шнур випромінювача до мережі та ввімкнути пристрій вимикачем "СЕТЬ".
2. Пересвідчитися, що лампа випромінювача працює (за наявністю світла у вікні випромінювача).
3. Зачекати, доки прогріється випромінювач на протязі 1-2 хвилин.
4. Через окуляр монохроматора, повертаючи ручку вимірювання довжини хвилі, спостерігати лінії спектра серії Бальмера. Для вимірювання довжини хвилі встановити відповідну лінію в центрі поля спостерігання монохроматора i за шкалою монохроматора визначити довжину хвиль.
5. По закінченню роботи необхідно вимкнути живлення пристрою вимикачем "СЕТЬ" та вимкнути шнур випромінювача від мережі.
Таблиця 1.1 Довжини хвиль спектральних ліній деяких елементів
| Лампа | Характеристика спектральних ліній | Довжина хвилі, 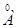
|
| Гелева | червона 1-а слабка | 7065,0 |
| червона 2-а яскрава | 6578,0 | |
| жовта | 5876,0 | |
| зелена 1-а | 5016,0 | |
| зелена 2-а | 4922,0 | |
| голуба | 4713,0 | |
| синя | 4471,0 | |
| фіолетова 1-а | 4026,0 | |
| фіолетова 2-а | 3889,0 | |
| Неонова | яскраво-червона | 6401,0 |
| червоно-оранжевий | 6242,5 | |
| Оранжева 1-а помітна | 5944,8 | |
| жовта | 5852,5 | |
| зелена ліва | 5400,6 | |
| зелена права | 5340,0 | |
| синьо-зелена | 4849,0 | |
| Воднева | червона яскрава | 6569,0 |
| зелено-блакитна | 4861,0 | |
| синя | 4340,0 | |
| фіолетова слабка | 4102,0 | |
| Ртутна | темно-червона | 6907,46 |
| яскраво-червона | 6438,46 | |
| Червоно-оранжева 1-а | 6234,37 | |
| Червоно-оранжева 2-а | 6123,27 | |
| оранжева | 6072,64 | |
| жовта 1-а | 5790,68 | |
| жовта 2-а | 5769,59 | |
| яскраво-зелена | 5460,72 | |
| темно-зелена | 4890,27 | |
| яскраво-синя | 4358,34 | |
| синя середня | 4347,15 | |
| синя слабка | 4339,23 | |
| фіолетова слабка | 4108,07 | |
| фіолетова середня | 4097,7681 | |
| фіолетова яскрава | 4046,56 | |
| Азотна | червона | 6482,0 |
| оранжево-жовта | 6008,0 | |
| оранжево-жовта | 5941,0 | |
| жовта 1-а | 5328,0 | |
| жовта 2-а | 5179,0 | |
| зелена | 5045,0 |
6. За відомими m, n та визначеними в досліді довжинами хвиль 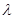 розрахувати сталу Рідберга R за формулою (1.2).
розрахувати сталу Рідберга R за формулою (1.2).
7. Знайти відносну похибку розрахунку сталої Рідберга.
8. Визначити номер рівня m, з якого електрон переходить на рівень n =2, випромінюючи фотон з довжиною хвилі 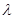 m2.
m2.
9. Розрахувати енергію фотона Ет - Еп = hvmn,, що випромінює електрон при переході з m -го рівня на рівень n =2.
10. Результати експерименту занести до таблиці 1.2.
Таблиця 1.2. Результати вимірів
| Лампа | Характеристика спектральних ліній | Довжина хвилі, 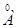
|
Контрольні питання.
1. Сформулювати постулати Н. Бора.
2. Які недоліки теорії Н. Бора?
3. Вивести формулу (1.9) енергії атома водню.
4. Який атом називається водневоподібним?
5. Пояснити фізичний зміст від¢ємного значення енергії електрона в атомі.
6. Визначити за рис.1.1 потенціал іонізації та енергію першого, другого та третього збудженого стану атома водню.
7. Одержати формулу (1.10) для сталої Рідберга.
8. Пояснити фізичний зміст квантового числа n.
9. Розрахувати довжину хвилі резонансної лінії водню.
10. Пояснити, чому, якщо в спектрі випромінювання спостерігається серія Лаймана, то спостерігаються і всі інші серії?
11. Які серії можуть спостерігатися у спектрі поглинання атома водню?
Лабораторна робота № 2
ВИЗНАЧЕННЯ ПОТЕНЦІАЛІВ ЗБУДЖЕННЯ АТОМІВ КРИПТОНУ. ДОСЛІД ФРАНКА І ГЕРЦА
Прилади і обладнання: криптонозаповнений тріод ПМИ-2; установка КФ02, амперметр, осцилограф.
 2015-09-06
2015-09-06 492
492








