Матеріальні тіла є джерелами електромагнітного випромінювання.
При зіткненні один з одним атоми і молекули отримують енергію, переходячи в збуджений стан. Потім цю енергію вони випромінюють. Таким чином, джерелом енергії при тепловому випромінюванні є кінетична енергія теплового руху атомів і молекул.
До початку ХХ століття було з'ясовано, що спектр випромінювання молекул складається із широких розмитих смуг без різких границь. Такі спектри називаються смугастими. Спектр випромінювання атомів складається з окремих різких ліній і називаються лінійчатими. Для кожного елемента існує цілком визначений випромінюваний їм лінійчатий спектр. У такий спосіб по спектру можна визначити елемент, якому він належить.
Закономірності в атомних спектрах. Лінії в спектрах розташовуються закономірно. Окремі лінії в спектрах можуть бути об'єднані в групи ліній, що називаються серіями (рис.1.1).

Рис. 1.1. Рівні енергії атома водню
Наприклад, Лайман відкрив серію ліній, що лежать в ультрафіолетовій частині спектра атома водню
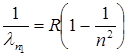 , (n =2, 3, 4…), (1.1)
, (n =2, 3, 4…), (1.1)
- де 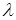 - довжина хвилі випромінювання відповідної лінії;
- довжина хвилі випромінювання відповідної лінії;
R-стала величина.
Бальмер відкрив, що лінії у видимій частині спектра водню можна представити формулою
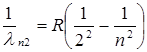 (n =3, 4, 5…). (1.2)
(n =3, 4, 5…). (1.2)
В інфрачервоній частині спектра атома водню були відкриті серії:
Пашена 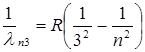 (n =4, 5, 6…), (1.3)
(n =4, 5, 6…), (1.3)
Брекета 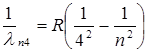 (n =5, 6, 7…), (1.4)
(n =5, 6, 7…), (1.4)
Пфунда 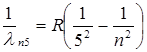 (n =6, 7, 8…). (1.5)
(n =6, 7, 8…). (1.5)
Розгляд формул (1.1-1.5) показує, що кожна з довжин хвиль є різницею величин, що залежать від цілого числа.
 2015-09-06
2015-09-06 201
201







