Существует два способа составления схем распределения электронов в атоме:
1. в виде формул электронных конфигураций, где верхний индекс указывает число электронов на данном подуровне
2. в виде квантовых ячеек (клетка, кружок или черточка) - для изображения электронной орбитали и стрелок - для обозначения электронов, направление которых указывает на ориентацию спинов электронов:
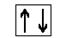
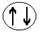
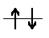
ПРИМЕР 2. Напишите электронную конфигурацию атома калия РЕШЕНИЕ:
19К – 1s2 2s2 2р6 3s2 3p6 4s1;
| n = 4 | ↑ | ||||||||||
| n = 3 | ↑↓ | ↑↓ | ↑↓ | ↑↓ | |||||||
| n = 2 | ↑↓ | ↑↓ | ↑↓ | ↑↓ | d | ||||||
| n = 1 | ↑↓ | p |
s
Каждый электрон в атоме можно охарактеризовать с помощью набора квантовых чисел.
ПРИМЕР 3. О пишите состояние пятого электрона на 4f подуровне (4f5) в атоме с помощью набора квантовых чисел.
РЕШЕНИЕ
Электрон находится на 4f-подуровне, цифра 4 показывает значение главного квантового числа n = 4, а f-подуровню соответствует орбитальное квантовое число 3 (см. таблицу 1), т.е. l =3.  Магнитное квантовое число приобретает значения от –l до +l, т.е. в данном примере
Магнитное квантовое число приобретает значения от –l до +l, т.е. в данном примере

| 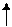
| 
| 
| 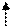
|
–3 –2 –1 0 +1 +2 +3
а пятый электрон попадает в магнитную квантовую ячейку с m=+1. Спиновое квантовое число S = — 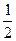 .
.
 2015-10-16
2015-10-16 564
564








