Полисахариды синтезируются из моносахаридов с соблюдением ряда закономерностей. Во-первых, моносахаридные единицы активируются первоначально путем фосфорилирования, катализируемого киназой. Затем моносахаридное звено акцептируется одним из нуклеозиддифосфатов, а образующийся сахаронуклеотид выполняет роль переносчика гликозильного остатка (нуклеотидной «ручки») на удлиняющуюся цепь полисахарида.
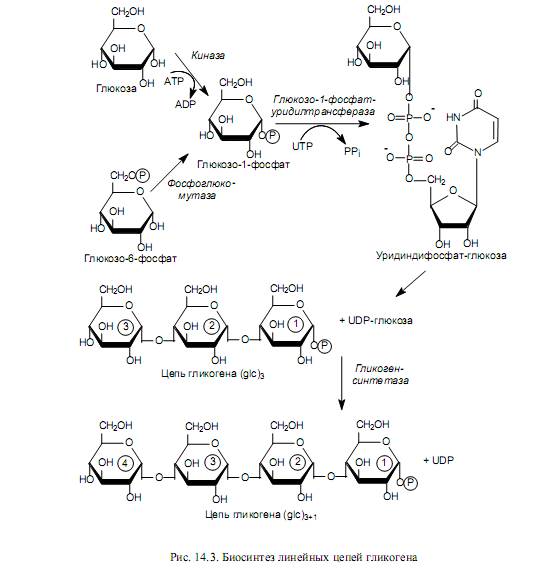
Биосинтез гликогена. Предшественниками для биосинтеза гликогена могут служить как свободная глюкоза, так и глюкозо-6-фосфат. В первом случае глюкоза фосфорилируется киназой с образованием глюкозо-1-фосфата, во втором — глюкозо-6-фосфат изомеризуется с участием фосфоглюкомутазы в глюкозо-1-фосфат (рис. 14.3).
Следующую стадию (образование сахаронуклеотида) катализирует пирофосфорилаза, причем у высших животных гликозильные остатки переносятся на уридиндифосфат (UDP), а в клетках растений и микроорганизмов эту роль выполняют ADP, CDP или GDP. На схемах (рис. 14.3, 14.4) показан процесс синтеза гликогена у животных, и пирофосфорилаза здесь носит название глюкозо-1-фосфат-уридилтрансфераза.
На следующем этапе гликозильная группа UDP-глюкозы переносится на концевую часть цепи гликогена (у нередуцирующего конца) и формируется очередная a(1→4)-гликозидная связь между первым атомом углерода добавляемого остатка глюкозы и кислородом гидроксила у четвертого атома углерода концевого остатка глюкозы цепи. Данную реакцию катализирует гликогенсинтетаза. С помощью этого фермента происходит постепенное удлинение линейных цепей гликогена, однако не может осуществиться образование точек ветвления, характерных для молекул гликогена (рис. 14.3). Функцию образования «ветвей» гликогена катализирует другой фермент —трансгликозилаза.
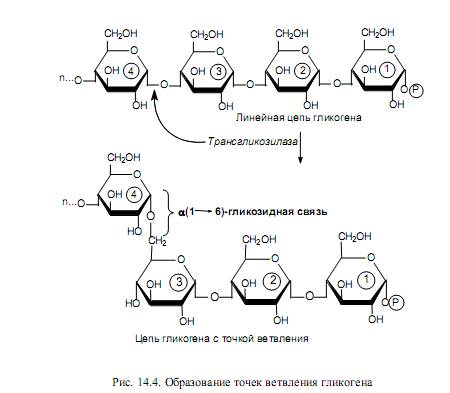
После того как линейная цепь гликогена достигнет длины примерно в 10 остатков глюкозы, трансгликозилаза атакует гликозидную связь в каком-либо месте цепи и переносит концевой олигосахаридный фрагмент, содержащий 6—7 гликозильных звеньев, на свободную 6-гидроксильную группу остатка глюкозы той же или другой цепи. Так катализируется образование a(1→6)- гликозидной связи, и в молекуле гликогена появляется точка ветвления (рис. 14.4). Аналогичным образом в клетках растений осуществляется синтез крахмала.
Биосинтез, а также распад гликогена регулируются у высших организмов гормонами. В частности, у животных в этих процессах принимают активное участие адреналин и глюкагон. При повышении их концентрации в крови количество гликогена уменьшается и, соответственно, увеличивается количество глюкозы.
Биосинтез муреина. В отличие от гликогена, биосинтез которого протекает внутри клетки, муреин, являясь компонентом клеточной стенки бактерий, синтезируется с участием нескольких стадий, осуществляющихся вне клетки — на наружной поверхности плазматической мембраны. При этом клетка вынуждена транспортировать через мембрану отдельные структурные компоненты муреина, для чего существует специальный механизм.
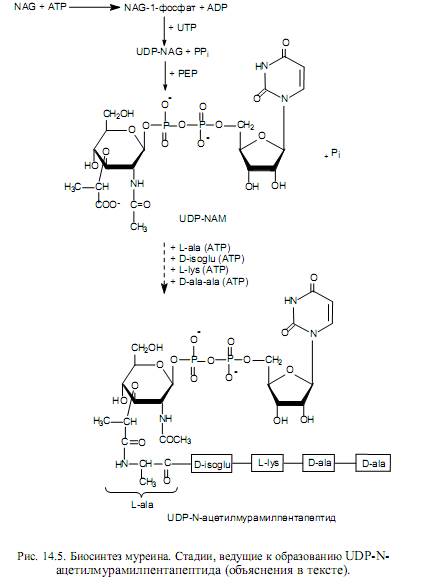
Непосредственным предшественником биосинтеза муреина служит N-ацетилглюкозамин, и первые этапы биосинтеза происходят с соблюдением уже описанных закономерностей, включая фосфорилирование предшественника и его перенос на остаток UDP (рис. 14.5). В результате этих реакций формируется UDP-N-ацетилглюкозамин (UDP-NAG).
На следующем этапе UDP-NAG трансформируется во второй компонент этого гетерополимера — UDP-N-ацетилмурамовую кислоту (UDP-NAM). Для этого к молекуле UDP-NAG присоединяется остаток молочной кислоты при взаимодействии с фосфоенолпируватом (РЕР). Далее к UDP-NAM добавляются последовательно остатки пяти аминокислот, и образуется UDP-N-ацетилмурамилпентапептид (рис. 14.5).
Пентапепидная цепь в составе UDP-N-ацетилмурамилпентапептида строится необычным образом: образование пептидных связей здесь происходит за счет энергии АТР с участием специальных ферментов. Такой пептид (содержащий D-аминокислоты и g-пептидную связь) не может быть синтезирован обычным путем на рибосомах.
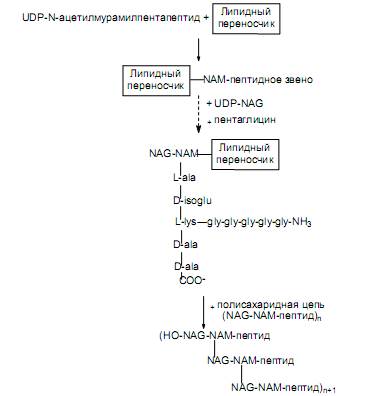
Сформированный N-ацетилмурамилпентапептид переносится с помощью фермента от UDP на связанный с мембраной липидный переносчик—гидрофобную молекулу, способную совершать челночные перемещения через мембрану. После этого к NAM-пептидной единице, связанной с липидным переносчиком, присоединяется NAG (его донором служит образованный ранее UDP-NAG) и формируется дисахаридное звено.
Структура b(1→4)-гликозидной связи между моносахаридными единицами представлена на рис. 5.4. Наконец, на e-аминогруппе остатка лизина в пентапептиде выстраивается пентаглициновый мостик (рис. 14.6).
Образовавшееся дисахарид-пептидное звено переносится от липидного переносчика на растущую полисахаридную цепь (рис. 14.6). На последнем этапе отдельные полисахаридные цепи поперечно связываются пентаглициновыми мостиками (реакция транспептидирования, катализируемая ферментом гликопептид-транспептидазой). В ходе этой реакции концевая аминогруппа пентаглицинового мостика атакует пептидную связь между двумя остатками D-аланина в пентапептиде другой дисахаридной единицы. Так возникает пептидная связь между концевым остатком глицина и остатком D-ala. При этом второй (концевой) остаток D-ala высвобождается. Данная реакция осуществляется уже вне клетки и не требует участия АТР, поскольку протекает за счет энергии гидролизу- емой связи D-ala—D-ala. Сформировавшаяся структура представлена на рис. 5.6.
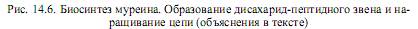
Процесс биосинтеза муреина подвержен ингибирующему действию со стороны некоторых антибиотиков. В частности, b-лактамные антибиотики ковалентно связываются с активным центром гликопептид-транспептидазы, вызывая ее необратимое ингибирование (глава 18). В таком случае не может осуществиться последняя стадия биосинтеза —образование поперечных сшивок между тетрапептидами. Бацитрацин блокирует регенерацию липидного переносчика, останавливая синтез клеточной стенки.
Большинство экзополисахаридов синтезируется с соблюдением описанных для биосинтеза муреина закономерностей: участие нуклеозиддифосфатов, липидных переносчиков, сборка полисахаридных молекул из дисахаридных звеньев на поверхности клетки с помощью внеклеточных ферментов.
 2015-10-16
2015-10-16 4019
4019
