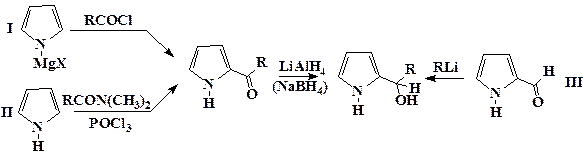
Пиррилкарбинолы самоконденсируются давая мезо- замещенные порфирины в условиях реакции Ротмунда. Выхода порфиринов в этой реакции сопоставимы с таковыми для конденсации пиррола с альдегидами. Кроме того, окрашенные промежуточные соединения, наблюдаемые при проведении конденсации пиррола с альдегидом, те же самые, что и при самоконденсации соответствующего пиррилкарбинола. Эти результаты доказывают, что пиррилкарбинолы действительно являются промежуточными продуктами при проведении реакции Ротмунда в кислой среде.
Синтез мезо- замещенных порфиринов обычно проводится в условиях сходных с условиями реакции Ротмунда, однако в некоторых случаях наблюдается значительное увеличение выхода порфиринов при добавлении в реакционную смесь ацетата цинка. Метод с использованием пиррилкарбинолов используется в основном для получения мезо- алкилпорфиринов и затрудненных порфиринов. Интерес вызывает тот факт, что объемистые пиррилкарбинолы, производные от 2-изобутирил- или 2-пивалоилпиррола не могут быть превращены в соответствующие порфирины.
Конденсация альдегида с пирролом позволяет получить порфирин, имеющий четыре одинаковые мезо -заместителя. Однако существует много задач, которые требуют наличия различных заместителей на периферии порфиринового цикла. Одним из простых подходов к этой цели является так называемая смешанно-альдегидная конденсация. Реакция пиррола со смесью двух альдегидов позволяет получить смесь шести порфиринов, которую разделяют с помощью тонкослойной хроматографии, а в случае наличия в одном из альдегидов сильнополярной группы с использованием колоночной хроматографии.
Синтез несимметрично замещенных мезо- тетразамещенных порфиринов
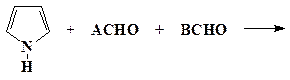
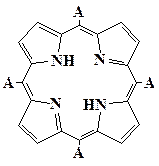
| 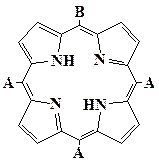
| 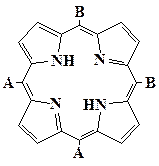
|
| A4 | A3B | цис- А2В2(ААВВ) |
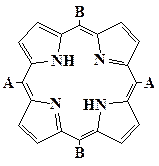
| 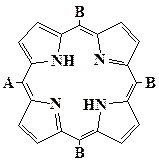
| 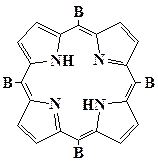
|
| транс- А2В2(АВАВ) | АВ3 | В4 |
Статистическое распределение смеси порфиринов при смешанноальдегидной конденсации
| Отношение Альдегидов (А:В) | A4 | A3B | цис- А2В2(ААВВ) | транс- А2В2 (АВАВ) | АВ3 | В4 |
| 1:1 | 6,25 | 12,5 | 6,25 | |||
| 3:1 | 31,64 | 42,19 | 14,06 | 7,03 | 4,69 | 0,39 |
Ожидаемое отношение порфиринов в смешанно-альдегидной конденсации задается биноминальным распределением. При соотношение альдегидов 1:1, распределение следующие: A4 - 6,25%; А3В - 25%; цис- A2B2 - 25%; транс- A2B2 – 12,5%; AB3 - 25%; B4 – 6,25%. Этот результат подразумевает равную реакционную способность обоих альдегидов во всех стадиях реакции образования порфирина. А3В -порфирины наиболее часто получают при смешанно-альдегдной конденсации. Фракция А3В -порфирина максимальна при соотношении реагирующих альдегидов 3: 1: A4 – 31,64%; А3В – 42,19%; цис- A2B2 – 14,06%; транс- A2B2 –7,03%; AB3 – 4,69%; B4 – 0,39%. Большее содержание А -альдегида повышает содержание A4 -порфирина при снижении абсолютного количества А3В -порфирина. Однако, отношение реагирующих альдегидов, дающее самый высокий изолированный выход А3В -порфирина, зависит от фактических реакционных способностей этих альдегидов, а также от легкости разделения смеси порфиринов. Когда для получения АB3 -порфиринов используется смесь сильнополярного, труднодоступного альдегида и малополярного альдегида, иногда бывает выгодно использовать большой избыток последнего, чтобы более полно прореагировал первый. При этом образуется, в основном, симметрично замещенный B4 -порфирин, который, однако, можно отделить хроматографически от требуемого АВ3 -порфирина.
Практически, изолированные выхода АВ3 -порфиринов в методе Адлера в основном бывают на уровне 5%, имея приблизительный общий выход смеси порфиринов в 20% порфиринов и статистическом распределении смеси порфиринов.
Реакционная способность альдегидов в смешанно-альдегидной конденсации в большинстве случаев резко различается, поэтому для проведения таких синтезов наиболее подходит метод Линдсея или модифицированный метод Адлера, когда первая стадия реакции проводится в отсутствии кислорода воздуха, чтобы избежать окисления порфириногена образованного более реакционноспособным альдегидом и добиться равновесия между порфириногенами задаваемого соотношением исходных альдегидов.
Иногда реакцию проводят с двумя альдегидами близкой реакционной способности или с альдегидами устойчивыми в условиях синтеза, а далее модификацией заместителей придают им требуемую полярность или структуру (окси из метокси, амино из нитро, формил из бром).
Интерес представляет тот факт, что порфирины которые не дают мезо -тетразамещенных порфиринов зачастую вступают в качестве одного из компонентов в смешанно-альдегидную конденсацию.
 2015-10-16
2015-10-16 673
673








