Мета роботи: визначити пероксидне число у маргарині (спреді).
Реактиви та матеріали:
- Ваги лабораторні згідно з ГОСТ 24104, 2-го класу точності з найбільшою межею зважування 200 г.;
- Склянки циліндричні для досліджуваної, проби необхідної місткості (за масою проби).
- Бюретки згідно з ГОСТ 29251
- Піпетки згідно з ГОСТ 29169.
- Циліндри 100 мл згідно з ГОСТ 1770
- Секундомір згідно з чинною нормативною документацією.
- Хлороформ згідно з ГОСТ 20015
- Кислота оцтова згідно з ГОСТ 61, х. ч., льодяна
- Калій йодид згідно з ГОСТ 4232, х. ч., водний розчин із масовою часткою 50…55 %,
- Натрій сірчистокислий (натрію тіосульфат) пентагідрат згідно з ГОСТ 27068, водний розчин молярних концентрацій c(Na2S2О3∙5Н2О) = 0,01 моль/дм3;
- Стандарт-титри тіосульфату натрію згідно з чинною нормативною документацією з масою речовини в ампулі, що дорівнює 0,1 г-екв. — 0,1 г-моль
- Крохмаль розчинний згідно з ГОСТ 10163, розчин з масовою часткою 0,5 %.
- Вода дистильована згідно з ГОСТ 6709
1. Правила приготування до аналізу
Розчин йодиду калію зберігають у темній посудині. Перед використовуванням його перевіряють. Для цього додають 2 краплі розчину крохмалю до 0,5 см3 розчину йодиду калію в 30 см3 суміші оцтової кислоти і хлороформу у співвідношенні 3:2. Якщо утвориться блакитна забарвленість, для знебарвлювання якої потрібно більше ніж 1 крапля 0,01 моль/дм3 розчину тіосульфату натрію то розчин йодистого калію не використовують і готують свіжий.
Розчин крохмалю готують так: 5 г розчинного крохмалю змішують із 30 см3 води, додають цю суміш до 1000 см3 киплячої води і кип'ятять протягом 3 хвилин.
Розчин натрію сіркуватистокислого (натрію тіосульфату) молярної концентрації с (Na2S2О3∙5Н2О)=0,1 моль/дм3 (0,1 н.) готують зі стандарт-титрів (фіксаналів) таким чином.
Теплою водою змивають напис на ампулі і добре її обтирають. У мірну колбу місткістю 1 дм3 вставляють спеціальну воронку, в яку вкладений скляний бойок (звичайно додають до кожної коробки стандарт-титрів), гострий кінець якого повинен бути звернений угору. Якщо спеціальної воронки нема, можна користуватися звичайною хімічною воронкою, в яку вставлено скляний бойок. Коли бойок буде правильно укладений у воронці, ампулі з речовиною дають вільно падати так, щоб тонке дно ампули розбилося під час удару об гострий кінець бойка. Після цього пробивають верхнє поглиблення ампули і весь її вміст обережним струшуванням висипають у колбу. Ампулу, не змінюючи її положення, промивають дистильованою водою. Після цього ампулу видаляють, а розчин доливають з дистильованою водою до мітки, закривають колбу пробкою і обережно ретельно перемішують до повного розчинення речовини. Розчин придатний до застосування через 10…14 діб. Розчин зберігають у склянці з темного скла.
Термін зберігання розчину тіосульфату натрію без додаткового контролю концентрації - 1 місяць.
Після закінчення терміну зберігання необхідно визначити поправку до номінальної концентрації розчину тіосульфату натрію. Якщо величина поправки становить не менше ніж 0,9, розчин може бути використаний.
Якщо під час зберігання з'являються пластівці або осад, розчин не треба застосовувати.
Для отримання розчину тіосульфату натрію необхідних молярних концентрацій с (Na2S2О3∙5Н2О)=0,002 моль/дм3 і с (Na2S2О3∙5Н2О)=0,01 моль/дм3 розчини розбавляють відповідно в 50 і 10 разів. Розбавляють безпосередньо перед використанням.
2. Підготовка проб для аналізу
Масу дослідної проби, залежно від передбачуваного пероксидного числа, визначають згідно з таблицею 8.1.
Таблиця 8.1. – Залежність величини дослідної проби від передбачуваного пероксидного числа
| Передбачуване значення пероксидного числа, ммоль/кг | Маса дослідної проби, г |
| 0…6,0 | 5,000…2,000 |
| 6,0…10,0 | 2,000…1,200 |
| 10,0…15,0 | 1,200…0,600 |
| 15,0…25,0 | 0,600…0,500 |
| 25,0…40,0 | 0,500…0,300 |
Пробу зважують у колбу. Якщо колбу не можна зважити безпосередньо, то дослідну пробу зважують у склянці. У випадку, якщо зважували в склянці, її разом із дослідною пробою вміщують у колбу.
3. Проведення аналізу
У колбу додають 10 см3 хлороформу, швидко розчиняють дослідну пробу, приливають 15 см3 оцтової кислоти і 1 см3 розчину йодиду калію, після чого колбу відразу закривають, перемішують вміст протягом 1 хв і залишають на 5 хв у темному місці за температури від 15 °С до 25 °С. Потім додають 75 см3 води, ретельно перемішують і додають розчин крохмалю до появи слабкої однорідної фіолетово-синьої забарвленості. Йод, що виділився, титрують розчином тіосульфату натрію до молочно-білої забарвленості, стійкої протягом 5 с, використовуючи розчин тіосульфату натрію молярної концентрації С (Na2S2О3∙5Н20) = 0,002 моль/дм3, якщо передбачуване пероксидне число не більше ніж 6,0 ммоль/кг.
Якщо передбачуване значення пероксидного числа більше ніж 6,0 ммоль/кг, після додавання води і перемішування йод, що виділився, титрують розчином тіосульфату натрію молярної концентрації С (Na2S2О3∙5Н2О) = 0,01 моль/дм3 до помітного зниження інтенсивності жовтої забарвленості розчину. Обережно додають крохмаль до появи слабкої однорідної фіолетово-синьої забарвленості. Йод, що залишився, титрують розчином тіосульфату натрію до молочно-білої забарвленості. Допустима наявність різних відтінків забарвленості відповідно до специфічних особливостей забарвленості дослідних олій.
Якщо очікуване пероксидне число менше ніж 1,0 ммоль/кг, то для титрування рекомендовано використовувати мікробюретку об'ємом 5 см3.
Для кожної дослідної проби виконують два вимірювання. Контрольне вимірювання проводять паралельно з основними вимірюваннями.
Якщо на контрольне вимірювання піде більше ніж 0,1 см3 0,01 моль/дм3 розчину тіосульфата натрію, то перевіряють відповідність реактивів вимогам стандартів.
4. Обробка результатів
Пероксидне число (X) в 1/2 О ммоль/кг обчислюють за формулою:
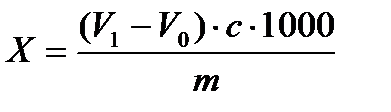 (8.3)
(8.3)
де V0 — об'єм розчину тіосульфату натрію, використаний у контрольному досліді, см3;
V0 — об'єм розчину тіосульфату натрію, використаний в основному досліді, см3;
с — дійсна концентрація використаного розчину тіосульфату натрію, обчислена з урахуванням поправки до номінальної концентрації, моль/дм3;
m — маса дослідної проби, г;
1000 — коефіцієнт, що враховує перерахунок результату вимірювання в ммоль/кг.
Висновки: ____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Запитання і завдання для самоконтролю:
1. Перелічити основні групи жирів.
2. Які вимоги пред’являються до оцінки якості твердих жирів?
3. Які вимоги пред’являються до оцінки якості олій?
4. Які фізико-хімічні показники контролюються в тваринних жирах?
5. Які фізико-хімічні показники контролюються в оліях?
6. Перелічити методи, які застосовуються для визначення якості жирів. Розкрийте суть методу визначення вмісту вологи.
7. Розкрийте суть методу визначення кислотного числа.
8. Які основні органолептичні показники контролюються у оліях?
 2015-10-13
2015-10-13 918
918







