1. Принцип Паулі. У атомі не може бути двох електронів, у яких значення всіх квантових чисел (n, l, m, s) були б однакові, тобто на кожній орбитали може знаходитися не більше двох електронів (з протилежними спинами).
2. Правило Клечковського (принцип найменшої енергії). У основному стані кожен електрон розташовується так, щоб його енергія була мінімальною. Чим менше сума (n + l), тим менше енергія орбіталі. При заданому значенні (n + l) найменшу енергію має орбіталь з меншим n. Енергія орбіталей зростає в ряду:
1S < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 5d» 4f < 6p < 7s.
3. Правило Хунда. Атом в основному стані повинен мати максимально можливе число неспарених електронів в межах певного підрівня.
Наприклад, розподіл електронів в атомі Хлор у: 1s22s22p6 3s2 3p5
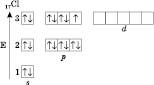
Один неспарений електрон визначає валентність Хлору в такому стані — 1, це нормальний або незбуджений стан атому.
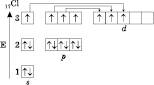
Під час отримання додаткової енергії (опромінення, нагрівання) можливе розпарування електронів (промотування). Такий стан атома ще називається збуджени м. При цьому кількість неспарених електронів збільшується і, відповідно, змінюється валентність атома.
Збуджений стан атома Хлор у- Відповідно до числа неспарених електронів Хлор може мати валентність III, V і VII.
Питання для самоконтролю
1. Скільки протонів, нейтронів і електронів знаходиться в атомах: Дейтерію, Карбону-12, Алюмінію-27? Наведіть електронні формули і схеми цих атомів, підкресліть валентні електрони.
2. Що таке орбіталь? Які форми орбіталей Ви знаєте?
3. Який фізичний зміст: протонного числа, номера групи, номера періоду?
4. Складіть схеми будови атомів елементів другого і третього періодів ПСХЕ.
5. При взаємодії 9,2г одновалентного металу з хлором добуто 23,4г хлориду. Визначте метал.
6. При взаємодії 4,6г одновалентного металу з водою виділилось 0,1моль водню. Визначте метал.
7. При взаємодії 12,4г оксиду одновалентного металу з водою добуто 16г його гідроксиду. Визначте метал.
8. Що спільне в будові атомів елементів з протонними числами: а) 3 і 8; б) 11 і 12; в) 33 і 34; г) 16 і 34?
9. Яку кількість неспарених електронів містить електронна оболонка атома елемента з протонним числом — 13,10,18?
10. Назвіть елемент за такими даними:
а) знаходиться в I групі, відносна молекулярна маса гідроксиду 102;
б) знаходиться в V групі, відносна молекулярна маса вищого оксиду 108.
Література:
1.Петров М.М., Михилев М.А., Кукушкина Ю.Н. Неорганическая химия, Л.: Химия, 1989.
2. В.П. Басов., Родіонов В.М. Хімія. –К.: Каравела, 2004.- 320с
 2015-10-13
2015-10-13 770
770







