При составлении настоящих таблиц предполагается, что во всем диапазоне табличных данных газ подчиняется уравнению состояния идеальных газов
pv = RT. (1)
Неточность этого уравнения, вообще говоря, возрастает с понижением температуры и ростом давления. Практически же в теплотехнических расчетах приходится иметь дело с повышенными давлениями в области высоких температур и с пониженными давлениями в области сравнительно низких температур. Иными словами, практически чаще всего в теплоэнергетике имеем дело с такими параметрами состояния газов, которые благоприятны с точки зрения точности принятого уравнения состояния. Так как внутренняя энергия и энтальпия газа, подчиняющегося уравнению (1), зависят только от температуры, то таблицы могут быть составлены только по одному параметру, что сильно упрощает расчеты.
Запишем основное уравнение термодинамики в форме
Tds = dh — vdp (2)
или
Tds = сpdT — vdp. (2a)
Для изоэнтропного процесса
0 = cpdT — vdp. (3)
Подставив в последнее выражение вместо и его значение и из уравнения (1), получим после разделения переменных
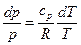 (3а)
(3а)
и после интегрирования
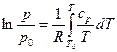 (4)
(4)
Обозначив 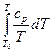 через s°, перепишем последнее выражение в виде
через s°, перепишем последнее выражение в виде
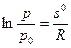 (5)
(5)
Если принять какую-либо температуру Т0 за базовую, то отношение давлений р/ро = π0, называемое ниже относительным давлением, определится как функция температуры независимо от значения энтропии.
Соответствующее отношение удельных объемов также является функцией температуры и определяется выражением
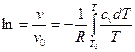 (6)
(6)
или
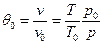 . (7)
. (7)
Уравнение (2) можно записать в таком виде:
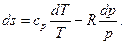 (8)
(8)
Значение энтропии может быть определено выражением
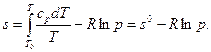 (9)
(9)
Здесь принят отсчет энтропии от произвольно выбранного нулевого значения при базовой температуре То и давлении, равном единице. Изменение энтропии между двумя состояниями равно
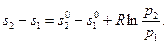
Анализируя уравнения (5), (9) и (10), можно установить, что отношение давлений p1 и р2 при изоэнтропном процессе, протекающем от температуры Т1 до температуры Т2, соответственно равно отношению относительных давлений π01 и π02, соответствующих температурам Т1 и Т2:
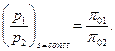 (11)
(11)
Аналогично
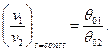 (12)
(12)
 2015-10-13
2015-10-13 353
353








