Раствор приобретает лимонно-желтую окраску.
г) Мерную пипетку на 10 мл промыть и заполнить рабочим раствором нитрата серебра (С осторожностью!)
д) Титровать раствор калия бромида рабочим раствором AgNO3 до окрашивания осадка в оранжево-жёлтый цвет.
Титрование повторить ещё 1 раз.
Вычислить средний объем:
V1 + V2
Vcp = -----------------;
е) Составить условие задачи, сделать расчёт:

KBr AgNO3
10 - 100 Сэ = 0,05 моль/л
\ / Vcp =
 5 K =
5 K =
W (%) =?
РЕШЕНИЕ
Написать уравнения реакций
 KBr + AgNO3
KBr + AgNO3
 AgNO3 + K2CrO4
AgNO3 + K2CrO4
Вычислить молярную массу эквивалента калия бромида
М (KBr) = 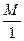
Вычислить титр по определяемому веществу
Cэ(AgNO3) • М (KBr)
T AgNO3/ KBr =--------------------------------;
Вычислить массовую долю калия бромида в растворе:
T(AgNO3) / KBr • V cp (AgNO3) • K • V(мер. колб) •100
W(%) = --------------------------------------------------------------
V исслед. р-р (10) • Vразбавл. р-р (5)
Сделать вывод по проделанной работе.

 2015-10-14
2015-10-14 610
610








