Изоферменты – ряд форм одного и того же фермента, которые катализируют одну и ту же реакцию, но различаются по свойствам: оптимуму температуры, отношению к ингибиторам, локализации. Обнаружены изоферменты более, чем у 100 ферментов.
Мультиферментные комплексы
Мультиферментный комплекс – группа ферментов, катализирующих последовательно все этапы превращения вещества.
Например, синтез жирных кислот катализируется комплексом, состоящим из 7 ферментов.
Коферменты
Коферменты – небелковые компоненты ферментов.
Рассмотрим наиболее важные в биологическом аспекте коферменты.
Никотиноамидные коферменты (НАД, НАДФ).
НАД (NAD) и НАДФ (NADP) по химической природе динуклеотидные коферменты, то есть состоящие из двух мононуклеотидов (АМФ и нуклеотида, содержащего амид никотиновой кислоты). Никотинамид – это водорастворимый витамин РР.
NH2



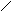
 О
О
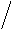




 -С N N
-С N N
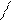
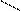
 NH2 O O
NH2 O O
|| ||




 N O CH2 – O – P – O – P – O – CH2 O N N
N O CH2 – O – P – O – P – O – CH2 O N N
 | |
| |

 H H OH OH H H
H H OH OH H H


OH OH OH OH
Никотинамидадениндинуклеотид (НАД)
NH2



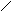
 О
О
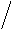




 -С N N
-С N N
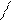
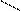
 NH2 O O
NH2 O O
|| ||




 N O CH2 – O – P – O – P – O – CH2 O N N
N O CH2 – O – P – O – P – O – CH2 O N N
 | |
| |

 H H OH OH H H
H H OH OH H H


 ОН
ОН
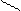 OH OH OH O – Р = О
OH OH OH O – Р = О
ОН
Никотинамидадениннуклеотидфосфат (НАДФ)
Биологическая роль НАД и НАДФ.
Входят в состав оксидоредуктаз – анаэробных дегидрогеназ, принимают участие в окислительно-восстановительных процессах поэтапного переноса водорода (цикл Кребса, дыхательная цепь). Витамин РР служит составной частью 150 анаэробных дегидрогеназ.
Коферменты ФМН (FMN) и ФАД (FAD).
Флавиномононуклеотид (ФМН) – по химической природе мононуклеотид.
Флавинадениндинуклеотид (ФАД) – по химической природе – динуклеотид, состоит из АМФ + ФМН. ФАД ФМН содержит витамин В2 (рибофлавин).
Рибофлавин = рибитол + изоллоксазин
Ферменты, содержащие в своем составе ФАД, называют флавиновыми или флавопротеидными. В клетках находится около 60 флавопротеидов. Флавиновые ферменты – аэробные дегидрогеназы, относятся к оксидоредуктазам.
CH3 N O NH

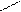








 Изоаллоксазин
Изоаллоксазин
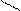
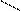
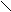



CH3 N O
|
CH2
|
H-C-OH
|
H-C-OH Рибитол
|
H-C-OH
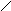 | OH
| OH
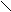 CH2 – O – P = O Флавинмононуклеотид (ФМН)
CH2 – O – P = O Флавинмононуклеотид (ФМН)
OH
CH3 N O NH

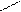












CH3 N O
|
CH2
| NH2
H-C-OH |

 | N N
| N N

 H-C-OH
H-C-OH
 |
|
H-C-OH О O
| || || N N
CH2 – O – P – O – P – O – CH2 O
 | | |
| | |
 OH OH H
OH OH H
OH
Флавинадениннуклеотид
Биологическая роль флавиновых ферментов – катализируют аэробные окислительно-восстановительные реакции в живой системе, например, окисляют восстановительные коферменты – НАД Н2, НАДФ Н2, несущие Н2 в дыхательной цепи.
Тиоловые коферменты
К тиоловым коферментам относится кофермент ацилирования (КоА, CoA, HSCoA), биологическая роль которого заключается в переносе ацильных группировок. Если КоА переносит ацетил СН3СО-, то он называется коферментом ацетилирования (СН3СО – ацетил). В состав КоА входит витамин В3 (пантотеновая кислота).
CH3
|
НО – СН2 – С – СН – С – NH – CH2 – CH2 – COOH
| | ||
CH3 OH O
Пантотеновая кислота (a, g-диокси-b, b¢-диметилбутирил-b-алинан)
 NH2
NH2




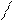





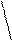

 N N O O CH3 H O
N N O O CH3 H O



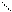




 CH2-O-P-O-P-O-CH2-C-C-C-NH-CH2-CH2-C
CH2-O-P-O-P-O-CH2-C-C-C-NH-CH2-CH2-C
OH OH CH3 OH O NH2
 N N O |
N N O |
| Пирофосфат CH2

 H H |
H H |
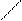 OH CH2
OH CH2
 OH O – P = O b-аминоэтантиол |
OH O – P = O b-аминоэтантиол |
OH SH
Аденозин-3-фосфат
Ацильные группы переносятся КоА за счет сложноэфирной связи с тиоловой группой – SН кофермента А.
Биологическая роль кофермента ацилирования:
1. КоА является ключевым веществом промежуточного метаболизма, переносчиком СН3СО-, которые вступают в цикл Кребса для окисления до Н2О и СО2 и генерации энергии.
2. Является коферментом активирования кислот – жирных кислот до аминокислот.
 2015-10-14
2015-10-14 4894
4894








