Обозначим:
a – исходная молярная концентрация гидроксида натрия в исследуемой системе, моль/дм3;
b – исходная молярная концентрация сложного эфира в исследуемой системе, моль/дм3;
x – молярная концентрация ацетата натрия в момент времени t, моль/дм3;
Va – аликвотная часть исследуемой системы, взятая для титрования t, см3;
V o – объем раствора гидроксида натрия, пошедший на титрование избытка кислоты, добавленной к аликвотной части исследуемой системы в момент времени t = 0, см3;
Vt – объем раствора гидроксида натрия, пошедший на титрование избытка кислоты, добавленной к аликвотной части исследуемой системы в момент времени t, см3;
V ¥ – объем раствора гидроксида натрия, пошедший на титрование избытка кислоты, добавленной к аликвотной части исследуемой системы после окончания реакции, см3;
сщ – молярная концентрация гидроксида натрия в титранте, моль/дм3.
Vк – объем раствора кислоты, добавленный к пробе, см3;
с (Н+) – молярная концентрация эквивалента кислоты в исходном растворе, моль/дм3.
Рассчитывают молярные концентрации всех участников реакции (таблица 7.2), исходя из следующих соотношений:
|
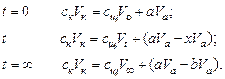
Изображают зависимости молярных концентраций всех участников реакции от времени.
Таблица 7.2 – Молярные концентрации сложного эфира, гидроксида натрия, ацетата натрия и этилового спирта
| Время | Объем титранта | Молярные концентрации с (Х), моль/дм3 | Константа скорости реакции, с-1×моль-1×дм3 | |||||
| t, с | Vщ, см3 | R1COOR2 | NaOH | R1COONa | R2OH | k | 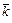
| 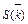
|
 2015-10-22
2015-10-22 388
388








