3.3.1Молекулярно-ионные уравнения обменных реакция.
Пример 1. Составление молекулярно-ионных уравнений между сильными электролитами.
Напишите в молекулярной и молекулярно-ионной формах реакции взаимодействия между следующими вещества: а)  и
и 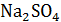 ;
;
б) 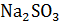 и HCL.
и HCL.
Решение. Обменные реакции между электролитами практически необратимы и идут до конца в случае образования малорастворимых, мало диссоциирующих и газообразных соединений. При составлении молекулярно-ионных уравнений реакций надо помнить о том, что малорастворимые, малодиссоциирующие и газообразные вещества записывают в виде молекул, а сильные электролиты в виде тех ионов, на которые они диссоциируют. Тогда реакции взаимодействия между названными веществами в молекулярно-ионном виде можно записать следующим образом:
а) 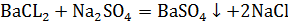
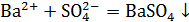
б) 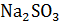 +2HCl=2NaCl+
+2HCl=2NaCl+ 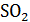 +
+ 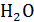
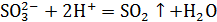
Пример 2. Составление молекулярно-ионных уравнений реакций обмена, если среди исходных веществ есть малорастворимые и слабодиссоциирующие вещества.
Напишите в молекулярно-ионном виде реакции взаимодействия между: а) Гидроксидом аммония и соляной кислотой.
Решение. Если исходными веществами реакции являются малодиссоциирующие или малорастворимые вещества, то кроме реакций связывания тех или иных ионов этих электролитов протекают реакции постепенной диссоциации слабого электролита или перехода ионов малорастворимого электролита в раствор. Итак, молекулярно-ионные уравнения:
а) 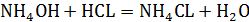

Пример 3. Сoставление молекулярных уравнений реакций к молекулярно-ионным уравнениям.
Дано краткое ионное уравнение:  Составьте по нему возможные молекулярно-ионные уравнения.
Составьте по нему возможные молекулярно-ионные уравнения.
Решение. В левой части молекулярно-ионного уравнения указаны свободные ионы 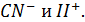 Эти иoны образуются при диссоциации каких-либо растворимых сильных электролитов. Ионы
Эти иoны образуются при диссоциации каких-либо растворимых сильных электролитов. Ионы 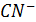 могут орбазовываться при диссоциации, например, KCN, NaCN, LiCN; поставщиками ионов
могут орбазовываться при диссоциации, например, KCN, NaCN, LiCN; поставщиками ионов 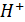 могут быть любые сильные кислоты.
могут быть любые сильные кислоты.
Молекулярные уравнения реакций, которым отвечает данное молекулярно-ионное уравнение, могут быть:
1) 
2) NaCN + HN 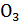 =Na
=Na 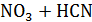
3) 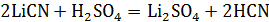
 2017-11-30
2017-11-30 454
454








