Устойчивость равновесных состояний относительно малых отклонений от равновесия может быть исследована с помощью термодинамических неравенств (5.1). Введя с помощью преобразований Лежандра свободную энергию Гельмгольца F и свободную энергию Гиббса Φ (см.(5.4)), получим следующую систему неравенств:
 (5.10)
(5.10)
откуда следует, что каждый из термодинамических потенциалов неравновесной системы уменьшается при поддержании постоянными пары соответствующих ему "естественных" переменных и в равновесии принимает минимальное значение. Так, например, если в неравновесной системе поддерживаются постоянными температура и давление, то свободная энергия Гиббса такой системы уменьшается и в равновесии принимает минимальное значение. Примерами таких процессов являются многие химические реакции и фазовые переходы. При этом неравенства (5.10) при известных зависимостях потенциалов от параметров и концентраций фаз или компонентов позволяют установить условия химического или фазового равновесия и исследовать устойчивость равновесных состояний.
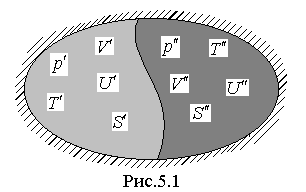
В качестве примера получим условия термодинамического равновесия однофазной изолированной системы. Разобьём мысленно систему на две подсистемы (') и (") (см. рис.5.1), для каждой из которых известны все термодинамические параметры, причём для аддитивных параметров будем иметь
 |
 . (5.11)
. (5.11) Температуры 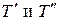 и давления
и давления  для каждой из подсистем не являются аддитивными величинами и потому определяться суммированием для всей системы не могут. Для каждой из подсистем, находящихся в состоянии равновесия, запишем уравнения Гиббса:
для каждой из подсистем не являются аддитивными величинами и потому определяться суммированием для всей системы не могут. Для каждой из подсистем, находящихся в состоянии равновесия, запишем уравнения Гиббса:

Просуммируем почленно эти два выражения:
 (5.12)
(5.12)
С другой стороны, для изолированной равновесной системы имеем 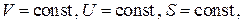 т.е. с учётом (5.11) получаем
т.е. с учётом (5.11) получаем
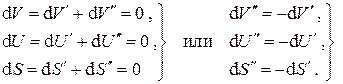
Подставляя эти выражения в (5.23), имеем

Ввиду произвольности значений дифференциалов  , из последнего выражения находим условия термодинамического равновесия изолированной системы:
, из последнего выражения находим условия термодинамического равновесия изолированной системы:
 (5.13)
(5.13)
 2017-10-25
2017-10-25 1134
1134
