Первый закон Рауля:
Давление пара, содержащего нелетучее растворенное вещество, прямо пропорционально молярной доле растворителя.
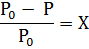
Где  - давление насыщенного пара чистого растворителя при данной температуре
- давление насыщенного пара чистого растворителя при данной температуре
P- давление насыщенного пара растворителя над раствором
X- мольная доля растворенного вещества.
(мольная доля растворённого вещества – это отношение количества растворённого вещества к общему количеству растворённого вещества и растворителя)
Из первого закона Рауля вытекает, что растворы нелетучих веществ должны кипеть при более высокой температуре и отвердевать при более низкой по сравнению с чистым растворителем.
Давление насыщенного пара - это давление пара, находящегося в равновесии с жидкостью.
При данной температуре давление насыщенного пара чистого растворителя – величина постоянная и является термодинамической характеристикой растворителя. При повышении температуры р0 над растворителем возрастает в соответствии с принципом Ле Шателье, так как испарение – процесс эндотермический. (∆Ниспар. => 0).
 2018-01-21
2018-01-21 1573
1573
