Ненасичені вуглеводні – вуглеводні, в молекулах яких атоми Карбону сполучені одним або кількома кратними зв’язками.
Лекція 1.
Алкени
Визначення:
Алкени (олефінами) – вуглеводні, молекули яких мають відкритий карбоновий ланцюг з одним подвійним зв’язком та мають закінчення «-ен»
Загальна формула CnH2n
Будова
Найпростішим представником етиленових вуглеводнів, її родоначальником є етилен (етен) С2Н4
 Електронна формула:
Електронна формула:
 Структурна формула:
Структурна формула:
За назвою першого представника цього ряду - етилену - такі вуглеводні називають етиленових.
В етиленових вуглеводнях (алкенів) атоми вуглецю знаходяться в стані sр2-гібрідизації. Між вуглецевими атомами виникає подвійний зв'язок, що складається з однієї ς і однієї π-зв'язку. Довжина і енергія подвійного зв'язку дорівнюють відповідно 0,134 нм та 610 кДж / моль. Різниця в енергіях ς -і π-зв'язків (610 - 350 = 260) є приблизною мірою, що характеризує міцність π-зв'язку.
Ізомерія
Ізомерія обумовлена:
1. Будовою карбонового ланцюга
2. Розміщенням подвійного зв’язку в карбоновому ланцюзі
3. Різним розміщенням замісників відносно π-зв’язку, характерна цис-транс-ізомерія.
Фізичні властивості
Перші три представники гомологічного ряду алкенів (етилен, пропілен і бутилен) - гази, починаючи з C5H10 (Амілі, або пента-1) - рідини, а з С18Н36 - тверді речовини. Зі збільшенням молекулярної маси підвищуються температури плавлення і кипіння. Алкени нормальної будови киплять при більш високій температурі, ніж їх ізомери, що мають ізостроення. Температури кипіння цис-ізомерів вище, ніж транс-ізомерів, а температури плавління - навпаки.
Алкени погано розчиняються у воді (проте краще, ніж відповідні алкани), але добре - в органічних розчинниках. Етилен і пропілен горять коптить полум'ям.
Хімічні властивості
1. Реакція гідрування

2. Реакція Вагнера (окиснення перманганатом Калію у лужному середовищі)

3. Реакції окиснення перманганатом Калію у кислому середовищі

4. Реакції приєднання HBr і HCl
Обґрунтування: У молекулі пропілену за рахунок індукційного ефекту електронна кустина зміщена від атому Карбона метильної групи до атому Карбону подвійного зв’язку. Н в свою чергу, зумовлює зміщення електронної хмари π-зв’язку, яка є досить рухливою до крайнього атома Карбону, сполученою подвійним зв’язком.
Внаслідок цього електронна хмара подвійного зв’язку поляризується і на атомах Карбону, сполучених цим зв’язком виникають часткові заряди. Отже, подвійний зв’язок у молекулі пропілену під впливом метальної групи поляризується.
У зв’язку з цим полярні речовини, наприклад, галоген оводні приєднуються до пропілену відповідно до поляризації його подвійного зв’язку.
А) Правило Марковникова: У результаті приєднання галогеноводнів до несиметричних алкенів Гідроген приєднується до найбільш гідрогенізованого атому Карбону.

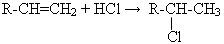
(каталізатор Н2О2)
Б) Проти правила Марковникова: перекісний ефект Хараша
5. Реакції приєднання Br2 і Cl2

6. Реакції приєднання води (за правилом Марковникова)

7. Реакції полімеризації

Добування
Промислові методи
1. Крекінг алканів нафти

Лабораторні методи
1. Дегідратація спиртів відбувається за правилом Зайцева, яке протилежне до правила Марковникова:

| NaOH C2H5OH |

3. Відщеплення галогенів (-Cl,-Br)

*для цієї реакції використовують спиртовий розчин цинку
| + Н2 |

(каталізатор Pd/PbO)
Застосування:
· Алкени застосовуються в якості вихідних продуктів у виробництві полімерних матеріалів (пластмас, каучуків, плівок) та інших органічних речовин.
· Етилен використовується для отримання поліетилену, політетрафторетилену (тефлону) етилового спирту, оцтового альдегіду, галогенопохідних і багатьох інших органічних сполук. Застосовується як засіб для прискореного дозрівання фруктів.
· Пропілен і Бутілени використовуються для отримання спиртів і полімерів.
Ізобутилен застосовується у виробництві синтетичного каучуку.
· Один з небагатьох природних алкенов - мускалур (ціс -трикозен-9) є статевим атрактантом самки домашньої мухи
Лекція 2.
 2018-01-21
2018-01-21 717
717








