Вода, являясь весьма слабым электролитом, в очень малой степени диссоциирует на ионы:
H2О ↔ H+ +OH-
Применим к этому обратимому процессу закон действующих масс.
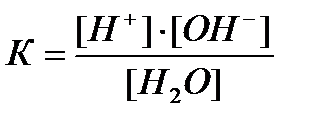 ,
,
где К – константа диссоциации воды, которую можно вычислить, например, используя значения электрической проводимости. При 22°С К = 1,8·10-16.
Так как вода диссоциирует крайне мало, то в уравнении концентрацию воды [Н2О] можно считать величиной постоянной. Численно [Н2О]=1000/18=55,56 моль/л. Уравнение можно переписать так:
K [H2О] = [H+][OH-] = Kв
К в – постоянная величина – называется ионным произведением воды. Подставляя значения К и [H2O] в уравнение, получаем численное значение ионного произведения воды при 22 °С:
Kв = [Н+] [ОН-] = 1,8·10-16·55,56 = 10-14.
Значит, K в = [H+][OH-] = 10-14
К в – величина постоянная при постоянной температуре.
 2018-01-21
2018-01-21 934
934








