Валентность — это способность атомов отдавать или присоединять определённое число электронов.
Степень окисления - это условный заряд атома в молекуле, вычисленный в предположении, что молекула состоит из ионов и в целом электронейтральна.
Наиболее электроотрицательные элементы в соединении имеют отрицательные степени окисления, а атомы элементов с меньшей электроотрицательностью - положительные.
Например:
N2H4 (гидразин)
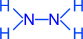 степень окисления азота – -2; валентность азота – 3.
степень окисления азота – -2; валентность азота – 3.
Дайте определение понятия «окислительно-восстановительные реакций». Приведите пример.
Реакции, в которых происходит изменение степеней окисления атомов элементов, входящих в состав реагирующих соединений называются окислительно - восстановительными.
2Mg0 + O20 = 2Mg+2O-2
Дайте определение понятий «окислитель», «процесс восстановления». Ответ подтвердите примерами.
Атомы или ионы, которые в данной реакции присоединяют электроны являются окислителями.
Процесс присоединения электронов - восстановление: При восстановлении степень окисления понижается.
Mn+4 + 2ē = Mn+2
Дайте определение понятий «восстановитель», «процесс окисления». Ответ подтвердите примерами.
Атомы или ионы, которые в данной реакции отдают электроны являются восстановителями
В окислительно-восстановительных реакциях электроны от одних атомов, молекул или ионов переходят к другим. Процесс отдачи электронов - окисление. При окислении степень окисления повышается:
H20 - 2ē = 2H+
Дайте определение понятия «гальванический элемент». Приведите пример работающего гальванического элемента.
ГЭ –называются ус-ва, в которых энергия хим. р-ций преобразуется в электрическую. Состоит из двух полуэлементов, одним из которых является анод, а другой катод.
А(-) Zn | ZnSO4 || CuSO4 | Cu, К(+)
А(-):Zn - 2e = Zn2+
К(+):Cu2+ + 2e = Cu
Токообразующая реакция: Cu2+ + Zn = Cu + Zn2+
Zn+ CuSO4 = ZnSO4 + Cu
 2018-01-21
2018-01-21 780
780








