Химические процессы, сопровождаемые качественными изменениями, показывают что исчезают одни вещества и образуются другие. Происходящая при этом перестройка электронных структур атомов, молекул, сопровождается энергетическим эффектом, т. е. выделением или поглощением энергии.
Внутренняя энергия системы- полная энергия системы, которая складывается из энергии движения полекул, ядер и электронов в атомах и молекулах, а также из энергий межмолекулярного взаимодействия. Запас внутренней энергии зависит от природы вещества, массы тела и параметров состояния системы. При химических реакциях должна выделяться или поглощаться энергия. В химических процессах под такой энергией понимается выделение или поглощение теплоты. Эта теплота называется тепловым эффектом реакции. Тепловой эффект зависит от условий протекания реакции.
Рассмотрим систему, состоящую из цилиндра, в котором находится поршень(поршень поднимаем, увеличивается объем газа).
Поглощенная теплота расходуется на изменение внутренней энергии  и на завершение работы против внешних сил, т. е. работа расширения газа.
и на завершение работы против внешних сил, т. е. работа расширения газа.
Первый закон термодинамики:Теплота, подводимая к системе расходуется на изменение внутренней энергии и совершение работы данной системы.l

Для химической реакции под работой внешних сил подразумевается работа против внешнего давления 
15) Виды термодинамических процессов. Определение теплового эффекта при р=соnst и v=const. Понятия экзо- и эндо-эффектов.
Изохорный процесс Qv=∆U
Изобарный процесс Qp=∆U+p∆V=(U2+pV2)-(U1+pV1)=H2-H1
H2 и H1 – энтальпия, т. е. теплосодержание системы.
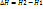
Реакции, сопровождаемые выделением теплоты называются экзотермическими. При таких реакциях  и +Q
и +Q
Реакции, сопровождаемые поглощением теплоты из вне, называются эндотермическими 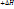 и –Q
и –Q
 2018-01-21
2018-01-21 566
566








