Существуют два метода составления окислительно - восстановительных реакций - метод электронного баланса и метод полуреакций.
В метод электронного баланса сравнивают степени окисления атомов в исходных веществах и в продуктах реакции, при этом руководствуемся правилом: число электронов, отданных восстановителем, должно равняться числу электронов, присоединённых окислителем.
Расставить коэффициенты в реакции, схема которой:
HCl + MnO2 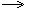 Cl2 + MnCl2 + H2O
Cl2 + MnCl2 + H2O
1.Указываем степени окисления химических элементов.

2.Составляем электронные уравнения, в которых указываем число отданных и принятых электронов.

За вертикальной чертой ставим число электронов, перешедших при окислительном и восстановительном процессах. Находим наименьшее общее кратное (взято в красный кружок). Делим это число на число перемещённых электронов и получаем коэффициенты (взяты в синий кружок). Значит перед марганцем будет стоять коэффициент-1, который мы не пишем, и перед Cl2 тоже -1.
Перед HCl коэффициент 2 не ставим, а считаем число атомов хлора в продуктах реакции. Оно равно - 4.Следовательно и перед HCl ставим - 4,уравниваем число атомов водорода и кислорода справа, поставив перед H2O коэффициент - 2. В результате получится химическое уравнение: 
Метод полуреакции применяется для составления уравнения ОВР, протекающих в растворах.
 2018-01-21
2018-01-21 659
659








